Clear Sky Science · nl
Misbruik van verslavende drugs en depressie - een focus op epigenetica
Waarom dit onderzoek van belang is voor het dagelijks leven
Verslavende drugs en depressie worden vaak als afzonderlijke problemen gezien, maar ze komen veelvuldig samen voor bij dezelfde persoon. Deze review legt uit hoe langdurig gebruik van middelen zoals methamfetamine, cocaïne, opioïden en cannabis blijvende "moleculaire littekens" in de hersenen kan achterlaten die het risico op depressie verhogen. Door deze verborgen veranderingen bloot te leggen, wijst het artikel op toekomstige tests die kunnen waarschuwen wie het meest kwetsbaar is — en op nauwkeurigere behandelingen die de schade mogelijk kunnen omkeren in plaats van alleen symptomen te maskeren.
Hoe verslaving en sombere stemming verstrengeld raken
De auteurs beginnen met het schetsen van de nauwe klinische verbinding tussen drugsmisbruik en depressie. Mensen die herhaaldelijk verslavende stoffen gebruiken melden veel vaker aanhoudende droefheid, verlies van plezier, slaapproblemen en suïcidale gedachten. Hersengebieden die beloning, motivatie, geheugen en besluitvorming regelen — de ventrale tegmentale area, nucleus accumbens, prefrontale cortex en hippocampus — spelen een centrale rol bij beide aandoeningen. Chronische blootstelling aan drugs verstoort hersenchemie zoals dopamine en serotonine, stresshormonen gestuurd door de hypothalamus-hypofyse-bijnier-as, immuunsignalen en de energievoorziening van neuronen. Samen maken deze veranderingen de hersenen minder veerkrachtig tegenover stress en gevoeliger voor depressieve toestanden, zelfs lang na de laatste dosis.
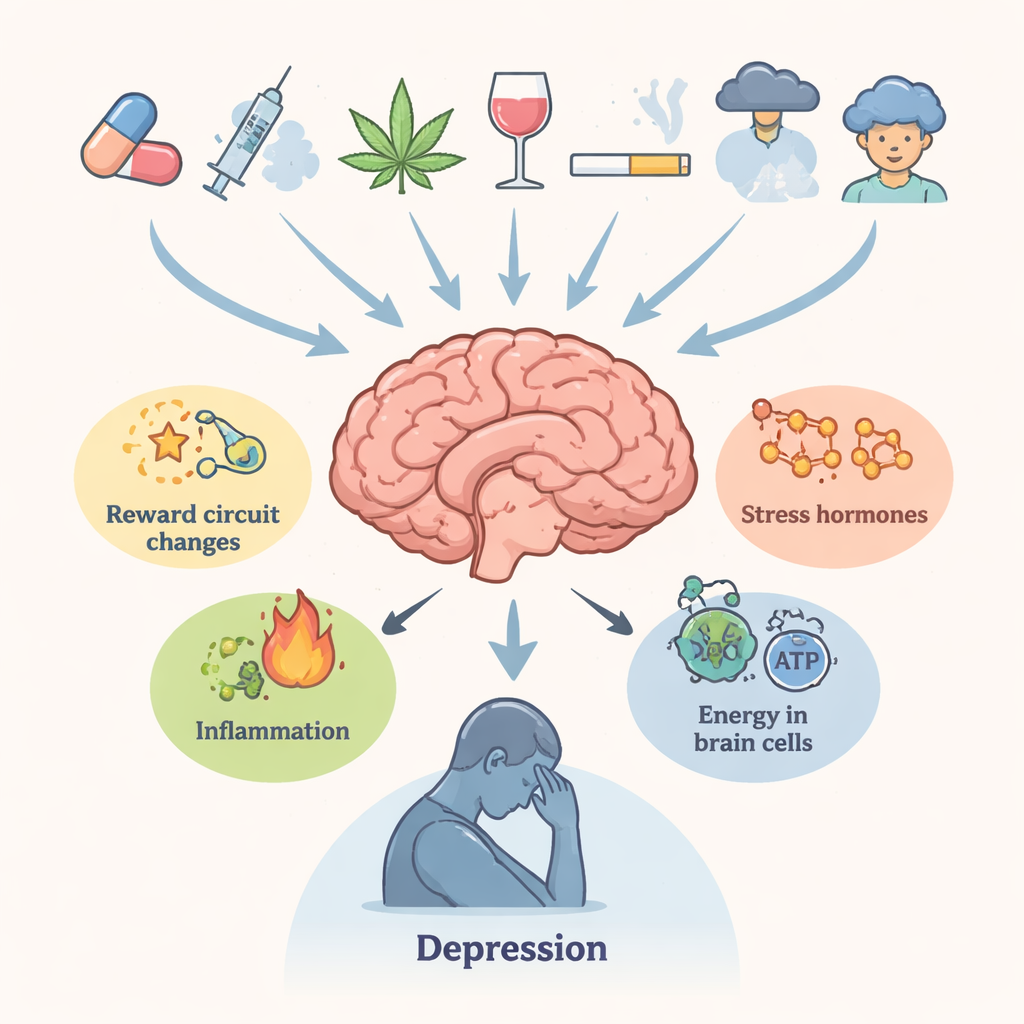
Drugs die de chemie van de hersenen herschikken
De review bespreekt verschillende belangrijke drugsklassen. Amfetamine-achtige stimulerende middelen en aanverwanten, waaronder synthetische "bath salts", veroorzaken krachtige pieken van dopamine en andere boodschappers die na verloop van tijd zenuwuiteinden beschadigen, het glutamaat-evenwicht verstoren, het endoplasmatisch reticulum belasten en cellen aanzetten tot schadelijke zelfvertering (autofagie). Cannabisgebruik tijdens de adolescentie wordt in verband gebracht met latere depressie en suïciderisico, waarschijnlijk via langdurige veranderingen in cannabinoïde-receptoren, de structuur van wit stof en de gevoeligheid van dopaminecircuitry. Opioïden, hoewel pijnverlichtend, kunnen ontsteking, mitochondriale falen en verminderde groeiondersteunende signalen zoals brain-derived neurotrophic factor (BDNF) veroorzaken. Cocaïne activeert herhaaldelijk het stresssysteem en verandert sleutelregulatoren zoals FKBP5, wat bijdraagt aan angst en sombere stemming tijdens onthouding. In elk geval blijven de biologische verstoringen vaak bestaan, wat helpt verklaren waarom emotionele klachten de duidelijke intoxicatie kunnen overleven.
Epigenetica: het geheugen van blootstelling
Om te begrijpen waarom de effecten van drugs aanhouden, richten de auteurs zich op epigenetica — chemische labels en moleculaire schakelaars die genactiviteit aanpassen zonder de DNA-letters te veranderen. Verslavende drugs wijzigen DNA-methylatie (een markering op cytosinebasen), brengen chemische groepen aan op histon-eiwitten die DNA verpakken, en wijzigen niet-coderende RNA's die fijnafstellen welke eiwitten worden geproduceerd. Bijvoorbeeld verschuiven methamfetamine en cocaïne methylatiepatronen in beloningsgerelateerde hersengebieden, waardoor de niveaus van enzymen die deze markeringen toevoegen of verwijderen veranderen. Opioïden en stimulerende middelen herschikken histonacetylatie en -methylatie op genen die glutamaatreceptoren, stresssignalisatie en synaptische structuur beheersen. Tientallen microRNA's, lange niet-coderende RNA's en circulaire RNA's nemen toe of af bij drugsexpositie en beïnvloeden gezamenlijk ontsteking, neuronale groei en de sterkte van synapsen. Deze epigenetische veranderingen functioneren als een moleculair "geheugen" van iemands drugsgeschiedenis.
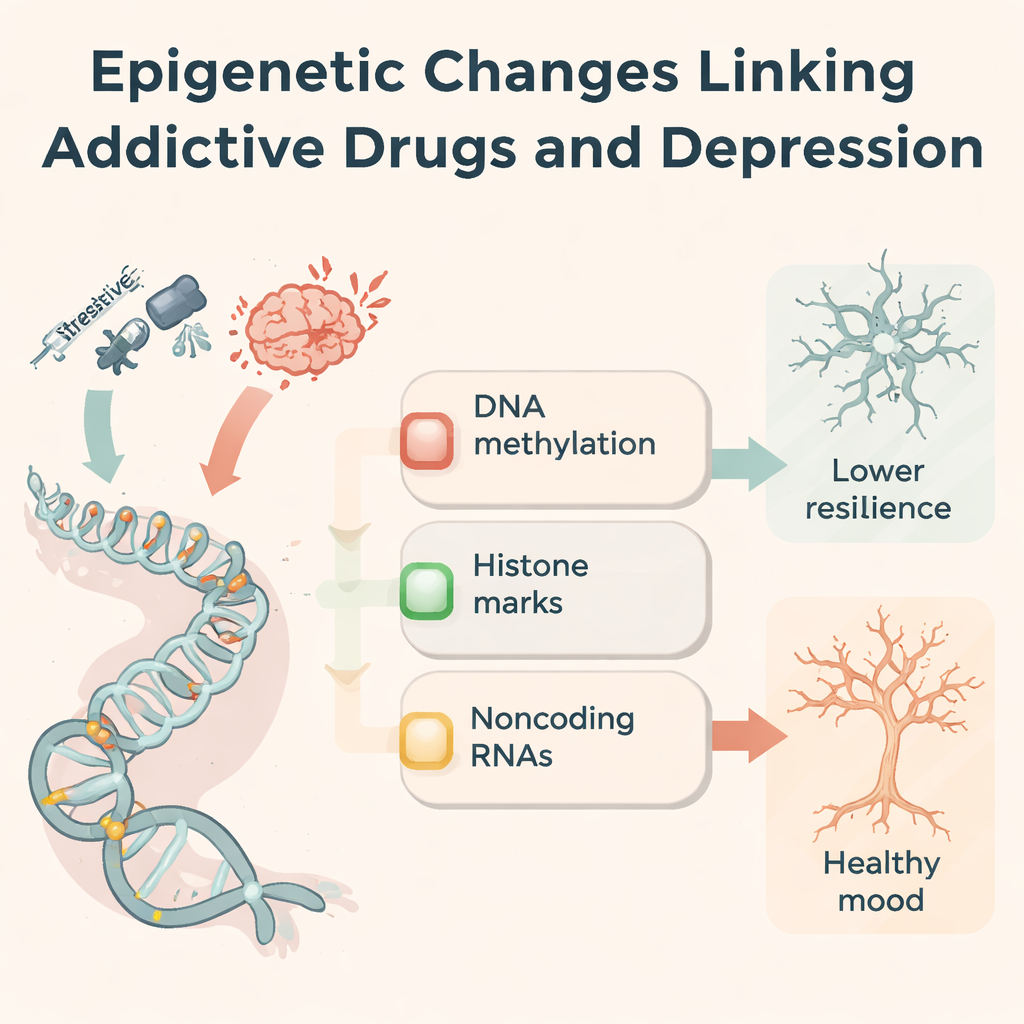
Gedeelde moleculaire routes bij depressie en verslaving
Dezelfde epigenetische mechanismen blijken ook aanwezig te zijn bij mensen en dieren met depressie die nooit drugs hebben gebruikt. Stressvolle ervaringen kunnen de methylatie van stresshormoonreceptoren (zoals NR3C1 en FKBP5) veranderen, behulpzame groeifactoren zoals BDNF verminderen, en immuun- en glutamaatroutes opnieuw bedraden. Veel van dezelfde niet-coderende RNA's die door drugs veranderen, zijn ook ontregeld bij depressie, wat invloed heeft op hoe nieuwe neuronen ontstaan, hoe microglia reageren op ontsteking en hoe sterk synapsen verbinden. De auteurs stellen een driedelig kader voor: regulatie van stressreactie, herstructurering van beloningscircuitry en synaptische plasticiteit. Over deze assen convergeren verslaving en depressie herhaaldelijk op een kleine set genen en markeringen, wat een biologische verklaring biedt voor waarom beide stoornissen zo vaak samen voorkomen.
Wat dit betekent voor toekomstige preventie en behandeling
Afsluitend betogen de auteurs dat epigenetische veranderingen vroege waarschuwingsbiomarkers en doelwitten voor volgende generatie behandelingen kunnen worden. Breedwerkende middelen die epigenetische markeringen wissen hebben in dieren al enkele antidepressiefachtige effecten getoond, maar zijn te grof voor routinematig gebruik bij mensen. Nieuwe instrumenten — zoals CRISPR-gebaseerde epigenoomeditors en therapieën die specifieke microRNA's of lange RNA's moduleren — kunnen op den duur probleembedragsgenen in bepaalde hersencellen aanpassen zonder andere cellen te treffen. De auteurs waarschuwen dat de meeste huidige gegevens afkomstig zijn van knaagdieren en bulk hersenweefsel, en dat menselijke biologie complexer is. Toch biedt dit werk, door te laten zien hoe verslavende drugs en depressie in hetzelfde moleculaire "notitieboek" schrijven, een hoopvolle weg naar meer gepersonaliseerde en duurzame therapieën.
Bronvermelding: Zhang, W., Xu, M., Wang, C. et al. Addictive drug abuse and depression-a focus on epigenetics. Commun Biol 9, 297 (2026). https://doi.org/10.1038/s42003-026-09705-9
Trefwoorden: verslaving en depressie, epigenetica, drugsmisbruik, DNA-methylatie, niet-coderend RNA