Clear Sky Science · nl
Proof-of-principle van NF1-gentherapie in xenograft-muismodellen voor plexiforme neurofibromen
Waarom dit onderzoek ertoe doet
Mensen met de erfelijke aandoening neurofibromatose type 1 (NF1) ontwikkelen vaak grote, ontsierende zenuwtumoren die plexiforme neurofibromen worden genoemd. Deze gezwellen kunnen pijn, bewegingsproblemen en grote cosmetische zorgen veroorzaken, terwijl de huidige behandelingen beperkt zijn en chirurgie vaak onmogelijk. Omdat NF1 wordt veroorzaakt door veranderingen in een enkel gen, hoopten veel onderzoekers dat gentherapie — het herstellen of vervangen van het defecte gen — deze tumoren ooit zou kunnen doen krimpen of zelfs verwijderen. Deze studie biedt een vroege maar krachtige toets van dat idee in muizen en stelt een eenvoudige vraag met grote implicaties: als u het ontbrekende NF1-gen in gevestigde tumoren herstelt, verdwijnen ze dan?
Een realistisch tumormodel in muizen opbouwen
De onderzoekers hadden eerst een laboratoriumsysteem nodig dat plexiforme neurofibromen bij mensen nauwkeurig nabootst. Ze gebruikten menselijke Schwanncellen, de ondersteunende cellen die normaal rond zenuwen liggen, afkomstig van een patiënt waarvan de cellen beide werkende kopieën van het NF1-gen hadden verloren. Deze cellen werden naast beschadigde ischiaszenuwen in immuungecompromitteerde muizen geplaatst. In de loop van weken ontwikkelden de zenuwen consequent verdikt, sterk cellulair weefsel met een ongeordende structuur en dichte collageenbundels — kenmerken van plexiforme neurofibromen. Controle-operaties zonder deze NF1-deficiënte cellen, of met cellen die slechts één defecte NF1-kopie hadden, vormden niet betrouwbaar tumoren. Dit toonde aan dat de menselijke cellen met volledig NF1-verlies de tumorgroei aandreven en een robuust, snel model van de ziekte creëerden.
NF1 weer inschakelen in tumorcellen
Met dit model ontwikkelde het team de tumorvormende Schwanncellen zodanig dat ze een schakelbare versie van het muizen-NF1-gen droegen. De schakel reageerde op het veelgebruikte antibioticum doxycycline: wanneer de muizen water met doxycycline dronken, werd het toegevoegde NF1-gen in de geïmplanteerde cellen geactiveerd. Muizen kregen eerst de tijd om tumoren te ontwikkelen, en pas daarna werd het gen ingeschakeld. De resultaten waren opvallend. Bij dieren waarbij NF1 uit bleef, huisvestten de meeste ischiaszenuwen nog steeds neurofibromen. Daarentegen zagen de meeste zenuwen er onder de microscoop normaal uit wanneer NF1 werd geheractiveerd, en chemische markers van overactieve groeisignalisatie waren sterk verminderd. In wezen duwde het terugschakelen van NF1 tumorgeweefsel weer richting een gezonde zenuwtoestand.
NF1-verlies op een tweede manier terugdraaien
Om te laten zien dat dit effect niet beperkt was tot één technische truc, bouwden de wetenschappers een tweede, aanvullende model. Ditmaal begonnen ze met menselijke Schwanncellen die slechts één beschadigde NF1-kopie hadden — vergelijkbaar met wat mensen met NF1 in al hun cellen erven. Ze voegden een genetische schakel toe die de resterende NF1-activiteit tijdelijk kon verlagen wanneer doxycycline aanwezig was. Toen muizen doxycycline dronken, daalden de NF1-niveaus verder en vormden tumoren zich eenvoudig. Cruciaal was dat, wanneer doxycycline werd verwijderd nadat tumoren zich hadden gevormd, de NF1-niveaus weer stegen en veel zenuwen naar een meer normale structuur terugkeerden. Ook hier daalden maten voor groeigerelateerde signalisatie in de zenuwen die normaliseerden. Samen wijzen deze twee tegengestelde schakelstrategieën — NF1 inschakelen of diens onderdrukking opheffen — op dezelfde conclusie: het herstellen van NF1 in tumorcellen kan gevestigde ziekte ongedaan maken.
Een realistischer afleveringsmethode testen
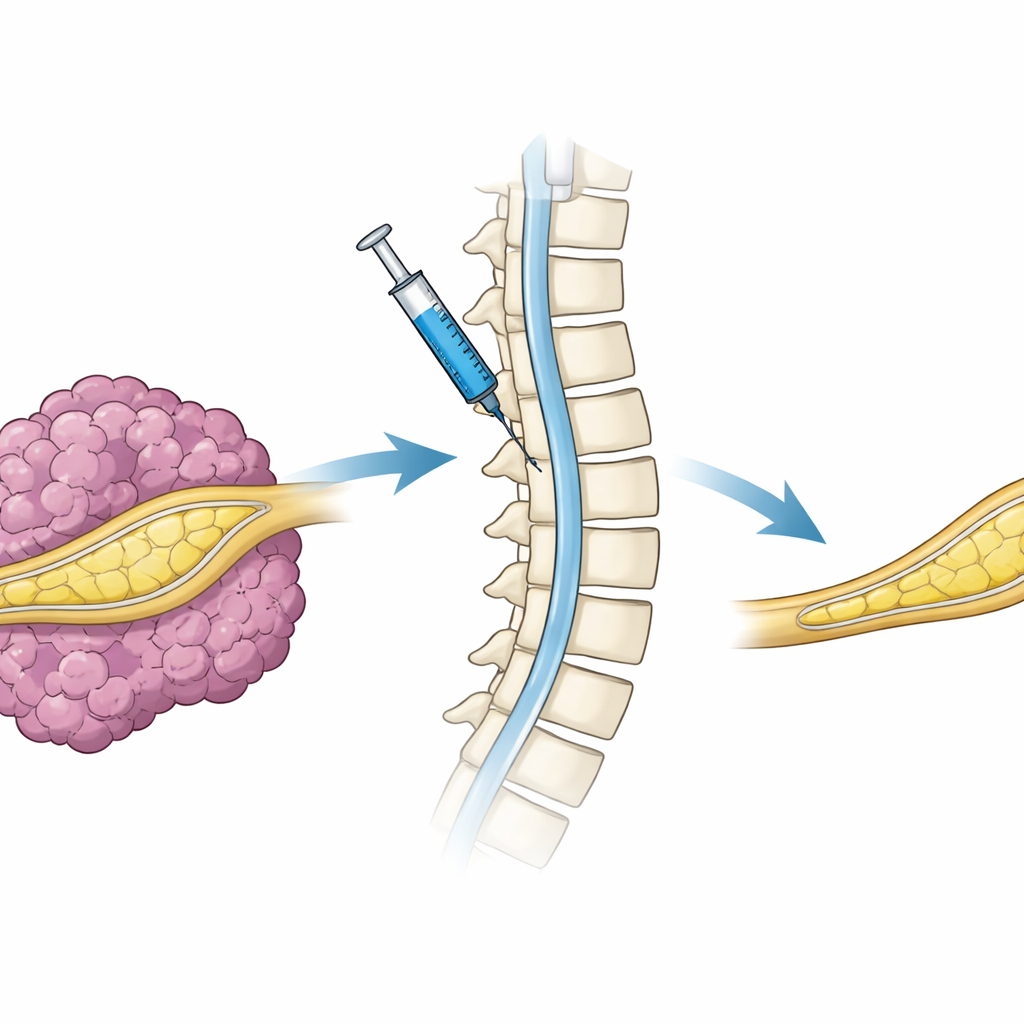
Naast genetische schakelaars ingebouwd in cellen in het laboratorium zou een echte therapie een werkend NF1-gen in het zenuwstelsel van een levend patiënt moeten afleveren. Om deze stap te onderzoeken verpakte het team het volledige NF1-gen in een lentivirale vector en injecteerde deze in de vloeistofruimte rond het ruggenmerg van muizen met tumoren, een route die bekendstaat als intrathecale toediening. De dieren kregen vervolgens doxycycline zodat het afgeleverde gen zou worden geactiveerd. In vergelijking met muizen die een controlevirus kregen, ontwikkelden degenen die behandeld waren met het NF1-bevattende virus aanzienlijk minder tumoren en leek hun zenuwweefsel normaler. Hoewel dit een korte, eenmalige proef was, toonde het aan dat NF1-genafgifte via het ruggenmergvocht perifere zenuwen kan bereiken en de tumorlast betekenisvol kan verminderen.
Wat dit werk betekent voor mensen met NF1
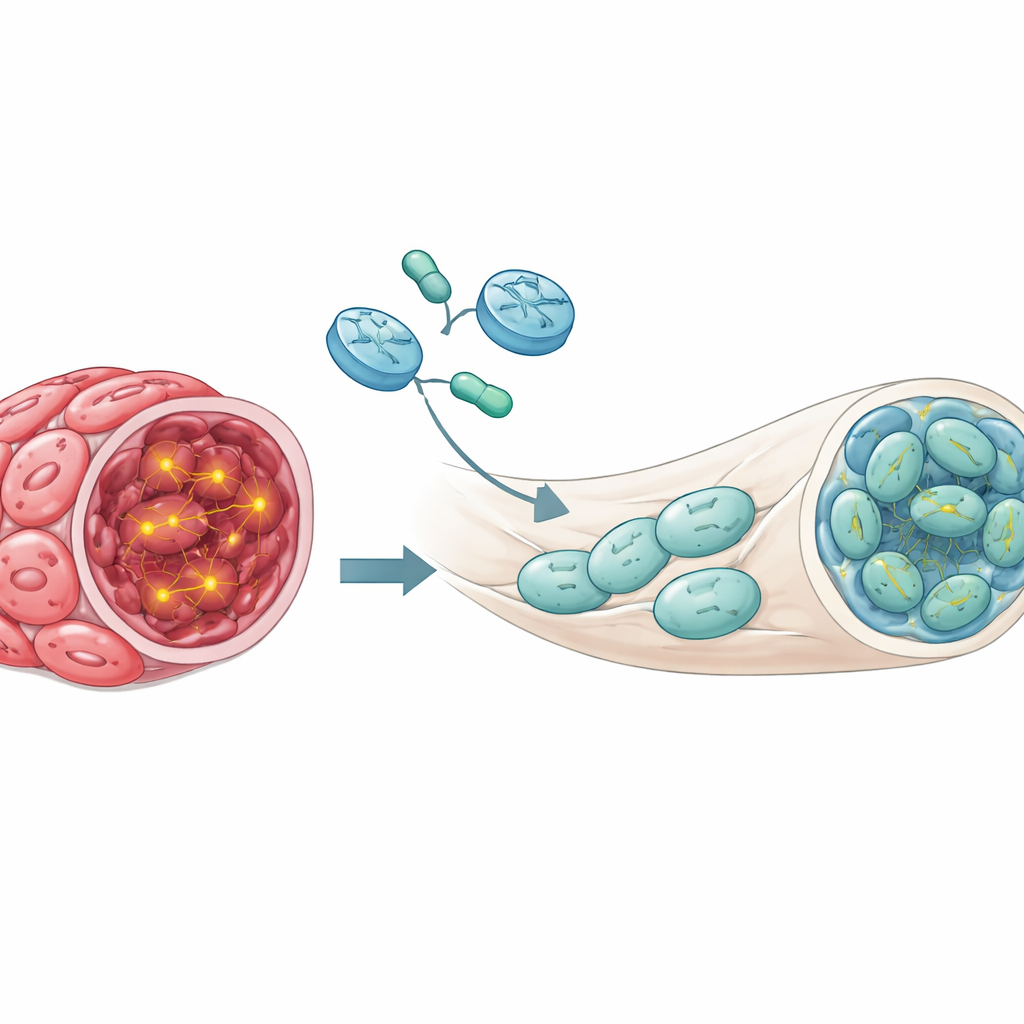
Deze studie biedt nog geen direct inzetbare behandeling voor patiënten, maar beantwoordt een cruciale vraag: in zorgvuldig ontworpen muismodellen die sterk lijken op menselijke plexiforme neurofibromen kan het herstellen van NF1 in tumorcellen gevestigde tumoren doen krimpen of normaliseren. Het werk levert een proof-of-principle dat NF1-gentherapie een plausibele strategie is, niet slechts een theoretische hoop. Er blijven vele uitdagingen — het vinden van de veiligste en meest efficiënte afleveringsmiddelen, bepalen hoeveel NF1-activiteit voldoende is, en het testen van langetermijneffecten in natuurlijkere modellen. Toch leggen deze resultaten een wetenschappelijke basis voor toekomstige gen-gebaseerde behandelingen die hopelijk ooit blijvende verlichting kunnen bieden van plexiforme neurofibromen bij mensen met NF1.
Bronvermelding: Hewa Bostanthirige, D., Plante, C., Caron, M. et al. Proof-of-principle of NF1 gene therapy in plexiform neurofibroma xenograft mouse models. Commun Biol 9, 419 (2026). https://doi.org/10.1038/s42003-026-09695-8
Trefwoorden: neurofibromatose type 1, gentherapie, plexiform neurofibroom, Schwanncellen, lentivirale afgifte