Clear Sky Science · nl
Heterogeniteit tussen VIP- en GRP-neuronen onderliggend aan AVP-receptorsignaalgeving in de suprachiasmatische kern van de muis
Waarom onze biologische klok zo moeilijk te resetten is
Iemand die net van een lange vlucht komt of moeite heeft met nachtdiensten weet dat onze interne klok zich niet goed verzet tegen plotselinge verschuivingen in het schema. Dit artikel stelt een zeer specifieke vraag die centraal staat in dat probleem: waarom ervaren sommige zenuwcellen in de hoofdklok van de hersenen een tijdsignaal sterk, terwijl hun buren het grotendeels negeren? Door een enkel chemisch signaal door dit kleine klokcircuit in muizen te volgen, ontdekken de auteurs een verborgen subgroep cellen die meebepalen hoe hardnekkig onze biologische klok is bij ‘jetlag’. 
Een piepkleine klok met veel verschillende spelers
De hoofdklok bij zoogdieren bevindt zich in een klein hersengebied dat de suprachiasmatische kern (SCN) wordt genoemd. Hoewel het slechts ongeveer 20.000 neuronen bevat, bestaat het uit meerdere onderscheiden groepen die met elkaar communiceren via verschillende chemische boodschappers. Cellen in het bovenste “omhulsel” (shell) geven voornamelijk een boodschapper af die argininevasopressine (AVP) heet, terwijl cellen in het onderste “kern”-gebied vaak andere boodschappers afgeven, waaronder vasoactief intestinaal peptide (VIP) en gastrine-releasing peptide (GRP). Samen moeten deze groepen synchroon blijven om de 24-uursritmes te genereren die slaap, hormoonafgifte en vele andere lichaamsfuncties regelen. Maar welke exacte cellen in de kern luisteren naar signalen van AVP-cellen in de shell was onduidelijk.
De bedrading volgen van zender- naar ontvangercellen
De onderzoekers brachten eerst in kaart hoe shell-AVP-cellen fysiek verbinding maken met VIP- en GRP-cellen in de kern. Ze gebruikten een virus om de uitgaande vezels en mogelijke contactpunten van AVP-neuronen in muizen te labelen en kleurden vervolgens hersenplakjes om te zien waar die vezels eindigden. Ze vonden dat AVP-vezels schijnbare contactplaatsen vormden op zowel VIP- als GRP-cellen, maar in verschillende verhoudingen: ongeveer een kwart van de VIP-cellen en meer dan de helft van de GRP-cellen toonden deze apposities. Dat toonde aan dat AVP-neuronen beide types kerncellen bereiken, maar liet nog niet zien welke ervan daadwerkelijk op het signaal reageren. Om dat te testen gebruikten de onderzoekers optogenetica—AVP-neuronen activeren met blauw licht—en onderzochten ze c-Fos, een merker voor celactivatie, in VIP- en GRP-neuronen.
Een kleine VIP-subgroep die echt "luistert" naar AVP
Wanneer AVP-neuronen door licht werden gestimuleerd, schakelden veel AVP-cellen zelf c-Fos in, zoals verwacht. Belangrijk was dat een kleine subset van VIP-cellen in de kern ook c-Fos-activatie toonde, hoewel zij niet direct het lichtgevoelige eiwit tot expressie brachten. Dit wees erop dat ze indirect door AVP-input werden aangedreven. Daarentegen toonden GRP-cellen zelden c-Fos, ondanks het ontvangen van AVP-contacten. De auteurs zochten vervolgens met gevoelige RNA-beeldvorming naar het genboodschap voor de AVP-receptor bekend als V1a in deze populaties. Ze ontdekten dat V1a slechts in een minderheid van VIP-cellen aanwezig was en nauwelijks detecteerbaar in GRP-cellen. Zo lijkt onder de vele VIP-neuronen een kleine V1a-positieve subgroep speciaal afgestemd om AVP-signalen te ontvangen en erop te reageren, terwijl de meeste GRP-neuronen dat niet doen. 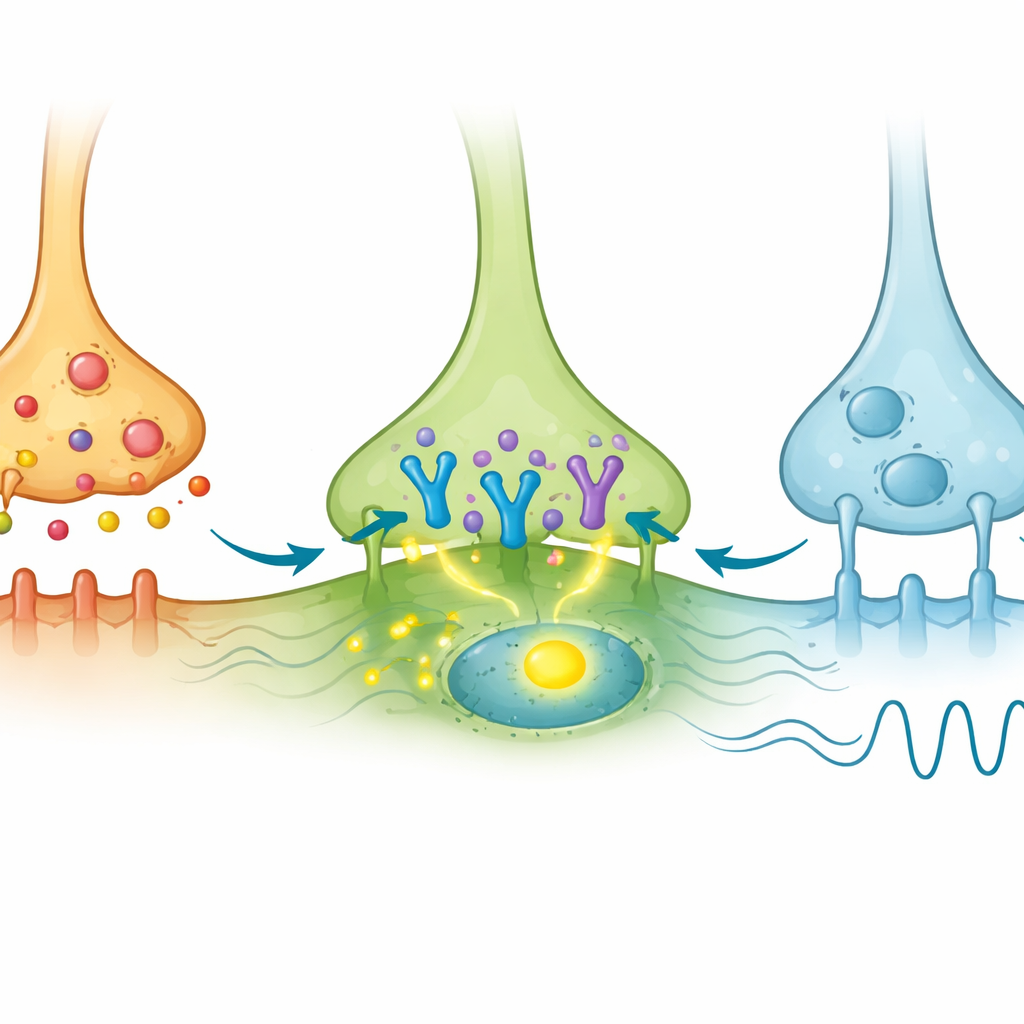
Hoe een kleine cellengroep het herstel van jetlag vormgeeft
Om de functie van deze V1a-bevattende VIP-neuronen te onderzoeken, creëerden de onderzoekers muizen waarbij de V1a-receptor alleen uit VIP-cellen was verwijderd. Deze dieren behielden een normale lengte van het dagelijkse ritme bij constante duisternis, wat aangeeft dat deze receptor in VIP-neuronen niet nodig is om het basale tempo van de klok vast te stellen. Toen het licht-donker-schema echter plotseling met acht uur werd vervroegd of vertraagd om jetlag na te bootsen, pasten de gemodificeerde muizen hun activiteitspatronen sneller aan dan hun normale nestgenoten, vooral na vervroegingen en bij mannelijke muizen. In andere experimenten had het verwijderen van V1a in de hele hersenen of specifiek in de SCN vergelijkbaar ‘jetlagbestendig’ gedrag opgeleverd. De nieuwe resultaten suggereren daarom dat een verrassend kleine groep VIP-neuronen met V1a-receptoren een buitenproportionele invloed kan hebben op hoe star of flexibel de algehele klok is.
Wat dit betekent voor ons tijdsgevoel
In dagelijkse bewoordingen toont deze studie aan dat binnen de centrale klok van de hersenen AVP-producerende neuronen functioneren als tijdhouders in een hogere laag en signalen sturen via V1a-receptoren naar een geselecteerde set VIP-neuronen in de lagere laag. Die paar VIP-cellen helpen het hele netwerk weerstand te bieden tegen plotselinge veranderingen in de licht-donkercyclus en vertragen hoe snel de klok zich na een verschuiving reset. Het verwijderen van hun AVP-gevoelige receptor maakt het systeem ontvankelijker voor verschuivingen, waardoor jetlag-achtige aanpassingen bij muizen worden vergemakkelijkt. Door deze verborgen diversiteit onder klokneuronen in kaart te brengen, levert het werk een gedetailleerder bedradingsoverzicht van hoe ons interne tijdsgevoel wordt gestabiliseerd—en het suggereert dat selectieve aanpassingen van soortgelijke paden bij mensen ooit kunnen helpen bij het beheersen van jetlag of andere ritmestoornissen.
Bronvermelding: Zhou, H., Moriyasu, D., Hsiao, SW. et al. Heterogeneity between VIP and GRP neurons underlies AVP receptor signaling in the mouse suprachiasmatic nucleus. Commun Biol 9, 414 (2026). https://doi.org/10.1038/s42003-026-09694-9
Trefwoorden: circadiaanse klok, suprachiasmatische kern, vasopressine-signaalgeving, VIP-neuronen, jetlag