Clear Sky Science · nl
Mitochondriale energietekorten liggen ten grondslag aan FLVCR1-gerelateerde sensorische neuropathie
Als pijnzenuwen zonder stroom komen te zitten
Sommige mensen worden geboren met vrijwel geen pijngevoel. Op het eerste gezicht lijkt dat een zegen, maar al snel verandert het in een vloek: zonder pijn als waarschuwingssignaal lopen ze brandwonden, breuken, infecties en zelfs blindheid op. Deze studie onderzoekt een zeldzame vorm van zulke pijnverliesstoornissen en onthult een verrassende schuldige: kleine energiecentrales binnen zenuwcellen waarvan de energieproductie ernstig verstoord raakt.
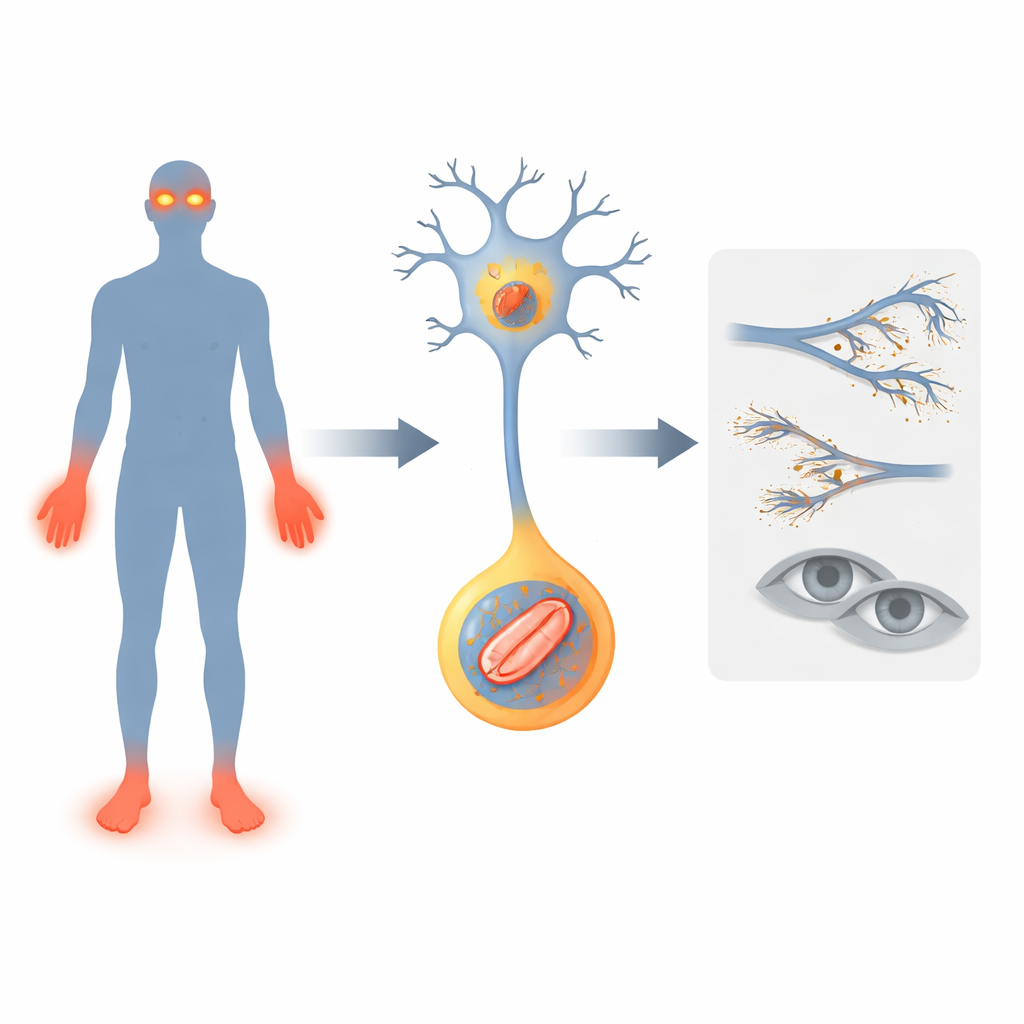
Een gen dat de alarmbellen doet verstommen
De onderzoekers richten zich op een gen genaamd FLVCR1, dat al in verband was gebracht met zeldzame zenuwafwijkingen waarbij mensen hun pijngevoel verliezen, onvast gaan lopen en soms progressief gezichtsverlies ontwikkelen. Ze beschrijven twee nieuwe patiënten met veranderingen in FLVCR1. Beide kinderen vertoonden vroege problemen: vertraagde motorische mijlpalen, frequente vallen, ernstige infecties en mutilatie van vingers en tenen doordat verwondingen onopgemerkt bleven. Eén ontwikkelde bovendien een degeneratieve oogaandoening genaamd retinitis pigmentosa, wat nachtblindheid veroorzaakte. Deze gevallen verbreden het beeld van hoe FLVCR1-defecten zich bij mensen kunnen manifesteren en versterken het idee dat dit gen essentieel is voor het in stand houden van pijngevoelige zenuwen en lichtgevoelige cellen in het netvlies.
De ziekte modelleren in kleine vissen
Om te onderzoeken hoe FLVCR1 de ontwikkeling van sensorische zenuwen beïnvloedt, gebruikte het team zebravissen, waarvan de doorzichtige embryo’s directe observatie van zenuwcellen mogelijk maken. Ze verminderden het niveau van de visvariant van het gen, flvcr1a, met genetische hulpmiddelen. Vissen met verlaagd flvcr1a hadden minder dorsale wortelganglia, clusters van neuronen die aanraking en pijn langs de rug detecteren. Gedragsmatig bewogen deze vissen minder uit zichzelf en zwommen ze na een lichte aanraking van de staart maar korte afstanden, wat wijst op een afgezwakte sensorische respons. Omdat eerdere muismodellen te vroeg overleden om hun sensorische zenuwen te analyseren, bieden deze zebravissen het eerste levende systeem waarin FLVCR1-gerelateerde zenuwdefecten en gedrag in detail kunnen worden gevolgd.
Drie verstoorde routes komen samen bij de celenergiecentrales
FLVCR1 zit in celmembranen en regelt verschillende belangrijke stoffen. Eerder werk suggereerde rollen in de verwerking van choline (een bouwsteen van membraanlipiden), heem (het ijzervatende pigment dat veel enzymen aandrijft) en de calciumstroom tussen celcompartimenten. De wetenschappers verzamelden huidcellen (fibroblasten) van vier patiënten met verschillende FLVCR1-mutaties en vergeleken die met cellen van gezonde mensen en symptoomvrije dragers. Ze vonden dat patiёntcellen lagere cholinegehalten en meer vloeibare celmembranen hadden—veranderingen die de delicate lipideomgeving kunnen verstoren die mitochondriën nodig hebben. Ze ontdekten ook dat een cruciaal enzym voor de heemproductie in mitochondriën, ALAS1, minder actief was, hoewel de totale heemhoeveelheid vrijwel normaal leek. Tegelijkertijd waren de fysieke contactplaatsen tussen het endoplasmatisch reticulum en mitochondriën—waar calcium normaal naar mitochondriën stroomt—korter en minder frequent, en was de calciumopname door mitochondriën verminderd. Drie problemen—choline-tekort, vertraagde heemproductie en verminderde calciumoverdracht—wezen allemaal op een aantasting van de mitochondriale werking.
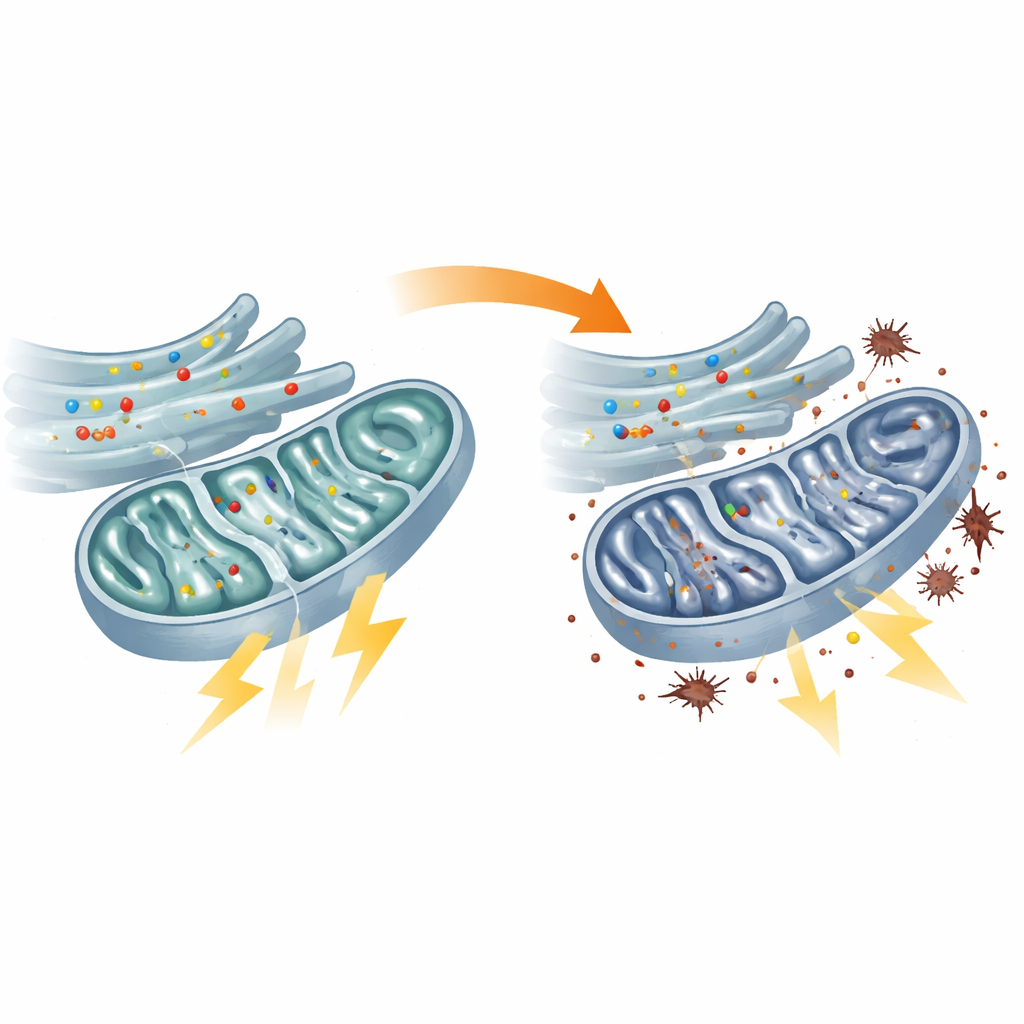
Uitgehongerde mitochondriën en overbelaste back-upsystemen
Directe tests van energiemetabolisme bevestigden dat de mitochondriën in patiёntfibroblasten onderpresteerden. De centrale brandstofverwerkende cyclus, het TCA-circuit, draaide trager, verschillende van zijn sleutelenzymen waren minder actief en de keten van reacties die normaal brandstof in ATP omzet—de energievaluta van de cel—was afgezwakt. Daardoor daalden de ATP-niveaus binnen mitochondriën. De cellen probeerden te compenseren door glycolyse op te voeren, een minder efficiënte suikerverbrandingsweg buiten de mitochondriën. Deze verschuiving in energiestrategie had nadelen: elektronen lekten uit de gestreste mitochondriale machine en veroorzaakten verhoogde lipideperoxidatie, een vorm van oxidatieve schade aan celmembranen. Vergelijkbare defecten werden gezien in zebravissen met verlaagd flvcr1a, waarmee mitochondriale uitval rechtstreeks werd gekoppeld aan het diermodel van sensorische neuropathie.
Aanwijzingen voor toekomstige behandelingen door het verhogen van celenergie
Veelbelovend is dat sommige van deze defecten in het laboratorium konden worden verlicht. Toen het team kunstmatig de calciumopname in mitochondriën verhoogde door overexpressie van een kanaaleiwit genaamd MCU in patiёntcellen, herstelde de energieproductie en nam de tekenen van oxidatieve schade af. Toediening van een heemprecursormolecuul, 5-aminolevulinezuur (ALA), verbeterde ook de TCA-cyclusactiviteit, de werking van de respiratoire keten en ATP-niveaus, hoewel langdurige ALA-blootstelling in eerdere studies schadelijk bleek. Extra choline normaliseerde membraanfluiditeit en hielp lipideschade te verminderen, maar leverde slechts bescheiden kortetermijnwinst in energieopbrengst. Deze rescue-experimenten suggereren dat geen enkele route alleen verantwoordelijk is; in plaats daarvan duwt een netwerk van verstoorde choline-, heem- en calciumhuishouding mitochondriën in chronische onderprestaties.
Waarom deze bevindingen ertoe doen voor patiënten
Door de gevolgen van FLVCR1-mutaties te volgen van moleculen via cellen tot hele organismen, stelt dit werk voor dat energiefalen in mitochondriën een drijvende kracht is achter deze vorm van pijnverliesneuropathie en de bijbehorende gezichtsproblemen. Sensorische zenuwen en fotoreceptoren verbruiken uitzonderlijk veel energie omdat ze lange axonen onderhouden of voortdurend lichtgevoelige structuren vernieuwen, waardoor ze bijzonder kwetsbaar zijn wanneer mitochondriale output wegvalt. Het zebravismodel en de patiёntafgeleide cellen uit deze studie bieden nu praktische testplatforms voor therapieën die het mitochondriale metabolisme versterken. Hoewel behandelingen zoals choline-suppletie, gecontroleerde heemverhoging of geneesmiddelen die mitochondriale calciumopname verbeteren zorgvuldige evaluatie in diermodellen en klinische proeven vereisen, is de centrale boodschap duidelijk: het herstellen van de energievoorziening van kwetsbare neuronen kan op een dag helpen mensen te beschermen die zonder het belangrijkste waarschuwingssignaal van de natuur—pijn—zijn geboren.
Bronvermelding: Bertino, F., Zanin Venturini, D.I., Grasso, E. et al. Mitochondrial energetic failure underlies FLVCR1-related sensory neuropathy. Commun Biol 9, 429 (2026). https://doi.org/10.1038/s42003-026-09691-y
Trefwoorden: sensorische neuropathie, mitochondriale disfunctie, FLVCR1, pijnongevoeligheid, zenuwenergiemetabolisme