Clear Sky Science · nl
Structurele basis voor herkenning van vleermuisreceptoren door SARS-CoV-2 en vleermuis SARS2-achtige coronavirussen
Waarom dit vleermuis–virusverhaal nog steeds van belang is
De COVID-19-pandemie begon meer dan zes jaar geleden, maar wetenschappers proberen nog altijd in kaart te brengen hoe het virus dat deze ziekte veroorzaakt, SARS-CoV-2, zo goed werd in het infecteren van mensen. Een centraal raadsel is hoe dit virus, en zijn nauwe verwanten die in vleermuizen worden gevonden, zich hechten aan een eiwit dat ACE2 heet op het celoppervlak — een eerste en cruciale stap voor infectie. Inzicht in deze microscopische sleutel–slotinteracties kan verduidelijken waar het virus vandaan kwam, hoe het zich aanpaste, en wat er kan gebeuren als aanverwante virussen in de toekomst in mensen overspringen. 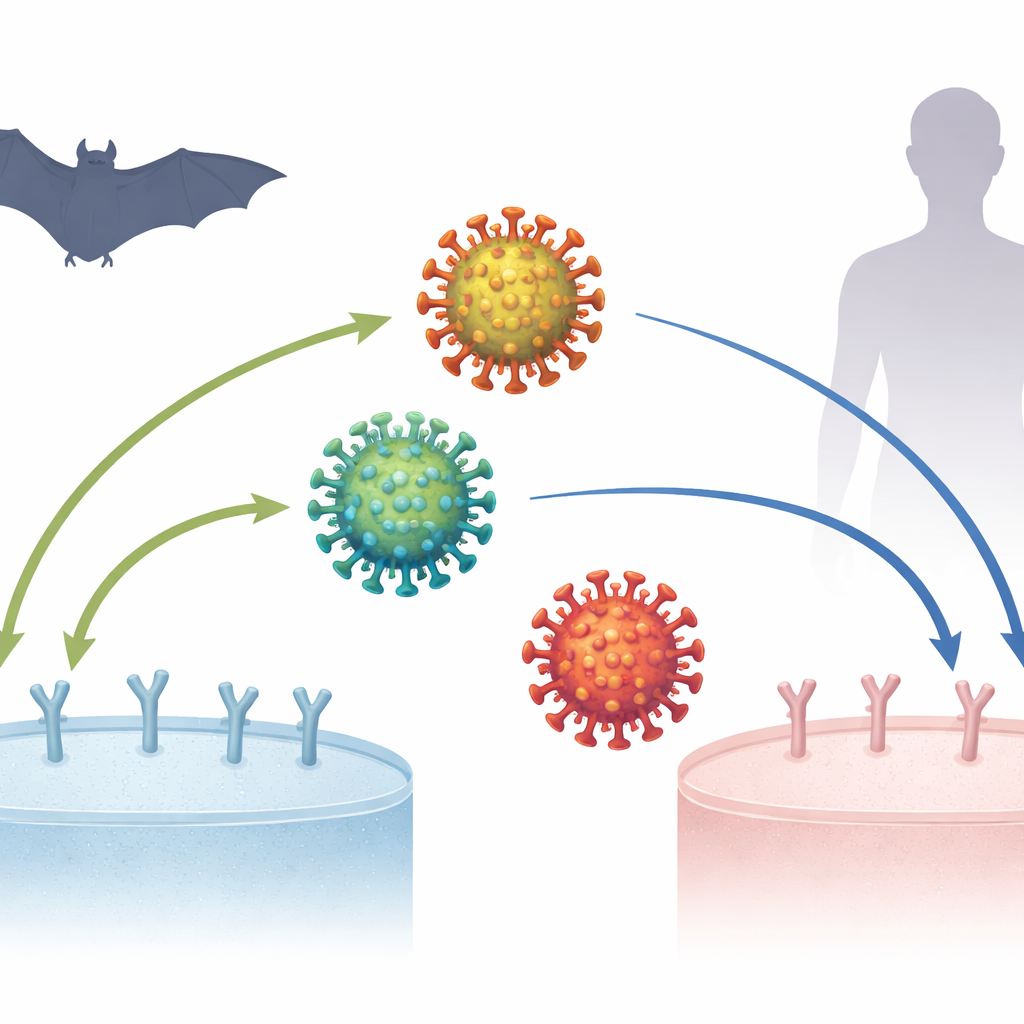
Kijken naar de virale handdruk
De studie richt zich op het spike-eiwit, de kroonvormige structuur op het virusoppervlak die ACE2 grijpt. Een klein gebied van de spike, het receptor-bindende domein (RBD), werkt als een vingertop die de ACE2-"deurknop" vastpakt. Eerder werk liet zien dat wanneer coronavirussen tussen soorten springen — bijvoorbeeld van vleermuizen naar civetkatten naar mensen — het RBD vaak mutaties oppikt die de grip op de ACE2 van de nieuwe gastheer verbeteren. Maar SARS-CoV-2 vormde een mysterie: de oorspronkelijke variant bond al bijzonder goed aan menselijke ACE2, zelfs voordat er veel tijd was voor aanpassing, en sommige vleermuisvirussen die verwant zijn aan SARS-CoV-2 leken menselijk ACE2 beter te binden dan vleermuis-ACE2. Dat bracht sommigen ertoe zich af te vragen of SARS-CoV-2 een uitzondering was op de gebruikelijke evolutionaire regels.
Het testen van vleermuis- en menselijke receptoren
Om dit mysterie te onderzoeken, bekeken de onderzoekers twee vleermuiscoronavirussen die nauw verwant zijn aan SARS-CoV-2, bekend als BANAL-52 en BANAL-236. Ze vergeleken hoe sterk de RBD's van deze virussen en die van SARS-CoV-2 zich hechtten aan ACE2 van mensen en van meerdere vleermuissoorten. Met celgebaseerde bindingsassays, hoogprecisie-biosensormetingen en infectietests met onschadelijke "pseudovirussen" vonden ze een duidelijk patroon. Het RBD van BANAL-52 bond het sterkst aan ACE2 van één vleermuissoort, Rhinolophus sinicus, en iets minder sterk aan menselijke ACE2. Het RBD van SARS-CoV-2 toonde daarentegen een bescheiden voorkeur voor menselijke ACE2 boven vleermuis-ACE2. Over het geheel genomen greep het RBD van BANAL-52 zowel vleermuis- als menselijke receptoren strakker dan dat van SARS-CoV-2, maar het was het fijnst afgestemd op die specifieke vleermuis-ACE2. 
Hoe een enkele atomaire aanpassing het evenwicht verandert
Het team ging vervolgens over op röntgenkristallografie, die structuren op atomaire schaal onthult, om precies te zien hoe de virale "vinger" en de ACE2-"deurknop" elkaar raken. Ze concentreerden zich op twee sleutelposities: één op het virale RBD (genoemd residue 498) en één op ACE2 (residue 41). In BANAL-52 gebruiken zowel de virale plek als de vleermuis-ACE2-plek hetzelfde bouwblok, histidine, wat een zeer nauwkeurige, gelaagde interactie mogelijk maakt — stapeling als twee munten en ook de vorming van een waterstofbrug. In menselijke ACE2 draagt diezelfde positie een verwant maar iets anders bouwblok, tyrosine, dat nog steeds goed stapelt met BANAL-52's histidine maar de extra waterstofbrug mist. SARS-CoV-2 gebruikt daarentegen glutamine op deze virale positie, dat niet op dezelfde manier kan stapelen, wat resulteert in zwakkere binding aan zowel vleermuis- als menselijke ACE2. Door doelbewust deze aminozuren in vleermuis-ACE2 om te wisselen, bevestigden de onderzoekers dat het versterken of verzwakken van dit ene contactpunt kon omkeren welke virus- of gastheerbinding werd bevoordeeld.
Waarom menselijke ACE2 zo’n gastvrije deur is
Voorbij dit ene contactpunt vroegen de auteurs zich af waarom menselijke ACE2 in het algemeen zo’n efficiënte poort is voor coronavirussen. Door vleermuis- en menselijke ACE2 naast elkaar te vergelijken, identificeerden ze meerdere mens-specifieke kenmerken die de virale handdruk verbeteren. Twee posities op menselijke ACE2, met de aminozuren histidine (op positie 34) en methionine (op positie 82), creëren sterkere waterstofbruggen en vette "vlekken" die helpen het virale RBD steviger te laten passen. Een ander menselijk residu, threonine op positie 27, maakt de binding eigenlijk iets zwakker dan in de vleermuisversie, maar in totaal wegen de gunstige contacten zwaarder. Deze details sluiten aan bij eerder werk waaruit blijkt dat menselijke ACE2 meerdere "hotspots" heeft die het van nature een aantrekkelijke receptor maken voor een breed scala aan coronavirussen.
Het oorsprongsverhaal herkaderen
Als je alle gegevens bij elkaar zet, betoogt de studie dat SARS-CoV-2 en zijn vleermuisverwanten nog steeds het gebruikelijke evolutionaire script volgen. De spike van BANAL-52 lijkt het best aangepast aan ACE2 van bepaalde vleermuizen, en is tegelijkertijd compatibel met menselijke ACE2. De spike van SARS-CoV-2 daarentegen is beter afgestemd op menselijke ACE2 dan op vleermuis-ACE2, geholpen door speciale contactpunten op de menselijke receptor. Kleine wijzigingen op slechts een paar posities — met name bij het virale residu 498 en aangrenzende plaatsen — kunnen het evenwicht verschuiven in welke gastheer wordt bevoordeeld. Voor niet-specialisten is de conclusie dat er geen noodzaak is om exotische verklaringen aan te halen: standaard, goed begrepen structurele principes van eiwit–eiwitinteractie zijn voldoende om te verklaren hoe deze virussen vleermuis- en menselijke cellen herkennen, en ze ondersteunen een nauwe evolutionaire band tussen SARS-CoV-2 en verwante vleermuiscoronavirussen.
Bronvermelding: Hsueh, FC., Shi, K., Aihara, H. et al. Structural basis for bat receptor recognition by SARS-CoV-2 and bat SARS2-like coronaviruses. Commun Biol 9, 398 (2026). https://doi.org/10.1038/s42003-026-09682-z
Trefwoorden: evolutie van SARS-CoV-2, vleermuiscoronavirussen, ACE2-receptor, virale gastheerbreedte, binding van spike-eiwit