Clear Sky Science · nl
Door het Afrikaanse varkenspestvirus gecodeerd eiwit MGF 505–3R schaadt de aangeboren immuniteit via ubiquitine-gemedieerde afbraak van MyD88
Waarom dit van belang is voor diergezondheid en daarbuiten
Afrikaanse varkenspest heeft varkensbedrijven wereldwijd verwoest, bedreigt de voedselvoorziening en veroorzaakt enorme economische schade. Het virus is deels zo dodelijk omdat het de vroege waarschuwingssystemen van het lichaam omzeilt. Deze studie onthult hoe één viraal eiwit, genoemd MGF 505–3R, stilletjes een belangrijke alarmschakelaar in cellen saboteert en toont dat een klein fragment van dit eiwit ook kan worden omgevormd tot een krachtig anti-inflammatoir middel bij muizen.
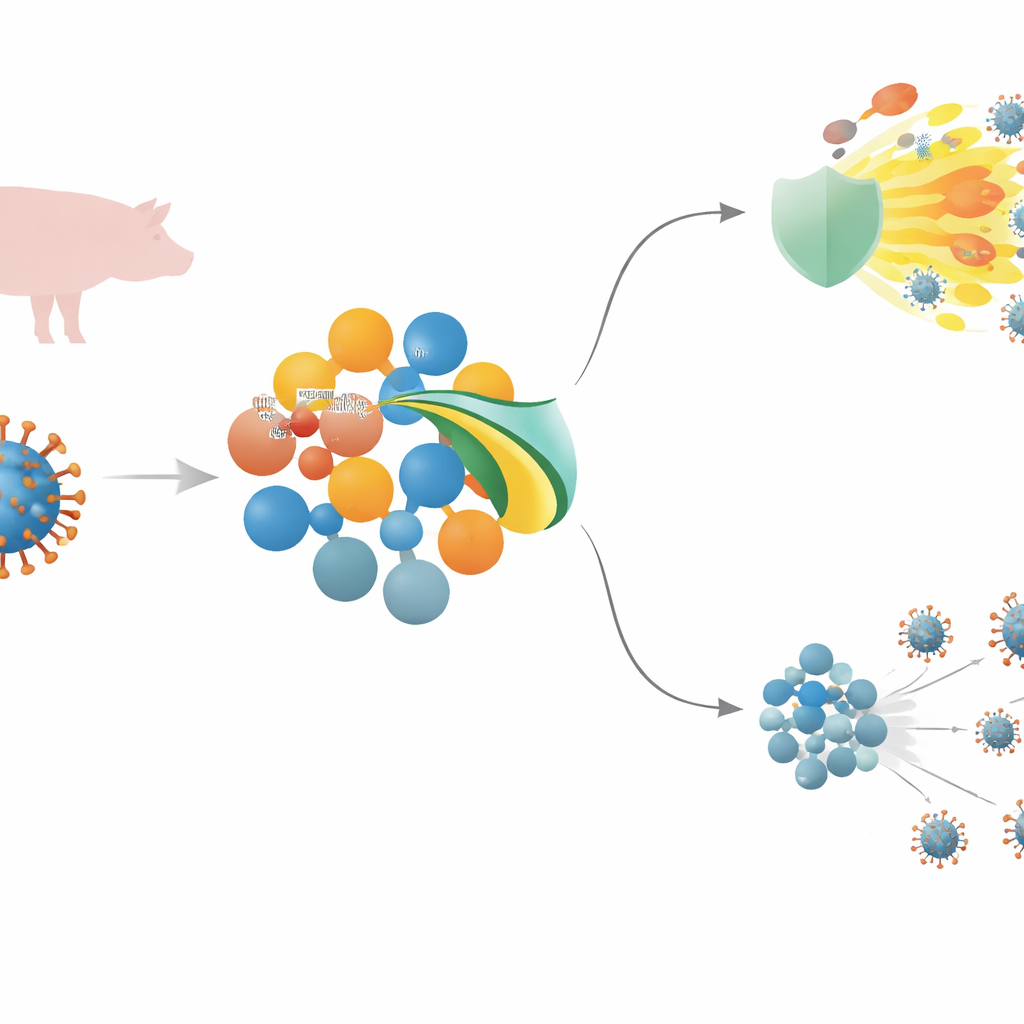
Een dodelijk varkensvirus en de eerste verdedigingslinie van het lichaam
Het Afrikaanse varkenspestvirus (ASFV) is een groot DNA-virus dat vrijwel elk geïnfecteerd varken kan doden. Om zich te vestigen moet het de aangeboren immuniteit te slim af zijn—de snelle, frontlinieverdediging die indringers detecteert en ontsteking en antivirale moleculen op gang brengt. Centraal in deze respons staat een signaalketen die sensoren op het celoppervlak, een relaisproteïne genaamd MyD88 en een meesterknop bekend als NF–κB omvatten, die samen de productie van ontstekingsboodschappers en antivirale interferonen aansturen. ASFV draagt vele genen waarvan wordt aangenomen dat ze in deze signalen ingrijpen, maar voor meerdere daarvan, waaronder MGF 505–3R, waren de precieze mechanismen niet goed begrepen.
Hoe het virus de bedrading van het immuunalarm doorknipt
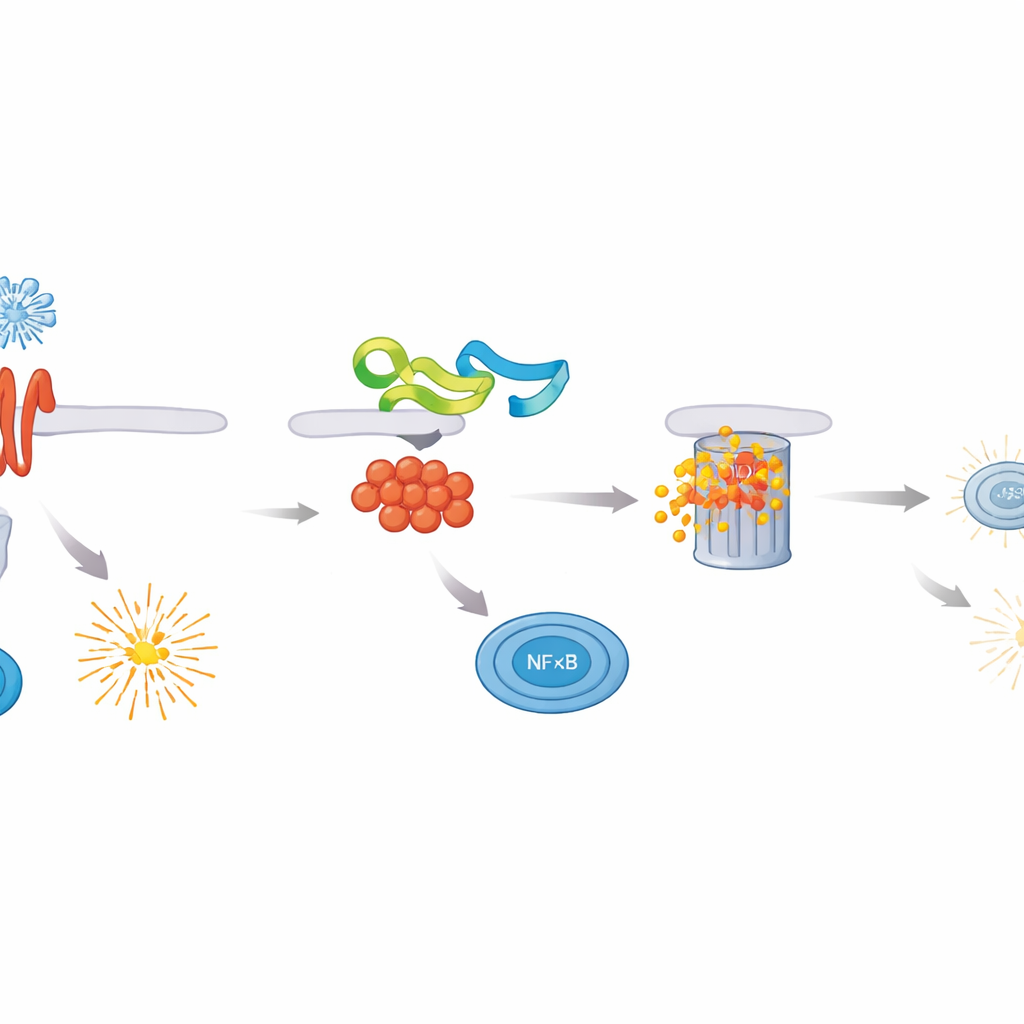
De onderzoekers screenden ASFV-eiwitten op hun vermogen om NF–κB-activiteit te verminderen en vonden dat MGF 505–3R een bijzonder sterke remmer was. Wanneer dit virale eiwit aanwezig was, produceerden cellen die aan verschillende immuunprikkels werden blootgesteld aanzienlijk minder ontstekingscytokinen en veel lagere niveaus van type I- en type III-interferonen. Nadere bestudering liet zien dat MGF 505–3R direct op MyD88 werkt, de centrale adapter die veel immuunsensoren met NF–κB verbindt. MGF 505–3R bindt MyD88 en markeert het voor verwijdering via het eiwitafbrekende apparaat van de cel, met behulp van een vorm van etikettering die K48-gekoppelde ubiquitinatie wordt genoemd. Terwijl MyD88 wordt afgebroken, slaagt NF–κB er niet in de kern binnen te gaan en beschermende genen aan te zetten, waardoor cellen ontvankelijker worden voor virale groei.
Inzoomen op een klein maar krachtig eiwitfragment
Om het cruciale deel van MGF 505–3R te identificeren maakten de onderzoekers verkorte versies van het eiwit en testten hun effecten. Ze ontdekten dat aminozuren 89–277 zowel noodzakelijk als voldoende waren om aan MyD88 te binden, de ubiquitinatie ervan te bevorderen en NF–κB-activatie te blokkeren. Geleid door computervoorspellingen van de eiwitstructuur sneden ze twee korte peptiden uit dit gebied. Eén daarvan, pep3R–1, bleek opvallend: het verminderde scherp NF–κB-activiteit, blokkeerde fosforylering en de kerntranslocatie van de NF–κB-subunit p65, en verlaagde de expressie van ontstekingscytokinen en interferonen in immuuncellen die met meerdere gevaarssignalen werden gestimuleerd. In kweekcellen dempten zowel het volledige MGF 505–3R als pep3R–1 niet alleen antivirale signalering maar maakten ze het ook mogelijk dat een testvirus efficiënter repliceerde, wat benadrukt hoe krachtig deze route is voor het beheersen van infecties.
Een viraal trucje omzetten in een potentiële medicijn
Het team vroeg zich vervolgens af of het peptide gebruikt kon worden om schadelijke ontsteking te kalmeren in plaats van virussen te helpen. In een muismodel van colitis dat werd opgewekt door een chemische stof genaamd DSS, verliezen dieren normaal gewicht, ontwikkelen ze bloederige diarree en vertonen ze ernstige schade en binnendringing van immuuncellen in de dikke darm. Muizen die met pep3R–1 werden behandeld deden het veel beter: de ziekte-scores waren lager, de darmen waren langer en gezonder, en microscopisch onderzoek toonde een bewaarde weefselstructuur met veel minder ontstekingscellen. De niveaus van belangrijke ontstekingsmoleculen zoals TNF–α, IL–1β, IL–6 en een enzym dat geassocieerd is met de instroom van witte bloedcellen waren zowel in darmweefsel als in bloed verminderd. In een afzonderlijk experiment verminderde pep3R–1 ook de ontstekingsreactie op een systemisch bacterieel toxine, wat aangeeft dat het zowel lokale als lichaam-brede ontstekingsstormen kan dempen.
Wat dit betekent voor varkens, mensen en toekomstige behandelingen
Dit werk toont aan dat het ASFV-eiwit MGF 505–3R het virus helpt gedijen door een centraal immuunrelais, MyD88, te ontmantelen, waardoor zowel ontstekings- als interferonverdedigingen worden uitgeschakeld. Tegelijkertijd kan een klein fragment van dit virale eiwit, pep3R–1, worden hergebruikt om overtollige ontsteking in muizen veilig te verminderen, ook in een model van darmziekte. Hoewel er nog veel moet gebeuren—zoals het verbeteren van stabiliteit, afleveringsmethoden en testen in meer ziektetoestanden—onthult de studie zowel een kritisch zwak punt waarop antivirale strategieën zich zouden kunnen richten als een veelbelovend plan voor het ontwerpen van nieuwe peptide-gebaseerde anti-inflammatoire geneesmiddelen geïnspireerd door virale immuunontwijking.
Bronvermelding: Liu, H., Sun, L., Wang, F. et al. African swine fever virus–encoded protein MGF 505–3R impairs innate immunity via ubiquitin–mediated degradation of MyD88. Commun Biol 9, 407 (2026). https://doi.org/10.1038/s42003-026-09681-0
Trefwoorden: Afrikaanse varkenspest, aangeboren immuniteit, NF-kappaB, MyD88, anti-inflammatoir peptide