Clear Sky Science · nl
Abnormale ijzerhomeostase veroorzaakt beschadiging van cochleaire haarcellen en gehoorverlies bij muizen zonder Gprasp2
Waarom dit belangrijk is voor alledaags horen
Gehoorverlies wordt vaak gezien als een simpel "slijtageproces", maar bij veel mensen wordt het veroorzaakt door verborgen defecten in hun genen. Deze studie onthult hoe een weinig bestudeerd gen, GPRASP2, helpt de kwetsbare geluidsgevoelige cellen van het binnenoor te beschermen tegen door ijzer veroorzaakte schade. Door precies te laten zien wat er misgaat wanneer dit gen ontbreekt, opent het werk de deur naar nauwkeurigere diagnoses en toekomstige therapieën voor erfelijke gehoorproblemen en mogelijk aanverwante stemmingsstoornissen.
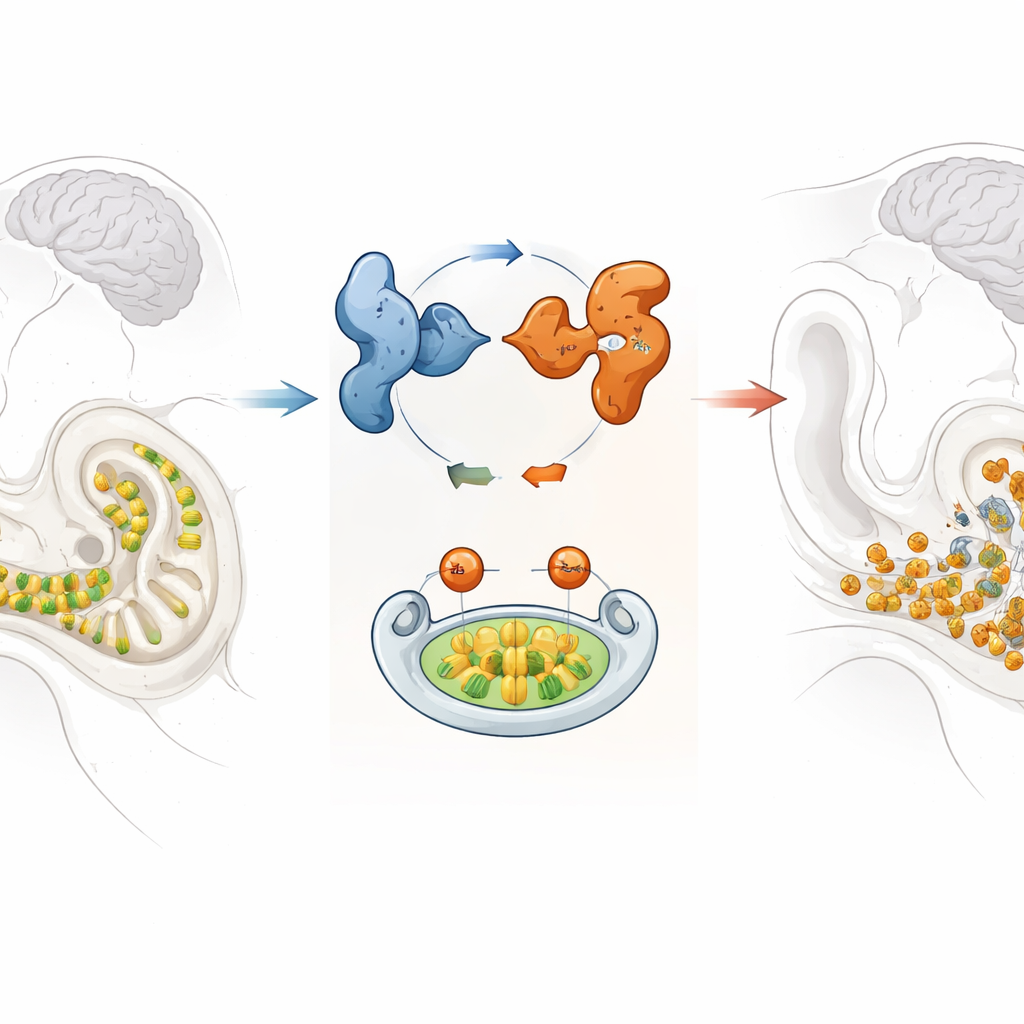
Een fragiele geluidssensor in het binnenoor
In de gekronkelde cochlea van het binnenoor liggen rijen haarcellen die kleine vibraties omzetten in elektrische signalen die de hersenen kunnen begrijpen. Zodra deze haarcellen verloren zijn, groeien ze niet terug, dus het is cruciaal ze gezond te houden voor levenslang gehoor. De onderzoekers richtten zich op GPRASP2, een gen dat eerder werd gevonden met mutaties in een familie met X-gebonden syndromisch gehoorverlies — een aandoening die vooral mannen treft en gepaard kan gaan met extra symptomen. Hoewel bekend was dat GPRASP2 actief is in de hersenen en het binnenoor, bleef de precieze rol in het gehoor onduidelijk.
Wat er gebeurt wanneer het gen ontbreekt
Om de menselijke situatie na te bootsen gebruikten de onderzoekers CRISPR-genbewerking om muizen te maken die geen werkende kopie van het Gprasp2-gen hebben. Deze dieren toonden duidelijk gehoorverlies over een breed spectrum van geluidsfrequenties bij gevoelige elektrische metingen van de gehoorzenuw. Hun reacties op plotselinge luide geluiden waren afgezwakt, terwijl balans en motoriek grotendeels normaal bleven — wat wijst op een specifiek probleem in het gehoor in plaats van een algemene bewegingsstoornis. Interessant genoeg vertoonden de muizen ook depressie-achtige gedragingen in verschillende standaardtests, wat suggereert dat dit gen gehoor en gemoedstoestand verbindt via zijn werking in zowel oor als hersenen.
Schade binnenin de cochlea
Bij onderzoek van de binnenoren van Gprasp2-deficiënte muizen vonden de onderzoekers dat veel buitenste haarcellen ontbraken of verplaatst waren, en dat de overgebleven cellen vaak vervormde bundels van kleine uitsteeksels hadden die normaal als stemvorken functioneren. Ze zagen ook veranderingen in de stria vascularis, een zeer actief weefsel dat de speciale vloeistof- en elektrische omgeving voor het horen in stand houdt. Op microscopisch niveau waren markers van celdood en oxidatieve stress verhoogd in de buitenste haarcellen en nabijgelegen zenuwcellen, wat aangeeft dat deze structuren zwaar werden aangevallen door reactieve moleculen en meer kans hadden te sterven.
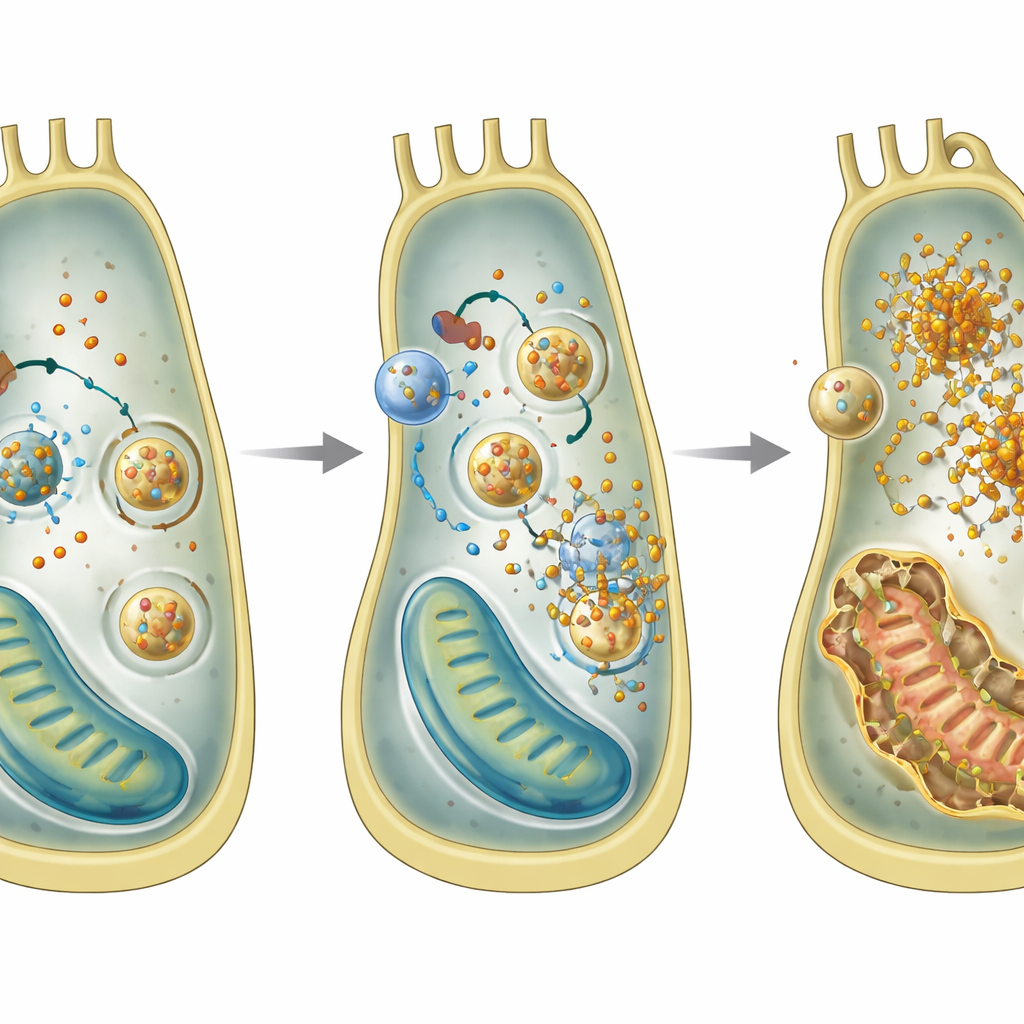
IJzerstapeling en uit de hand lopend recyclen
Dieper gravend gebruikten de onderzoekers een celijn van het binnenoor om te onderzoeken wat er misgaat in individuele cellen zonder GPRASP2. Ze ontdekten een patroon dat kenmerkend is voor een vorm van celdood genaamd ferroptose, die wordt aangedreven door ijzer en lipidenperoxidatie. Cellen zonder Gprasp2 stapelden meer ferros ijzer op, produceerden meer reactieve zuurstofsoorten, hadden lagere niveaus van het antioxidant glutathion en vertoonden beschadigde mitochondriën. Gen- en proteïneanalyses wezen op een toename van ferritinophagie, een proces waarbij ijzeropslagdeeltjes naar recyclingcompartimenten worden vervoerd en afgebroken, waardoor extra ijzer vrij komt in de cel. Het blokkeren van deze recylingstap verminderde de ijzerophoping, wat het idee ondersteunt dat overmatige ferritinophagie centraal staat in de schade.
Een sleutelpartner-eiwit dat ijzer in toom houdt
De onderzoekers vroegen zich vervolgens af hoe GPRASP2 dit ijzerbeheersysteem reguleert. Door de eiwitten in kaart te brengen die met GPRASP2 interageren, identificeerden ze NCAM1, een celadhesiemolecuul dat vooral bekend is om zijn rol in leren, geheugen en stemming. Ze toonden aan dat GPRASP2 fysiek bindt aan NCAM1, en dat verlies van GPRASP2 leidt tot lagere NCAM1-niveaus in haarcellen en in gecultiveerde auditieve cellen. Lagere NCAM1 hing samen met verhoogde ferritinophagie en ijzerstapeling. Het herstellen van NCAM1 in Gprasp2-deficiënte cellen verlaagde het ijzergehalte en dempte belangrijke regulatoren van ferritinophagie, ook al bleef algemene autofagie actief. Dit suggereert dat GPRASP2 een specifiek ijzerrecyclingpad via NCAM1 fijnregelt, in plaats van het gehele recyclingsysteem aan of uit te schakelen.
Wat dit betekent voor gehoor en daarbuiten
In eenvoudige termen laat dit werk zien dat GPRASP2 fungeert als een veiligheidsmanager voor ijzer in cochleaire haarcellen. Wanneer GPRASP2 aanwezig is, werkt het samen met NCAM1 om te voorkomen dat te veel opgeslagen ijzer terug in de cel wordt vrijgegeven, waardoor oxidatieve schade wordt beperkt. Wanneer het gen verstoord is, raakt de ijzerhuishouding uit balans, roesten de cellen van binnenuit en sterven cruciale haarcellen, wat leidt tot gehoorverlies. Omdat GPRASP2 en NCAM1 ook in de hersenen functioneren, kan hetzelfde pad helpen de gemoedstoestandveranderingen te verklaren die bij sommige patiënten worden gezien. Het begrijpen van deze ijzergebaseerde faalmode biedt een duidelijk doel voor toekomstige medicijnen of genhersteltherapieën gericht op het behoud van gehoor bij mensen met GPRASP2-gerelateerde of soortgelijke genetische aandoeningen.
Bronvermelding: Lu, Y., Sheng, F., Yao, J. et al. Abnormal iron homeostasis mediates cochlear hair cell impairment and hearing loss in Gprasp2-deficient mice. Commun Biol 9, 425 (2026). https://doi.org/10.1038/s42003-026-09679-8
Trefwoorden: erfelijk gehoorverlies, cochleaire haarcellen, ijzerhomeostase, ferroptose, GPRASP2