Clear Sky Science · nl
Een praktische gids voor gerichte single-cell RNA-sequencing technologieën
Waarom het belangrijk is naar individuele cellen te kijken
Elke cel in je lichaam draagt hetzelfde DNA, maar verschillende cellen gedragen zich sterk verschillend. Dat doen ze door specifieke genen aan of uit te zetten en door RNA-moleculen op subtiele manieren te bewerken. Moderne single-cell RNA-sequencing kan aflezen welke RNA’s in duizenden cellen tegelijk aanwezig zijn, maar mist momenteel het grootste deel van de boodschap. Deze review legt uit waar de huidige technieken informatie verliezen en hoe nieuwe “gerichte” methoden worden ontwikkeld om in te zoomen op de belangrijkste delen van RNA-moleculen voor onderzoek, diagnose en behandelontwerp.
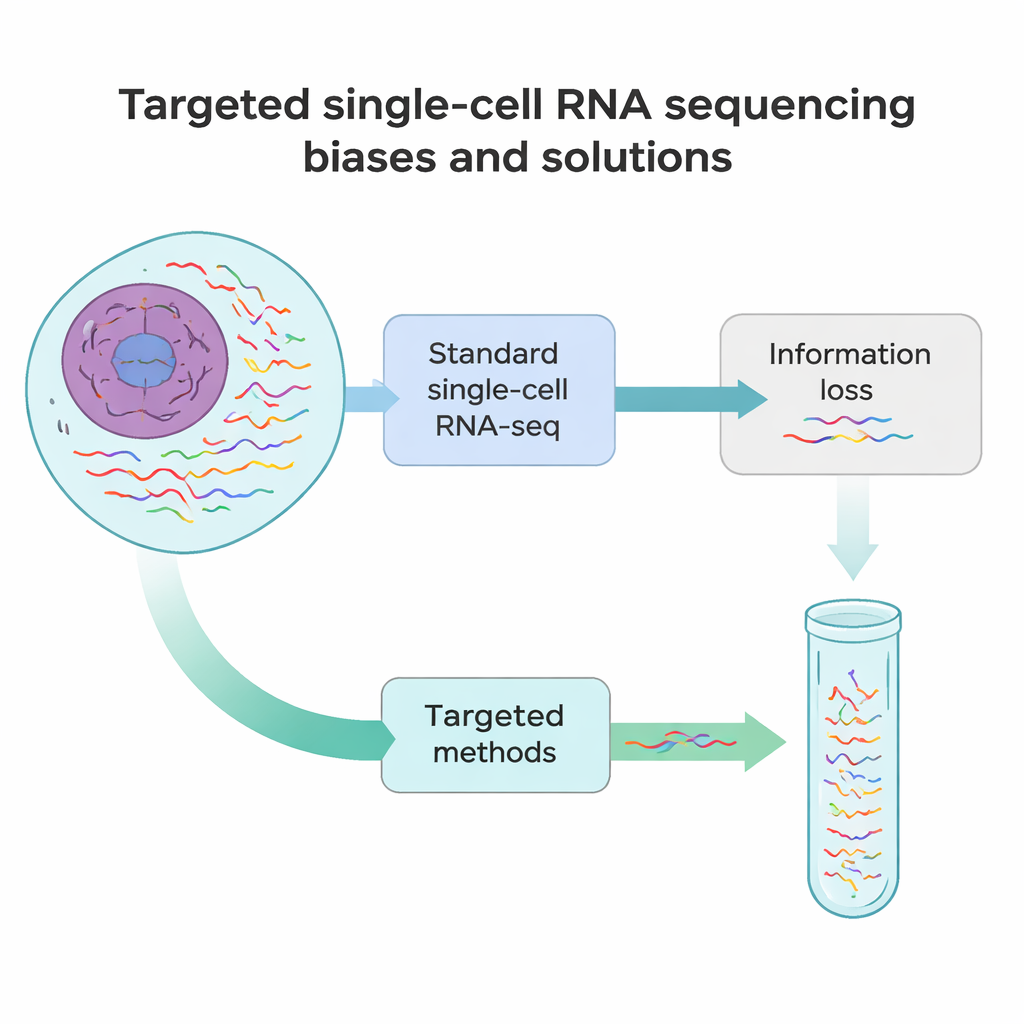
Waar de huidige methoden tekortschieten
Standaard single-cell RNA-sequencing werkt een beetje als het nemen van een snelle snapshot van elk bericht in een cel in plaats van een volledige film. In de meeste experimenten wordt slechts ongeveer 10–40% van alle RNA’s in een cel gedetecteerd, en wordt alleen het begin of het einde gelezen. Dat betekent dat veel zeldzame maar belangrijke RNA’s — zoals markers die de identiteit van een cel bepalen, of genversies die ziekteveroorzakende mutaties dragen — gemakkelijk gemist worden. Bovendien introduceren meerdere technische stappen, van weefsels tot losse cellen maken tot het kopiëren van RNA naar DNA en het amplificeren daarvan, systematische vertekeningen. Sommige RNA’s worden vroeg afgebroken, sommige oververtegenwoordigd en andere verdwijnen helemaal uit de data.
Waarom interne RNA-details ertoe doen
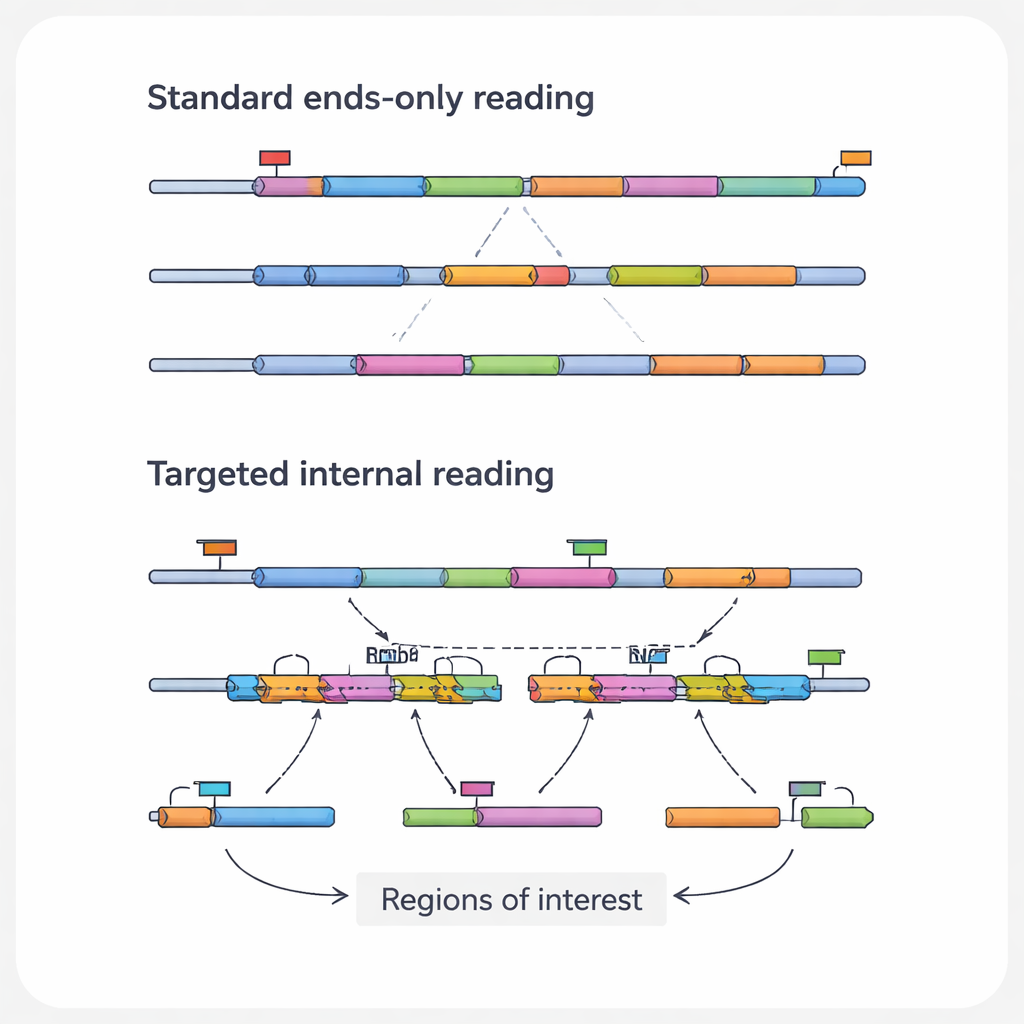
De medisch meest relevante informatie in een RNA-molecuul ligt vaak in de interne regio’s, niet aan de uiteinden die standaardmethoden zien. Deze binnenste secties kunnen puntmutaties bevatten die kanker aandrijven, fusiepunten waar twee genen abnormaal aan elkaar zijn gekoppeld, of splice-juncties die verschillende eiwvervarianten uit hetzelfde gen creëren. Ze kunnen ook de sporen vastleggen van genbewerkinstrumenten zoals CRISPR. De auteurs noemen deze specifieke kenmerken “regio’s van interesse” en de RNA’s die ze dragen “transcripten van interesse.” Omdat gangbare hoogdoorvoersplatforms vooral de uiteinden van RNA’s lezen, overzien ze routinematig deze cruciale details, vooral in lange of weinig voorkomende transcripten.
Nieuwe manieren om de schijnwerper te richten
Om deze blinde vlekken te overwinnen hebben onderzoekers een familie van gerichte single-cell RNA-sequencingbenaderingen ontwikkeld. In plaats van te proberen elk RNA gelijkmatig te lezen, verrijken deze methoden doelbewust geselecteerde transcripten of regio’s. Sommige strategieën herontwerpen de capture-deeltjes zodat ze zich hechten aan interne RNA-sequenties in plaats van alleen aan de staart, waardoor gekozen boodschappen al in de eerste stap in de bibliotheek terechtkomen. Andere voegen aangepaste prim ers toe die intern starten met kopiëren, of extra PCR-stappen die specifiek een kortlijst van genen uit een bestaande bibliotheek amplificeren. Weer een andere groep gebruikt DNA-probes die hybridiseren met doel-RNA’s of hun kopieën en die vervolgens ‘uitvissen’, vaak met eenvoudige chemische labels. Elke categorie maakt afwegingen tussen gevoeligheid, aantal cellen, aantal doelen en kosten, maar heeft hetzelfde doel: meer betekenisvolle details terugwinnen uit hetzelfde of minder sequentievolume.
Toepassingen van virussen tot tumoren
Deze gerichte methoden hervormen al verschillende gebieden van de biologie en geneeskunde. Bij infecties kunnen ze eindelijk virale of bacteriële RNA’s vastleggen die de poly(A)-staarten missen waar standaardprotocollen op rekenen, waardoor zichtbaar wordt in welke gastheercellen ze voorkomen en hoe ze de gastheer-genexpressie wijzigen. Bij kanker kan gerichte single-cell sequencing aanwijzen welke celtypen specifieke mutaties of fusiegenen dragen en die koppelen aan gewijzigde genprogramma’s, wat helpt verklaren waarom sommige cellen resistent worden tegen therapie. Andere methoden richten zich op alternatieve splicing en onthullen welke celtypen welke isoformen gebruiken, of op zeldzame celpopulaties en subtiele markers die anders onder de detectiedrempel zouden blijven. In gepoolde CRISPR-screens laat verbeterde vangst van guide-RNA’s wetenschappers elke genetische perturbatie koppelen aan de exacte cellulaire respons.
De juiste tool kiezen en wat er daarna komt
Omdat er nu een drukgevulde gereedschapskist met gerichte benaderingen bestaat, stellen de auteurs een beslisboom voor om onderzoekers te helpen een methode te kiezen. Belangrijke vragen zijn of volledige transcriptomeprofilering nodig is, hoeveel genen of regio’s moeten worden gericht, hoe ver die regio’s van de RNA-uiteinden liggen en hoeveel cellen verwerkt kunnen worden. Vooruitkijkend beargumenteren ze dat de grootste winst zal komen van het verbeteren van de allereerste capture-stappen, het opschalen van slimme probe-gebaseerde strategieën en het combineren van targeting met opkomende long-read en directe RNA-sequencingplatforms. Tot het praktisch wordt elk RNA in elke cel van begin tot eind te lezen, zal gerichte single-cell RNA-sequencing essentieel blijven om de delen van het cellulaire bericht te zien die het meest relevant zijn voor biologie en ziekte.
Bronvermelding: Moro, G., Brunner, E. & Basler, K. A practical guide to targeted single-cell RNA sequencing technologies. Commun Biol 9, 250 (2026). https://doi.org/10.1038/s42003-026-09675-y
Trefwoorden: single-cell RNA sequencing, gerichte sequencing, transcriptomica, kankermutaties, spatiale transcriptomica