Clear Sky Science · nl
ZIKV-omhullingsproteïne blokkeert krachtig vroege richtinggevende differentiatie in de neurale lijn
Waarom dit belangrijk is voor zich ontwikkelende hersenen
Het zikavirus kwam aanvankelijk in het nieuws omdat het ervoor zorgde dat baby’s met uitzonderlijk kleine hoofden en ernstige hersenschade werden geboren. Maar hoe kan een infectie in de moeder zo krachtig de allereerste stappen van hersenopbouw in het embryo ontregelen? Deze studie zoomt in op één viraal onderdeel – het omhullingsproteïne dat de Zikavirusdeeltjes omgeeft – en onderzoekt of dat eiwit op zichzelf de ontwikkeling van zenuwcellen kan misleiden. Door vroege hersenontwikkeling in het lab na te bootsen met muizenstamcellen, laten de onderzoekers zien hoe dit virale eiwit op stille maar krachtige wijze de normale aanleg van neurale netwerken blokkeert.
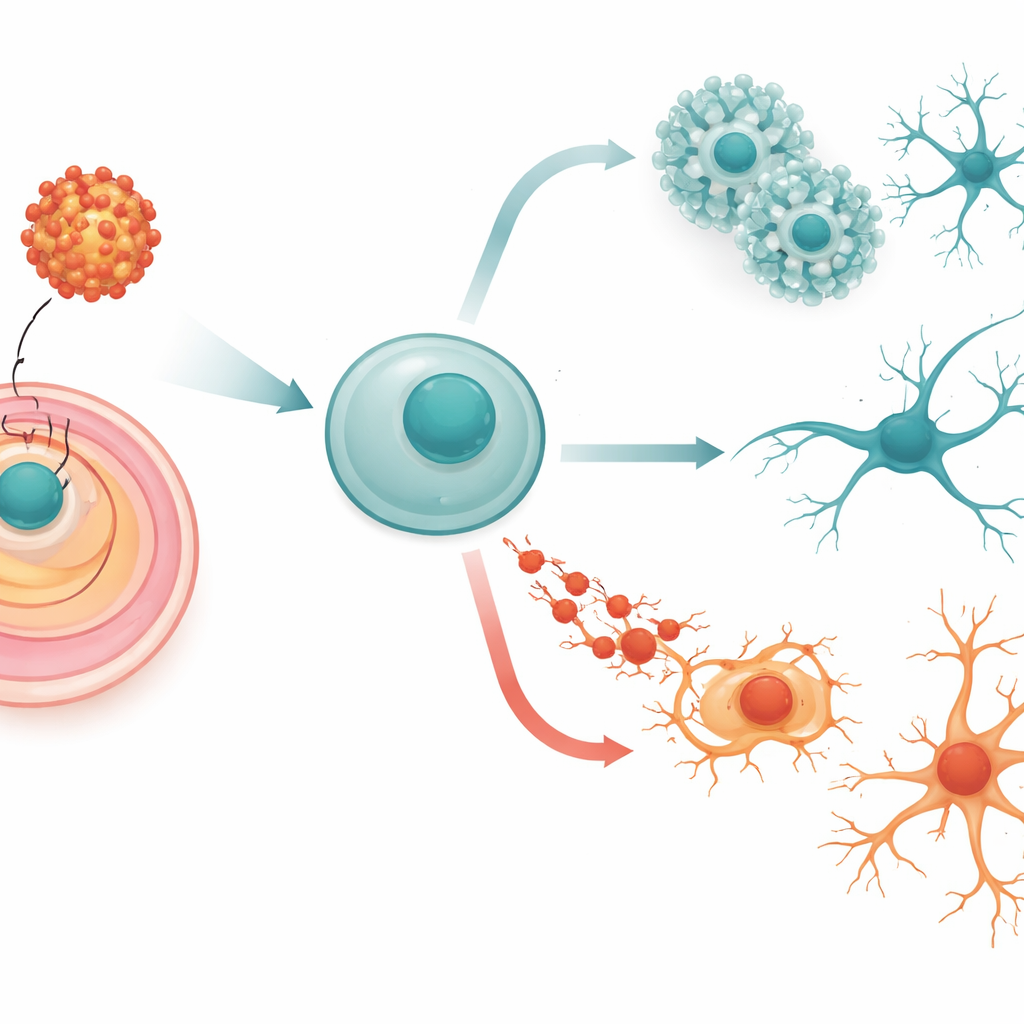
Van flexibele begincellen naar toekomstige zenuwcellen
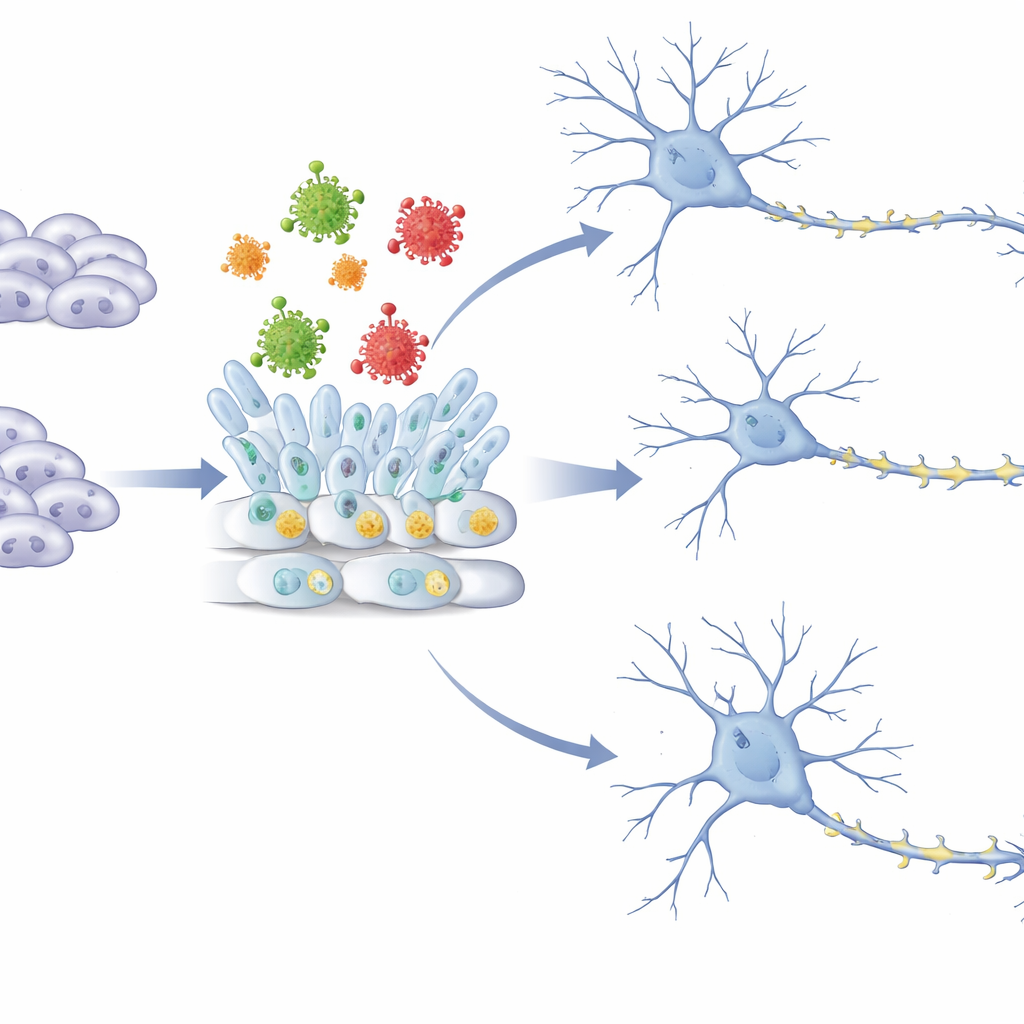
Onze hersenen beginnen als eenvoudige, zeer flexibele cellen die embryonale stamcellen worden genoemd. Deze cellen kunnen in elk weefsel van het lichaam veranderen, maar onder de juiste omstandigheden volgen ze een zorgvuldig uitgestippeld traject richting zenuwcelidentiteit. Eerst verbinden ze zich aan de “neurale” route, vervolgens vormen ze rozetachtige structuren die doen denken aan het vroege zenuwstelsel, en uiteindelijk rijpen ze uit tot neuronen die via lange, vertakte uitlopers verbindingen maken. Het team gebruikte muis-embryonale stamcellen als model voor deze vroege fasen en schakelde ze zo in dat ze het Zika-omhullingsproteïne produceerden, met of zonder een kleine wijziging op een belangrijke suikerbindingsplaats die bekendstaat als beïnvloedend voor de virale eigenschappen.
Viraal omhulselproteïne bevriest de eerste stappen van hersenopbouw
Toen de stamcellen het Zika-omhullingsproteïne produceerden, leken ze nog gezond en behielden ze hun brede potentie om veel weefsels te vormen. Toen ze zich echter ongeremd mochten differentiëren, was hun vermogen om complexe 3D-clusters te vormen die de drie basisweefsellagen van het embryo representeren sterk verminderd, en daalden markers van alle drie de lagen. Dit suggereert dat het virale eiwit de stamcellen niet rechtstreeks doodt, maar subtiel hun vermogen verstoort om aan normale ontwikkelingspaden te beginnen. Een gemuteerde versie van het eiwit, zonder een specifieke suikeraanhangsel, veranderde dit patroon op een ongelijkmatiger manier, wat suggereert dat de fijne chemische versiering van het eiwit bepaalt hoe het ontwikkeling schaadt.
Het blokkeren van de weg van stamcel naar neuron
De onderzoekers richtten zich vervolgens specifiek op de overgang van stamcel naar vroege neuron met twee gevestigde labmodellen: een plat “monolaag”-cultuur en een 3D “neurosfeer”-cultuur die het vroege hersenweefsel nabootst. In beide systemen namen bij de controles de expressie van markers voor neurale stamcellen en neuronen in de loop van dagen soepel toe, en vormden zich georganiseerde rozetten en vele jonge neuronen. Cellen die het omhullingsproteïne maakten, produceerden daarentegen veel minder neurale stamcellen, minder rozetten en aanzienlijk minder vroege neuronen, wat zichtbaar was door gereduceerde niveaus van cruciale genen en eiwitten die met zenuwidentiteit geassocieerd zijn. De suikervrije mutant veroorzaakte over het algemeen een nog sterkere blokkade op genniveau en activeerde extra ontstekingsgerelateerde celdoodroutes, wat wijst op een mechanisme voor ernstigere schade.
Communicatiegedempt in jonge zenuwnetwerken
Om te begrijpen wat er intracellulair fout ging, vergeleek het team de globale genactiviteit in normale cellen en cellen die het omhullingsproteïne produceerden op kritieke differentiatiestadia. Ze vonden dat veel genen die verband houden met zenuwgroei, synapsvorming en de kleine uitsteeksels op dendrieten die herinneringen opslaan, werden onderdrukt. Routes die betrokken zijn bij het laden en vrijgeven van neurotransmitters, het verbinden van axonen met hun doelen en het samenstellen van synapsen, waren allemaal geremd. Tegelijkertijd werden signaalwegen gekoppeld aan calcium en bepaalde celoppervlaktereceptoren geactiveerd, wat de cellen mogelijk te prikkelbaar of verkeerd gesignaleerd maakte. Deze ingrijpende veranderingen verschenen zowel in platte als in 3D-culturen, wat aantoont dat het omhullingsproteïne herhaaldelijk ontwikkelende neurale cellen wegstuurt van het opbouwen van robuuste, goed verbonden netwerken.
Wat dit betekent voor Zika-gerelateerde geboorteafwijkingen
Voor niet-specialisten is de kernboodschap dat het zikavirus niet actief hoeft te repliceren en cellen te doden om de zich ontwikkelende hersenen te schaden. Dit werk toont aan dat het buitenste omhulselproteïne op zichzelf vroege stamcellen van het normale pad naar neuronvorming kan duwen, en de genetische programma’s die nodig zijn voor gezonde synapsen en dendritische spinnen kan verzwakken. Zulke vroege, stille verstoringen helpen te verklaren hoe blootstelling in de baarmoeder kan leiden tot aandoeningen zoals microcefalie en langdurige cognitieve problemen. De bevindingen waarschuwen ook dat vaccins of therapieën die omhullingsproteïnen gebruiken zorgvuldig moeten worden beoordeeld op mogelijke effecten op hersenontwikkeling, zelfs wanneer er geen levend virus aanwezig is.
Bronvermelding: Ma, ZH., Wang, Y., Hassaan, N.A. et al. ZIKV envelope protein is a strong blocker of early directional differentiation in the neural lineage. Commun Biol 9, 395 (2026). https://doi.org/10.1038/s42003-026-09672-1
Trefwoorden: Zikavirus, hersenontwikkeling, neurale stamcellen, viraal omhullingsproteïne, microcefalie