Clear Sky Science · nl
Single-cell-transcriptomica onthult mechanismen van skeletspierdifferentiatie tijdens eendembryonale ontwikkeling
Waarom de ontwikkeling van eendenspieren ertoe doet
Skeletspier stelt dieren in staat te bewegen en te vliegen en bepaalt bij landbouwdieren ook de textuur en smaak van hun vlees. Deze studie richt zich op hoe de borstspier van Pekingeenden zich vormt vóór het uitkomen, met krachtige single-cell-methoden om tienduizenden individuele cellen te volgen terwijl ze groeien en specialiseren. Door de ontwikkeling van elke cel te volgen van een vroeg, stamcelachtig stadium tot een volledig gevormde spiervezel, onthullen de onderzoekers hoe verschillende spiervezeltypen ontstaan, hoe ze van identiteit kunnen wisselen en welke regels daarbij vogels en zoogdieren gemeen hebben.
Spieropbouw vanuit de vroegste cellen
Eendenspieren beginnen als een mengeling van sterk flexibele, stamcelachtige cellen in het vroege embryo. Het team stelde een gedetailleerde “cellenatlas” samen door het RNA te sequencen van bijna 77.000 enkele cellen uit eendembryo’s op tien tijdstippen, van zeer vroege ontwikkeling tot het uitkomen. Ze vonden twee hoofdgroepen van stamcellen die de vroegste fasen domineren en geleidelijk vele ondersteunende en spiervormende celtypen voortbrengen. Onder deze cellen lijkt een subset van mesenchymale stamcellen, gemarkeerd door het molecuul MYL9, de belangrijkste bron van toekomstige spierprogenitorcellen te zijn. Na verloop van tijd differentiëren deze progenitoren tot myoblasten die samensmelten tot grotere structuren en uiteindelijk de lange, meerkernige vezels vormen die functionele spier geven.
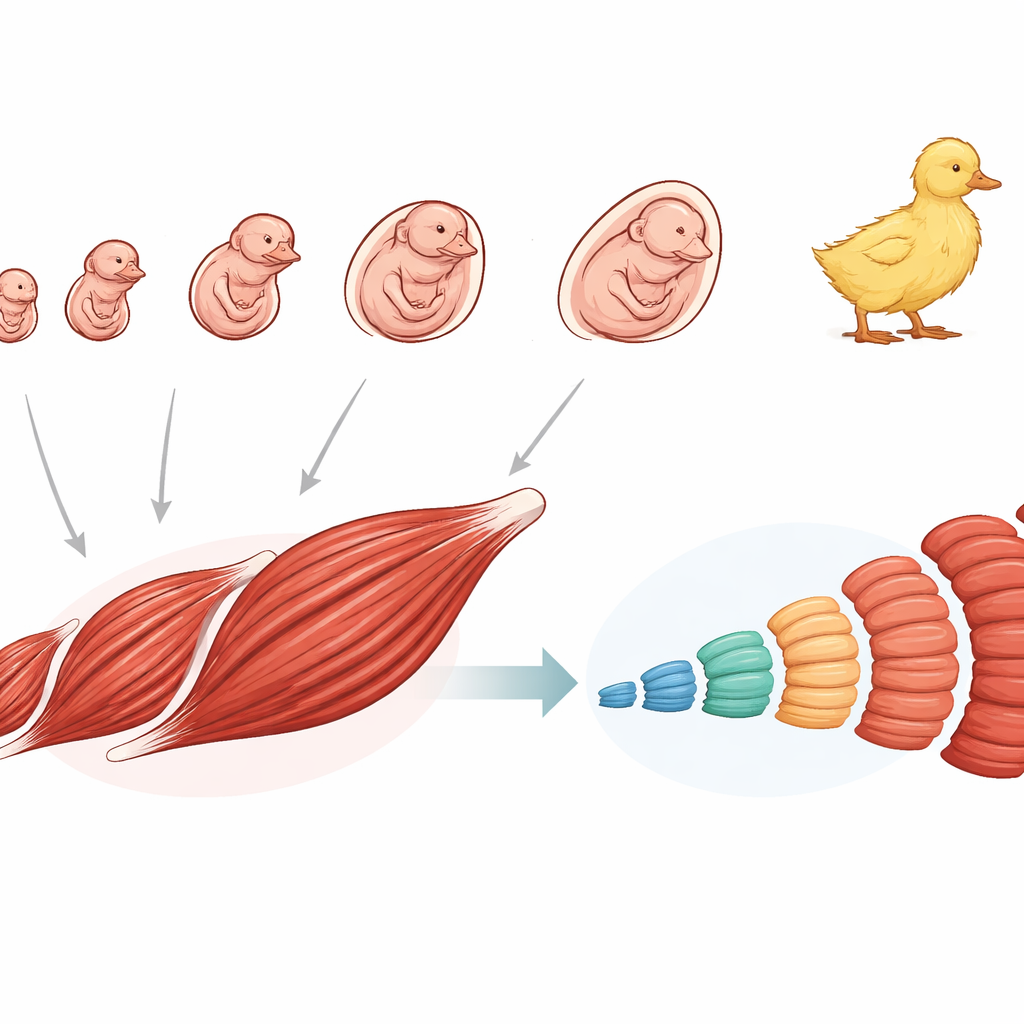
Twee belangrijke takken: werkende vezels en cellen die repareren
Toen de onderzoekers spierlijncellen volgden over ontwikkelings-“pseudotijd”, zagen ze dat vroege progenitoren zich opsplitsten in twee grote takken. De ene tak produceert de volwassen spiervezels die nodig zijn voor contractie. De andere vormt satellietcellen, de langlevende “reparatieploeg” die meestal inactief blijft totdat ze later in het leven nodig zijn voor groei of regeneratie. Langs de satellietceltak worden specifieke genen gecoördineerd aan- en uitgezet, waardoor cellen van een rusttoestand naar actieve, delende cellen verschuiven. De analyse wijst op een handvol regelgevende genen die waarschijnlijk als schakelaars voor dit activatieproces fungeren. In de tak die vezels maakt, benadrukt de studie cellulaire processen zoals membraantransport en cel–cel-adhesie die cruciaal zijn voor myoblasten om te fuseren en robuuste spiervezels op te bouwen.
Hoe langzame vezels snel worden
Een van de meest opvallende bevindingen is dat spiervezels niet simpelweg vanaf het begin als “langzaam” of “snel” worden gevormd. In plaats daarvan zijn vroege eendentwikkelingen rijk aan langzame (slow-twitch) vezels—beter in steady, uithoudingsachtige arbeid—terwijl snelle (fast-twitch) vezels die snelle, krachtige bewegingen aandrijven zeldzaam zijn. Naarmate het embryo rijpt, keert dat evenwicht zich om. Door genactiviteit binnen individuele vezels te volgen, ontdekten de onderzoekers een stapsgewijze “langzaam-naar-snel” transitie. Langzame vezels doorlopen een tussenstaat, inclusief een nieuw beschreven subtyp gemarkeerd door de factor LEF1, en verwerven vervolgens kenmerken van snelle vezels. Onderweg vertonen sommige vezels tijdelijk een hybride identiteit met eigenschappen van zowel langzame als snelle typen, wat wijst op een flexibele periode waarin hun lot nog veranderbaar is.
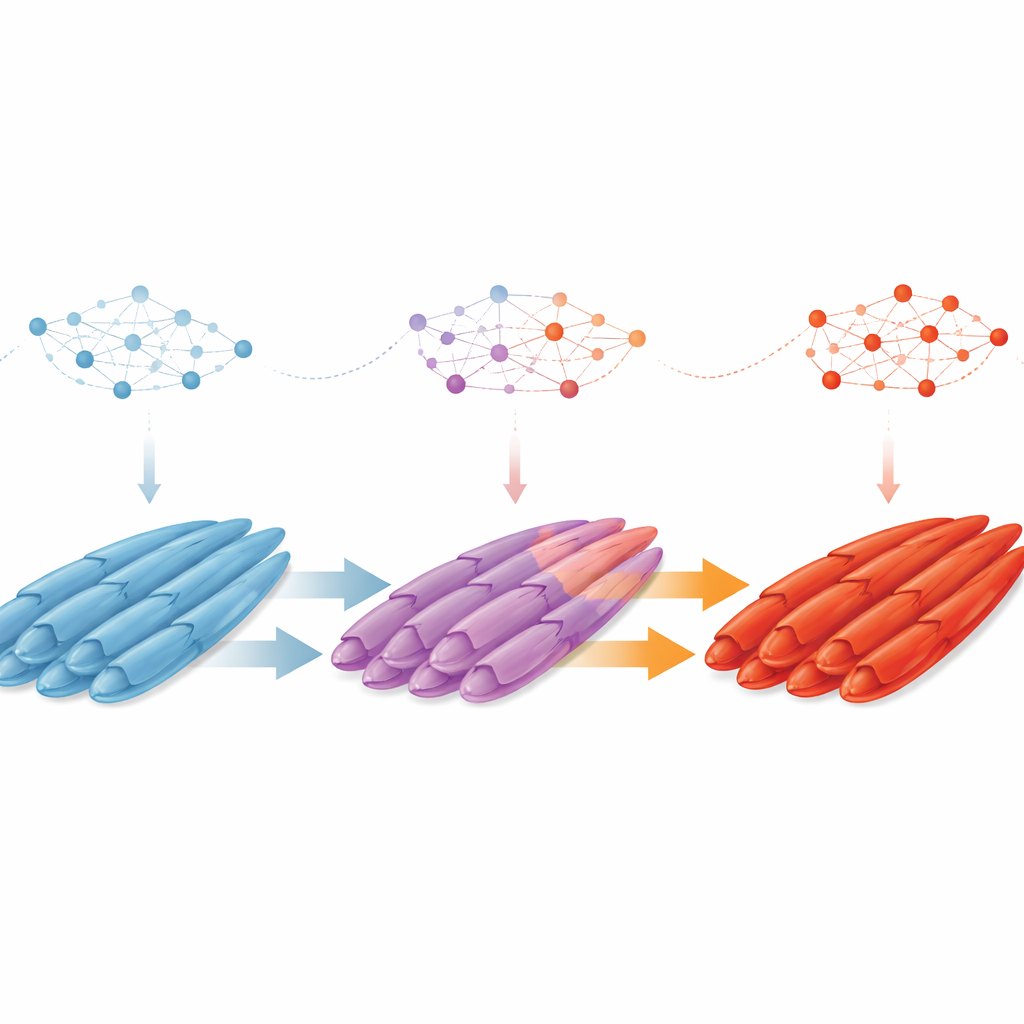
Regelgevende genen en gedeelde principes tussen soorten
Het team onderzocht vervolgens wat deze verschuiving in vezelidentiteit reguleert. Door gennetwerken te reconstrueren identificeerden ze 13 sleuteltranscriptiefactoren—meesterregelaars die groepen genen coördineren—die cellen leiden van vroege progenitoren via myoblasten naar rijpende vezels en satellietcellen. Twee factoren, TBX15 en PBX3, springen eruit als sterke kandidaten om vezels van langzaam naar snel gedrag te sturen, via bekende groeioverlevingsroutes zoals PI3K–Akt en receptor-tyrosinekinase-signaleringspaden. Ten slotte tonen vergelijkingen van de eendgegevens met single-cell-kaarten van varkens, kippen en muizen aan dat veel celtypen, markergenen en zelfs het algemene patroon van de langzaam-naar-snel overgang geconserveerd zijn tussen vogels en zoogdieren. Dit suggereert dat diepgewortelde, gedeelde genetische programma’s bepalen hoe werveldier spieren specialiseren.
Wat dit betekent voor biologie en daarbuiten
Voor niet-specialisten is de belangrijkste conclusie dat spiervezels niet vanaf geboorte vastliggen: bij eenden, en waarschijnlijk bij veel wervels, kunnen vroege langzame vezels transformeren naar snelle vezels via een goed georganiseerde reeks tussenstaten die worden bestuurd door specifieke genen en signaalroutes. Het begrijpen van deze routekaart helpt verklaren hoe dieren hun spieren afstemmen voor vliegen, rennen of andere taken en waarom vezelsamenstelling de vleeskwaliteit beïnvloedt. Op de lange termijn kunnen dezelfde principes strategieën informeren om spierekens van vee te verbeteren of regeneratieve therapieën te ontwerpen die menselijke spieren herbouwen of hervormen na letsel of ziekte.
Bronvermelding: Sun, Y., Li, Z., Jie, Y. et al. Single-cell transcriptomics reveal mechanisms of skeletal muscle differentiation across duck embryonic development. Commun Biol 9, 404 (2026). https://doi.org/10.1038/s42003-026-09665-0
Trefwoorden: ontwikkelingen van skeletspier, spiervezeltypen, single-cell-transcriptomica, eendembryogenese, overgang van langzaam naar snel vezeltype