Clear Sky Science · nl
Activering van het cytomegalovirus-gecodeerde G-eiwit-gekoppelde receptor UL33 door een inwendig N-terminaal peptide
Hoe een veelvoorkomend virus onze cellen herbedrading
Het humane cytomegalovirus (HCMV) infecteert stilletjes de meeste mensen op aarde en blijft meestal onopgemerkt. Toch kan het bij pasgeborenen, transplantatiepatiënten en anderen met een verzwakt immuunsysteem ernstige ziekte veroorzaken. Deze studie onthult, op moleculair niveau, hoe één viraal eiwit genaamd UL33 fungeert als een ingebouwde schakelaar die geïnfecteerde cellen voortdurend in het voordeel van het virus duwt. Inzicht in deze verborgen schakelaar helpt verklaren hoe HCMV levenslang kan aanblijven en wijst op nieuwe manieren om het te ontwapenen zonder normale celsignalering te schaden.
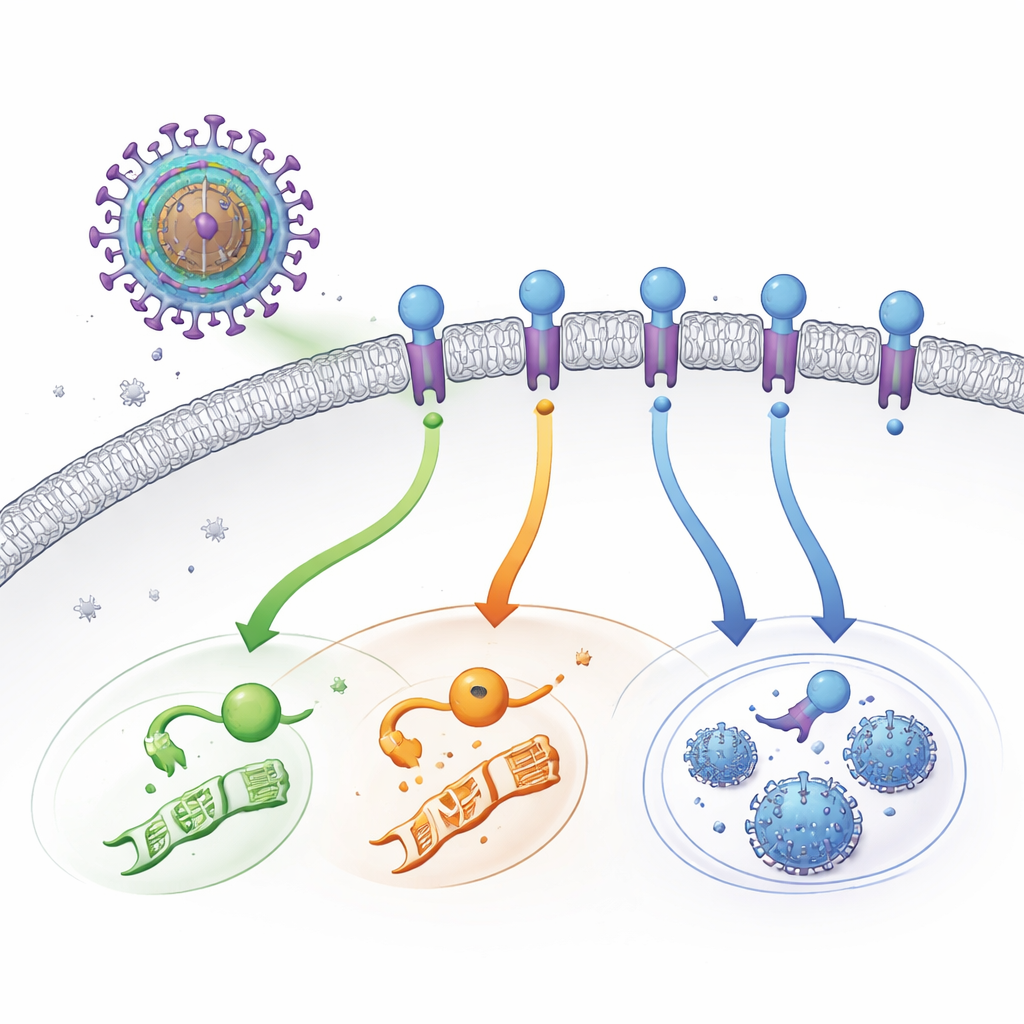
Een heimelijke virale schakelaar op het celoppervlak
HCMV draagt zijn eigen versies van receptoren op het celoppervlak — eiwitten die normaal hormonen of immuunsignalen waarnemen. UL33 is een van deze virale receptoren. Anders dan typische receptoren, die wachten op een extern signaal, staat UL33 “altijd aan”. Zodra het in het buitenmembraan van een geïnfecteerde cel is geplaatst, kan het tegelijk op meerdere van de belangrijkste communicatiepaden van de cel inschakelen. Deze paden regelen processen zoals genactiviteit, metabolisme en de beslissing om in rust te blijven of meer virus te produceren. Jarenlang wisten wetenschappers dat UL33 actief was, maar niet wat het aanzette, vooral omdat er nooit een extern activerend molecuul (ligand) was gevonden.
Een zelfstart: de receptor die zijn eigen sleutel meebrengt
Met behulp van geavanceerde cryo-elektronenmicroscopie legden de auteurs driedimensionale momentopnames vast van UL33 gebonden aan een van de signaalpartners van de cel, een G-eiwit genaamd Gs. De beelden tonen dat het allereerste gedeelte van het UL33-eiwit — de korte N-terminale staart — terugvouwt in een holte op de receptor zelf, veel als een sleutel die permanent in een slot is achtergelaten. Deze “verankerde” staart nestelt zich in een klein zijvak dat bij verwante menselijke receptoren normaal gesproken een deel van een immuunsignalerend eiwit, een chemokine, zou ontvangen. Door dit vak van meet af aan in te nemen, blokkeert UL33 de binding van buitenkomende chemokines volledig, wat verklaart waarom het zich gedraagt als een “wees”receptor die niet op normale gastheerboodschappers reageert.
Cruciale atomen in de virale aan‑schakelaar
Om te bevestigen dat deze ingebouwde staart daadwerkelijk de trigger is, veranderde het team systematisch individuele bouwstenen van UL33 in menselijke cellen. Ze concentreerden zich op de eerste paar aminozuren van de staart en corresponderende punten binnenin het vak die deze vastgrijpen. Toen ze deze sleutelresiduen vervingen door neutralere aminozuren of een ervan helemaal verwijderden, zakte UL33’s signalering bijna tot nul — hoewel de gewijzigde receptoren nog steeds in normale hoeveelheden het celoppervlak bereikten. Met andere woorden: het eiwit was aanwezig maar stil. Dit toont aan dat de staart niet slechts structurele versiering is; het is het essentiële zelf-activerende onderdeel dat UL33 ingeschakeld houdt.
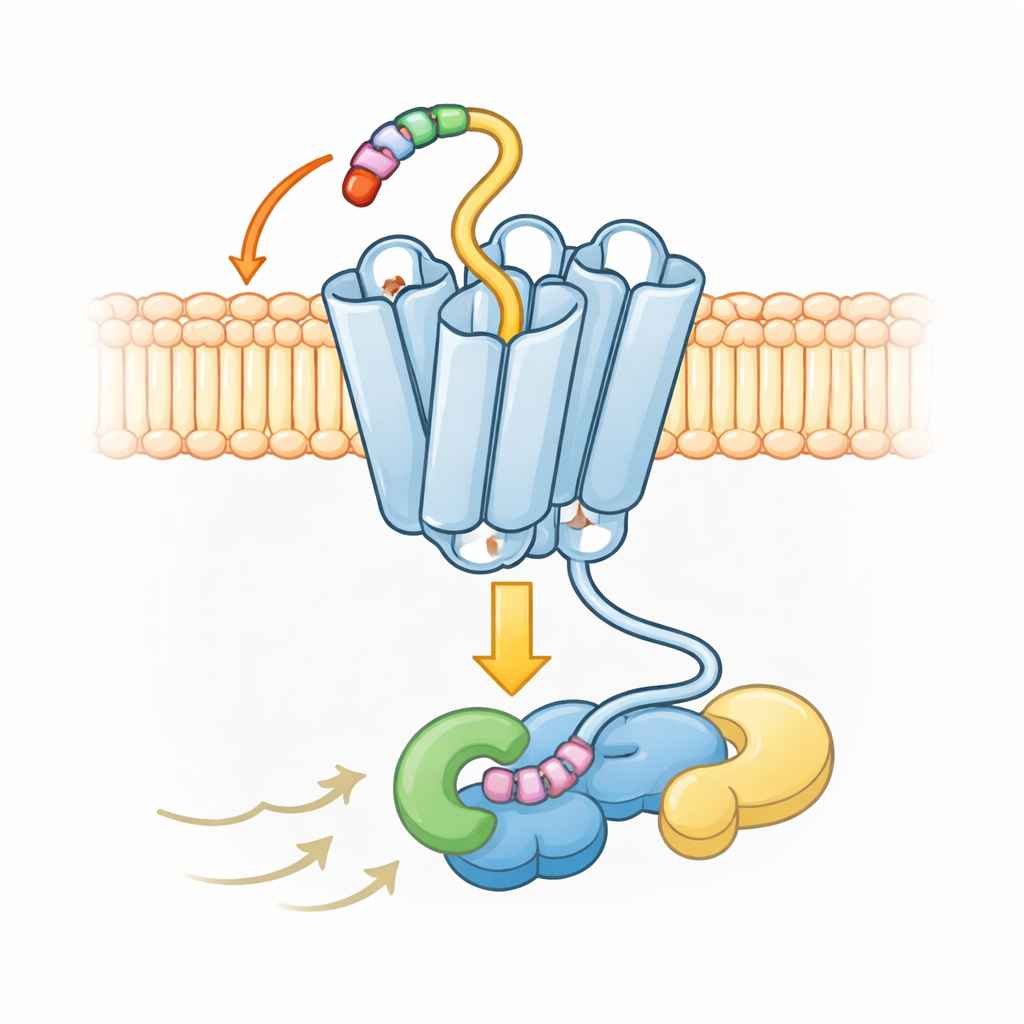
Een ongebruikelijke vorm voor brede maar gecontroleerde signalering
De structurele kaarten laten ook zien dat UL33 een iets andere actieve vorm aanneemt vergeleken met typische menselijke receptoren. Bij de meeste receptoren uit deze familie zwaait een van de zeven helixen nabij de binnenkant van de cel dramatisch naar buiten wanneer de receptor geactiveerd wordt, waardoor een grote holte ontstaat waarin G-eiwitten kunnen aanhaken. Bij UL33 blijft die helix veel dichter bij het centrum, wat een strakkere passing creëert. Desondanks kan UL33 nog steeds met verschillende soorten G-eiwitten samenwerken — Gs, Gq en Gi — door precieze contacten te maken met de punt van het G-eiwit die in de receptor past. Deze contacten bevoordelen sommige G-eiwitten en sluiten andere uit, zoals de G12/13-groep, waardoor het virus de reacties van de cel kan sturen zonder ongecontroleerde signalering los te laten.
Nieuwe kwetsbaarheden voor een oud virus
Door structurele beeldvorming te combineren met functionele tests schetst de studie een helder beeld: UL33 is een zelfstartende virale receptor waarvan de eigen staart fungeert als een permanent aangehechte activator. Dit ontwerp stelt HCMV in staat de signaalering van gastheercellen subtiel maar persistent bij te sturen om virale replicatie en reactivatie te ondersteunen, vooral door paden te versterken die virale genen aanzetten. Tegelijkertijd onthult het werk zwakke punten die door geneesmiddelen kunnen worden aangesproken, zoals een smalle tunnel die naar het vak leidt waar de staart bindt. Moleculen die in dit gebied klemmen of de staart verplaatsen, zouden UL33’s activiteit kunnen dempen en de virale schade verminderen, terwijl de normale receptoren van het lichaam gespaard blijven. Voor patiënten die risico lopen door HCMV zou het richten op deze virale “meesterschakelaar” op termijn een preciezere manier kunnen bieden om het virus onder controle te houden.
Bronvermelding: Drzazga, A.K., Suzuki, S., Wouters, C. et al. Activation of cytomegalovirus-encoded G protein-coupled receptor UL33 by an innate N-terminal peptide. Commun Biol 9, 415 (2026). https://doi.org/10.1038/s42003-026-09660-5
Trefwoorden: cytomegalovirus, viraal GPCR, celsignalering, cryo-EM-structuur, doelwit voor geneesmiddelen