Clear Sky Science · nl
Onderzoek naar Salmonella-biofilmreacties op antibiotische behandeling met optische photothermale infraroodspectroscopie
Waarom kleverige bacteriesteden ertoe doen
Veel ziekteverwekkende bacteriën leven bij voorkeur in dicht opeengepakte gemeenschappen die biofilms worden genoemd, waarin cellen aan elkaar en aan oppervlakken in het lichaam of aan medische apparaten vastplakken. Binnen deze slijmerige “steden” kunnen microben antibiotica naast zich neerleggen die hen normaal gesproken zouden doden. Deze studie introduceert een nieuwe manier om biofilms in fijne details te bekijken, waardoor zichtbaar wordt welke cellen actief groeien en hoe ze reageren wanneer krachtige geneesmiddelen worden toegevoegd. Inzicht in deze onzichtbare activiteitspatronen kan artsen helpen behandelingen te ontwerpen die eindelijk de koppige verdediging van biofilms doorbreken.
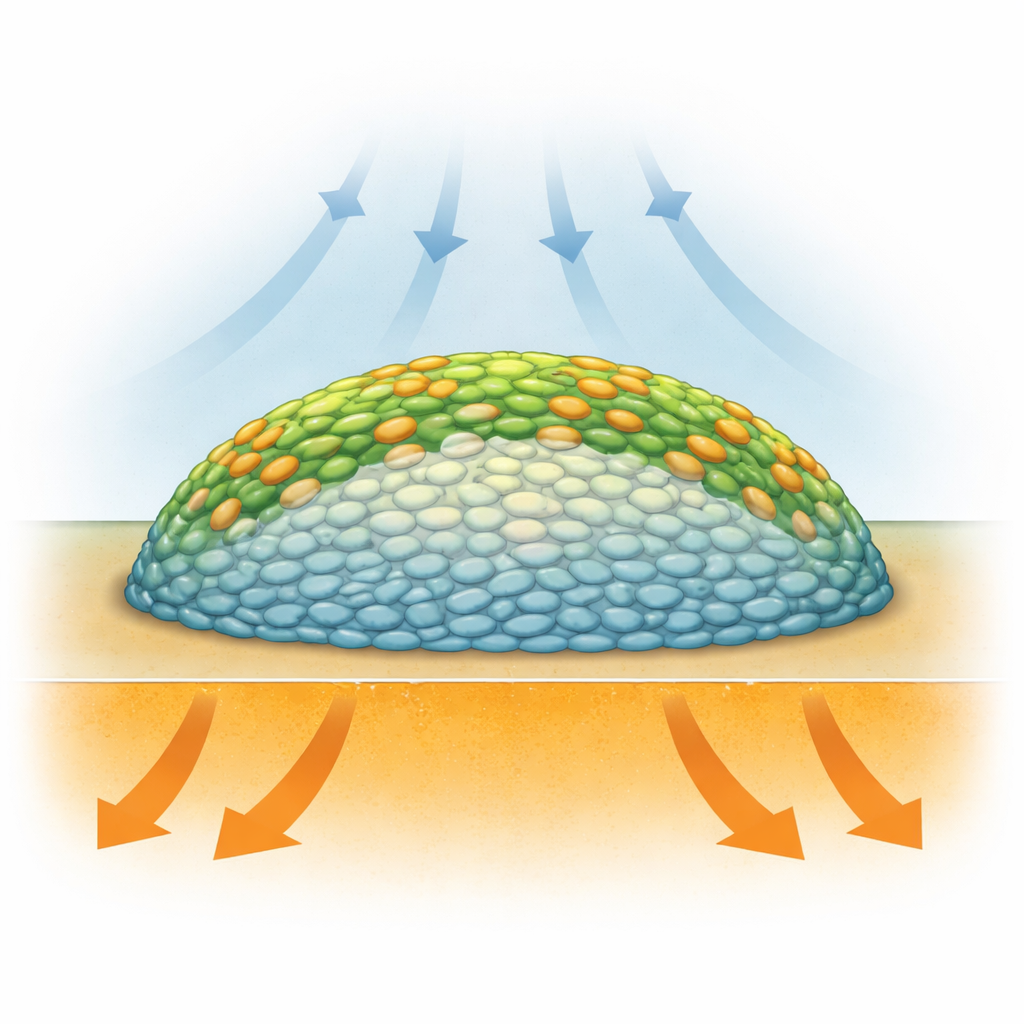
Verborgen leven binnen bacteriesteden
Biofilms zijn geen willekeurige klonteringen van microben: het zijn gelaagde structuren waarin bacteriën sterk verschillende omstandigheden ervaren, afhankelijk van hun positie. Cellen aan de buitenkant hebben meer toegang tot zuurstof uit de lucht, terwijl de in het midden ingesloten cellen zuurstoftekort hebben en kunnen vertragen of in dormantie gaan. Eerdere methoden zoals fluorescentiemicroscopie konden wel structuur laten zien, maar vereisten vaak toegevoegde kleurstoffen of genetische tags die de biologie kunnen verstoren, en ze maten niet rechtstreeks wat de cellen chemisch deden. Onderzoekers hadden een manier nodig om de chemie van levende biofilms laag voor laag te ‘‘zien’’, zonder ze uiteen te scheuren of sterk te veranderen.
De chemie zien met onzichtbaar licht
Het team wendde zich tot een techniek die optische photothermale infraroodspectroscopie (O-PTIR) heet, die pulsen van onzichtbaar infraroodlicht en een zichtbare laser gebruikt om minuscule trillingen in moleculen te detecteren. Deze trillingen fungeren als vingerafdrukken van belangrijke celcomponenten, zoals eiwitten, vetten en DNA. Om het metabolisme—het actieve gebruik van voedingsstoffen—te volgen, voedden ze Salmonella Typhimurium-biofilms met een speciale vorm van suiker waarin de koolstofatomen iets zwaarder waren dan gewoonlijk (een stabiel isotoop bekend als koolstof-13). Wanneer cellen druk bezig zijn met groeien en nieuwe eiwitten maken, bouwen ze deze zwaardere atomen in hun structuren in, wat subtiele maar detecteerbare verschuivingen in het infraroodsignaal veroorzaakt. Door de biofilm te cryosectioneren en dunne dwarsdoorsneden te scannen, maakten de onderzoekers chemische kaarten die lieten zien waar in de biofilm deze zware koolstof was ingebouwd.
Activiteitsringen en stille kernen
Infraroodbeeldvorming van onbehandelde Salmonella-biofilms toonde een opvallend patroon: de buitenste regio’s en oppervlaktelagen vertoonden sterke opname van de zware koolstof, terwijl een groot centraal kerngebied zeer weinig liet zien. Met andere woorden, de biofilm gedroeg zich als een ring van actieve cellen rondom een rustige binnenkant. Statistische analyse van de infraroodspectra bevestigde dat signalen van eiwitgerelateerde trillingen meer verschoof in de buitenste lagen dan in het centrum, wat duidt op hogere eiwitsynthese aan de randen. Deze bevindingen ondersteunen het idee dat zuurstofbeschikbaarheid, die het grootst is nabij het oppervlak, de belangrijkste aanstichter is van metabolische ‘‘hete zones’’ in dit koloniemodel, zelfs hoewel voedingsstoffen van onderen binnenstromen. De studie leverde een van de duidelijkste, hoogst-resolverende beelden tot nu toe van hoe het metabolisme binnen een biofilm gelaagd is.
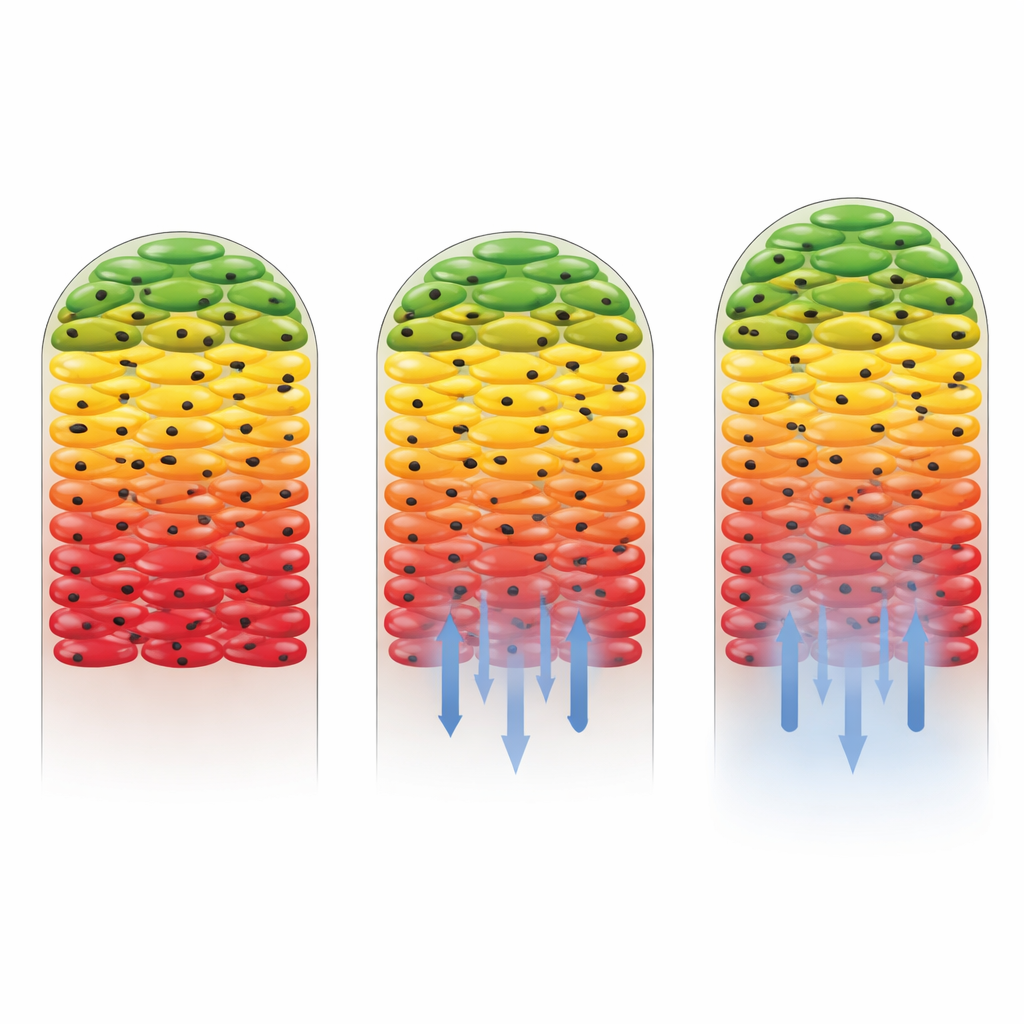
Hoe verschillende antibiotica de biofilmactiviteit hervormen
Vervolgens onderzochten de onderzoekers wat er gebeurt wanneer antibiotica worden toegediend. Ze gebruikten twee middelen: kanamycine, waartegen de Salmonella-stam gevoelig is, en gentamicine, waarvoor de stam grotendeels onvatbaar was gemaakt. Wanneer gentamicine aanwezig was, veranderde het algehele patroon van actieve buitenlagen en een stille kern nauwelijks, wat aantoont dat resistente cellen doorgroeiden en zware koolstof in grote delen van de biofilm bleven opnemen. Daarentegen verminderde kanamycine de metabole activiteit drastisch, vooral nabij de onderkant van de biofilm waar de geneesmiddelconcentratie het hoogst was. Alleen een dunne band cellen het verst van de antibiotica-bron verwijderd toonde nog tekenen van koolstofopname. Dit toonde niet alleen aan dat het middel effectief was, maar ook dat de biofilmstructuur sommige cellen hielp te beschermen door het middel te verzwakken terwijl het naar binnen diffundeerde.
Nieuwe vensters voor de behandeling van hardnekkige infecties
Voor een breed publiek is de kernboodschap dat dit werk een krachtig ‘‘chemisch microscoop’’ biedt om te observeren hoe bacteriegemeenschappen leven en behandelingen overleven in drie dimensies. Door een niet-destructieve infraroodbeeldvormingsmethode te combineren met een veilige zware koolstofvorm, konden de onderzoekers precies vaststellen waar bacteriën actief groeiden en hoe die activiteit verschoof onder verschillende antibiotica. Hun resultaten bevestigen dat biofilms een mix van drukke en vrijwel inactieve cellen huisvesten, en dat effectieve middelen toch afgezwakt kunnen worden door de fysieke barrière van de biofilm. In de toekomst kan deze benadering worden gebruikt om nieuwe therapieën te testen, te onderzoeken hoe verschillende soorten samenwerken of resistentie delen in gemengde biofilms, en uiteindelijk slimmer strategieën te ontwerpen om hardnekkige infecties uit te roeien.
Bronvermelding: Smaje, D., Zhu, X., Hinton, J.C.D. et al. Investigating Salmonella biofilm responses to antibiotic treatment using optical photothermal infrared spectroscopy. Commun Biol 9, 405 (2026). https://doi.org/10.1038/s42003-026-09655-2
Trefwoorden: biofilms, Salmonella, antibioticaresistentie, infraroodbeeldvorming, stabiele isotopenonderzoek