Clear Sky Science · nl
Modelselectie in preklinisch onderzoek naar nucleïnezuurtherapieën
Genen omzetten in geneesmiddelen
Nucleïnezuurtherapieën zijn een nieuw soort geneesmiddel dat niet werkt door eiwitten te blokkeren, zoals de meeste medicijnen, maar een stap eerder ingrijpt op het niveau van onze genetische boodschappen. Deze review legt uit hoe wetenschappers de juiste laboratorium- en diermodellen kiezen om deze RNA-richtende middelen te testen voordat ze patiënten bereiken. Een niet-specialistische lezer zou hierom geven omdat slimme modelkeuzes kunnen zorgen voor snellere, veiligere en effectievere behandelingen voor genetische aandoeningen, inclusief zeldzame kinderziekten en meer voorkomende aandoeningen zoals hartziekte.
Wat maakt deze genetische geneesmiddelen anders?
Nucleïnezuurtherapieën (NATs) omvatten korte strengen die antisense-oligonucleotiden (ASO’s) en small interfering RNAs (siRNA’s) worden genoemd. In plaats van te vertrouwen op de vorm en chemie van eiwitdoelen, herkennen deze middelen hun doelmoleculen door base‑paringregels—dezelfde A‑T en G‑C‑matching die ten grondslag ligt aan DNA. Dat maakt ze programmeerbaar: zodra je de RNA‑sequentie kent die je wilt veranderen, kun je vaak snel veel kandidaatmiddelen ontwerpen zonder jaren van traditionele chemie. Het lastige is niet langer “Kunnen we een actief bestanddeel maken?” maar “Hoe meten we of het echt werkt in een realistische biologische omgeving?” Omdat zelfs een enkel letterverschil in de sequentie activiteit kan maken of breken, wordt de keuze van de juiste testsystemen cruciaal.
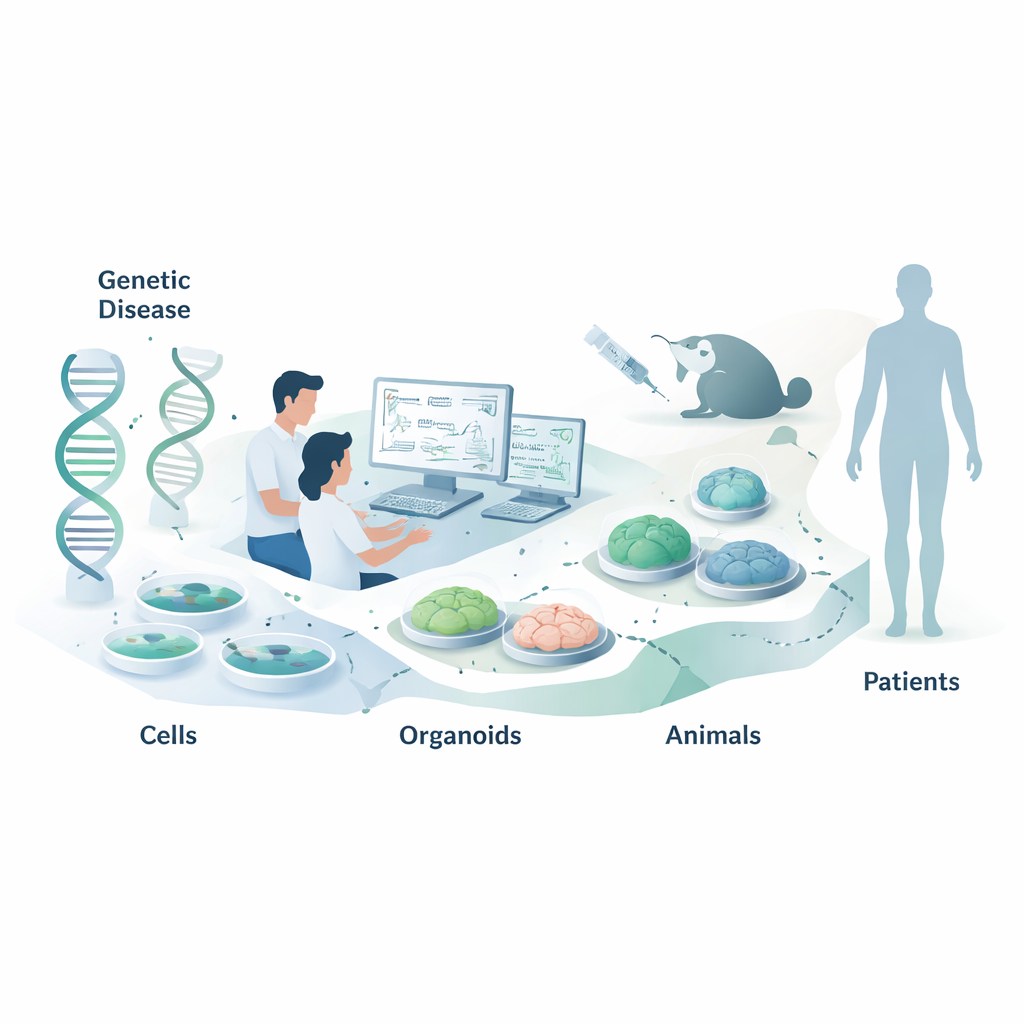
Eenvoudige celtests: snel maar niet het hele verhaal
De eerste halte voor de meeste NATs is een paneel van relatief gemakkelijk te kweken cellijnen, zoals HeLa- of HEK293-cellen, die het doel‑RNA al produceren. Onderzoekers voegen grote bibliotheken van kandidaat-ASO’s of siRNA’s toe en meten vervolgens hoeveel het doel‑RNA en het bijbehorende eiwit afnemen, met technieken zoals PCR en Western blotting. Ze werken mogelijk ook met cellen van patiënten, die iemands exacte genetische achtergrond beter vastleggen en het testen van “allel-selectieve” middelen mogelijk maken die alleen de foutieve kopie van een gen stilleggen. Wanneer het natuurlijke gen niet vanzelfsprekend tot expressie komt, introduceren wetenschappers soms kunstmatige mini-genen of reporterplasmiden die oplichten wanneer het RNA wordt geknipt of correct gespliced. Deze systemen zijn krachtig om veel ontwerpen snel te vergelijken, maar ze kunnen belangrijke details missen, zoals natuurlijke RNA-structuur of celspecifieke verwerking, dus de resultaten moeten worden bevestigd in realistischere contexten.
Van moleculaire reparatie naar echt celgedrag
Veel NATs streven er niet alleen naar fout RNA te vernietigen maar het te herstellen door splicing te beïnvloeden, het proces dat stukjes van de genboodschap aan elkaar plakt. Zorgvuldig ontworpen ASO’s kunnen ervoor zorgen dat cellen een schadelijk exon overslaan, een ontbrekend stuk herstellen of de invoeging van een “pseudo‑exon” voorkomen dat de code verbreekt. Om te zien of zulke veranderingen werkelijk de celfunctie verbeteren, gaan onderzoekers verder dan eenvoudige metingen van RNA- en eiwitniveaus. In patiëntafgeleide cellen testen ze of enzymactiviteit terugkeert, of ionentransport in longcellen normaliseert, of signaleringspaden in immuuncellen correct reageren. Steeds vaker gebruiken ze driedimensionale organoïden—mini‑weefsels gekweekt uit stamcellen van patiënten—die hartslagen, netwerkactiviteit van de hersenen of ander complex gedrag kunnen nabootsen. Deze 3‑D‑modellen liggen dichter bij echte organen maar zijn moeilijker, trager en duurder te gebruiken, dus teams moeten realisme afwegen tegen doorvoersnelheid.
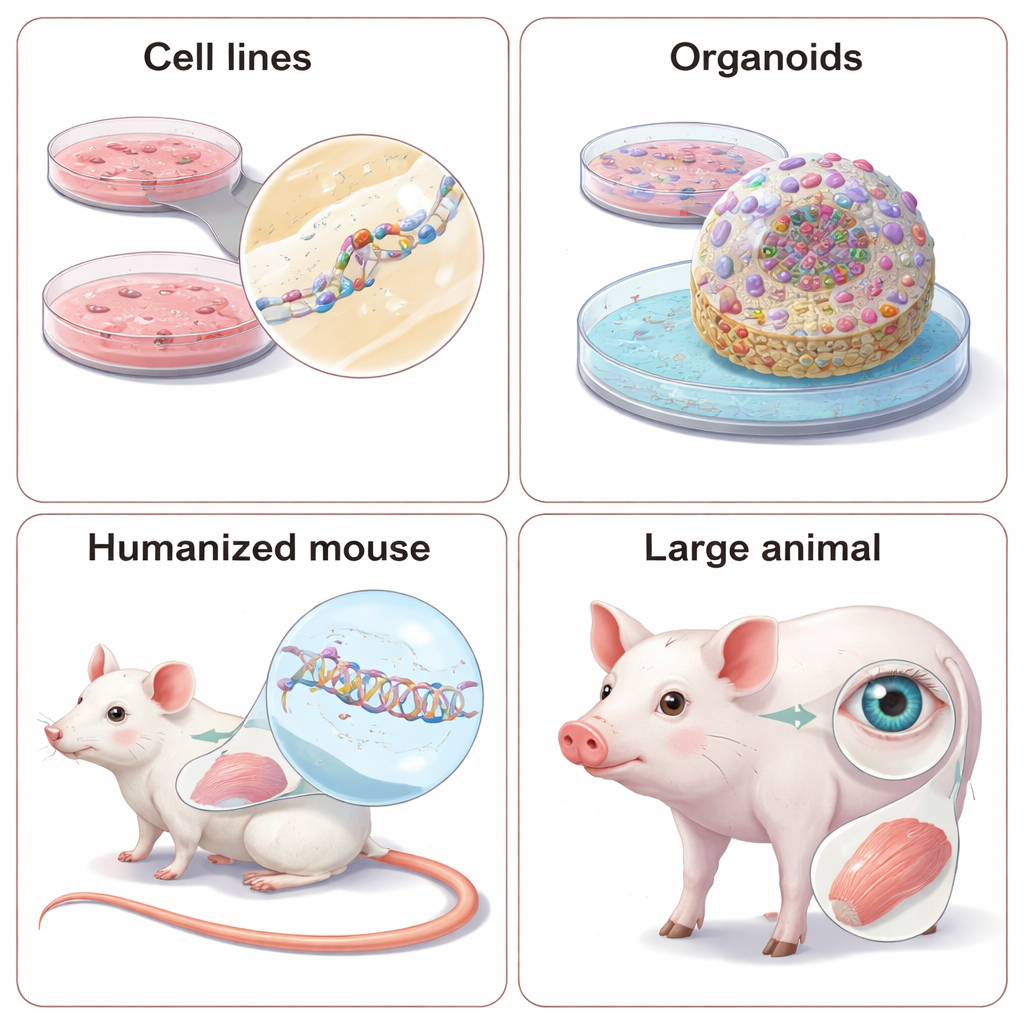
Waarom dieren nog steeds belangrijk zijn—en hoe ze te humaniseren
Sommige ziektekenmerken, zoals volledig lichaamsmetabolisme, orgaan‑tot‑orgaaninteracties of gedrag, kunnen simpelweg niet in schaaltjes worden vastgelegd. Hiervoor worden NATs getest in levende dieren. Omdat deze middelen letten op exacte RNA‑sequenties, staan wetenschappers voor een keuze: ontwerp “surrogaat”middelen die passen bij de dierlijke versie van het gen, of herontwerp het dier zodat het menselijke genetische sequenties draagt. Surrogaat‑ASO’s en siRNA’s kunnen aantonen of verlaging van een gen symptomen verbetert in goed onderzochte muismodellen, maar ze bootsen het humane doelmiddel niet perfect na. Gehumaniseerde modellen—muizen of zelfs minivarkens met secties of volledige kopieën van menselijke genen—maken testen van de echte klinische kandidaat mogelijk maar vergen aanzienlijke tijd en kosten, en subtiele verschillen in genregulatie tussen soorten kunnen nog steeds tot verrassingen leiden. De review belicht ook het groeiende gebruik van grote dieren, vooral voor ziekten van oog en spier, waar de anatomie meer lijkt op die van mensen.
Vooruitkijken: slimmere modellen en minder giswerk
De auteurs concluderen dat er niet één “beste” model is voor nucleïnezuurmiddelen; in plaats daarvan heeft elk project een op maat gemaakt traject nodig dat begint met snelle, eenvoudige assays en doorwerkt naar complexere, mensrelevante systemen. Naarmate regelgevers en financiers aandringen op verminderd dierengebruik, wordt verwacht dat geavanceerde organoïden, organ‑on‑a‑chip‑apparaten en computermodellen een groter deel van de last zullen dragen, vooral in combinatie met machine learning‑tools die voorspellen welke sequenties en chemieën het beste zullen werken. Uiteindelijk kunnen onderzoekers, door de sterke punten en blinde vlekken van elk model te begrijpen—en door best practices en data binnen het veld te delen—programmatische genetische ideeën betrouwbaarder omzetten in veilige, effectieve geneesmiddelen voor patiënten.
Bronvermelding: Oliver, P.L., Hill, A.C. Model selection in preclinical nucleic acid therapeutics research. Commun Biol 9, 200 (2026). https://doi.org/10.1038/s42003-026-09650-7
Trefwoorden: nucleïnezuurtherapieën, antisense-oligonucleotiden, siRNA, preklinische modellen, gentherapie