Clear Sky Science · nl
Wnt11 bemiddelt de interactie tussen fibroblasten en gladde spiercellen en bevordert neurogene blaasfibrose bij ratten
Wanneer zenuwen falen, litteken de blaas
Veel mensen met een dwarslaesie, multiple sclerose of de ziekte van Parkinson ontwikkelen een "neurogene blaas", waarbij beschadigde zenuwen urineopslag en -lediging niet meer goed kunnen aansturen. Na verloop van tijd kan de blaaswand dik en stijf worden door littekenachtig weefsel, wat de gezondheid van de nieren en de kwaliteit van leven bedreigt. Deze studie bij ratten onthult een belangrijke moleculaire dader achter dat littekenweefsel en suggereert nieuwe manieren om de schade te vertragen of zelfs te voorkomen.
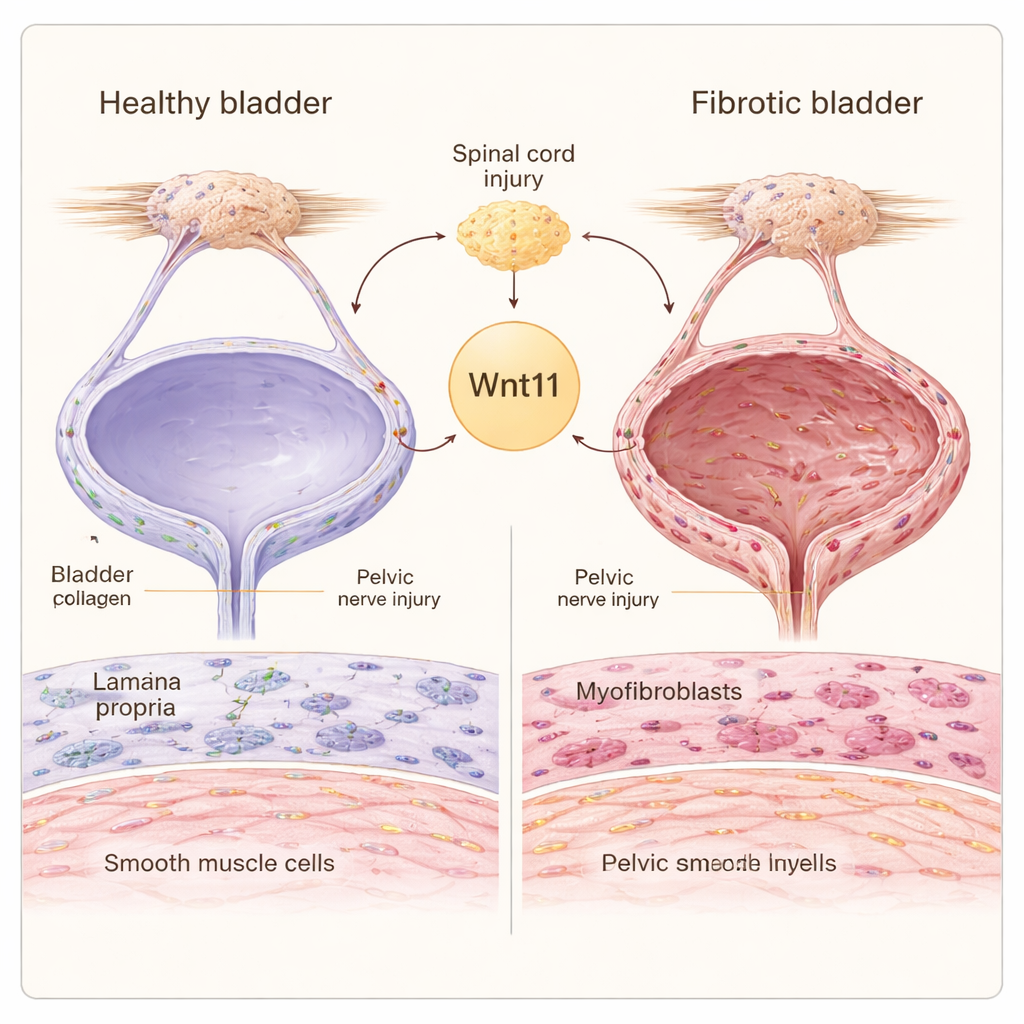
Een verborgen prijs van zenuwbeschadiging
Wanneer de zenuwen die de blaas bedienen beschadigd raken, in het ruggenmerg of nabij het bekken, moet het orgaan harder werken om urine te verwerken. De blaaswand bevat twee belangrijke ondersteunende celtypen: fibroblasten, die het steunmateriaal rond cellen maken, en gladde spiercellen, die samentrekken om urine uit te drijven. Bij neurogene blaas kunnen fibroblasten omschakelen naar zeer actieve "myofibroblasten" die overmatige collageen aanmaken, terwijl gladde spiercellen overschakelen van een slank, contractiel stadium naar een omvangrijker, meer synthetisch fenotype. Samen leggen deze veranderingen stijf littekenweefsel neer dat het vermogen van de blaas om te rekken en te legen vermindert.
Een signaalmolecuul in de schijnwerpers
De onderzoekers richtten zich op een familie van cel‑tot‑cel communicati eiwitten genaamd Wnt‑liganden, die bekendstaan om hun rol bij weefselgroei en littekenvorming in andere organen. Bij het screenen van blazen van ratten met zenuwbeschadiging vonden ze dat één lid, Wnt11, consequent en sterk verhoogd was in fibrotische blazen veroorzaakt door zowel een dwarslaesie als kneuzing van de bekkenzenuw. Wnt11‑niveaus stegen zowel in fibroblasten als in gladde spiercellen, en de hoeveelheid Wnt11 correleerde met de ernst van de blaasdisfunctie. Wanneer normale blaascellen in kweek werden blootgesteld aan een ander pro‑fibrotisch middel, TGF‑β1, verhoogden zij ook hun Wnt11‑productie, wat wijst op een versterkende lus tussen deze twee signalen.
Van chemische boodschap naar blijvend litteken
Om te testen of Wnt11 slechts toeschouwer of een actieve veroorzaker is, voegden de onderzoekers extra Wnt11‑eiwit toe aan ratten met zenuwbeschadiging en blokkeerden ze ook Wnt‑secretie met een middel genaamd LGK974. Extra Wnt11 vergrootte de blazen, verergerde drukpatronen tijdens vulling en lediging, verdikte de spierlaag en verhoogde collageenafzetting. Het blokkeren van Wnt‑secretie had het omgekeerde effect, verzachtte urineproblemen en verminderde littekenvorming. In geïsoleerde cellen duwde Wnt11 fibroblasten richting het myofibroblast‑stadium en schoof het gladde spiercellen naar het synthetische, fibrosebevorderende fenotype. Het uitschakelen van het Wnt11‑gen zelf dempte deze veranderingen, wat duidelijk maakt dat Wnt11 een centrale versnellingsmotor is van blaasremodellering.
Hoe cellen het fibrose‑signaal decoderen
Dieper gravend bracht de studie het pad in kaart van Wnt11 aan het celoppervlak tot genveranderingen in de kern. Wnt11 bleek te binden aan een receptor genaamd Vangl2 op blaasfibroblasten en gladde spiercellen. Deze interactie gebruikte niet de klassieke Wnt‑route met het eiwit β‑catenine; in plaats daarvan activeerde ze een andere keten die het planar cell polarity (PCP)‑pad wordt genoemd. Hier rekruteren Wnt11 en Vangl2 een adaptorproteïne genaamd DVL2, die vervolgens het enzym JNK inschakelt. JNK activeert op zijn beurt de transcriptiefactoren c‑JUN en NFAT5, die naar de kern verplaatsen en helpen pro‑fibrotische genen aan te zetten. Het TGF‑β1‑pad, een bekende bestuurder van littekenvorming, kwam fysiek en functioneel samen met deze Wnt11–Vangl2–JNK‑route, zodat de twee signalen elkaar versterken zowel aan het celmembraan als in de kern.
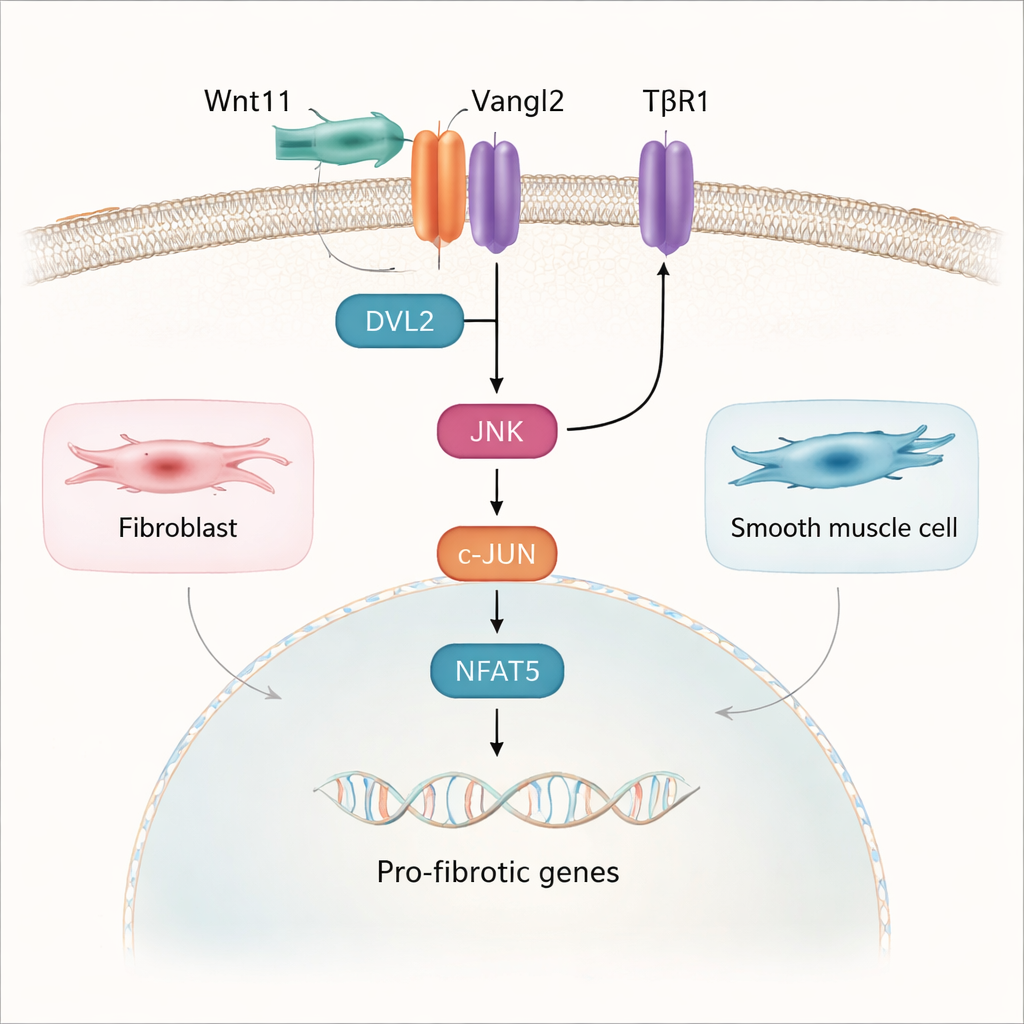
Op weg naar soepelere, gezondere blazen
Aangezien Wnt11 en TGF‑β1 samenwerken om de blaas te verharden, testte het team geneesmiddelen die sleutelstappen in beide paden blokkeren. Bij ratten met een neurogene blaas gaf gecombineerde remming van de TGF‑β‑receptor TβR1 en het enzym JNK de beste resultaten: kleinere blazen, dunnere spierwanden, minder collageen en verbeterde urineopslag en ‑lediging vergeleken met behandeling met één middel. Voor een lezer zonder specialistische achtergrond is de kernboodschap dat een specifiek door zenuwbeschadiging geïnduceerd signaal, Wnt11, helpt normale ondersteunende en spiercellen om te zetten in littekenvormende cellen. Het onderbreken van dit signaal, vooral in combinatie met klassieke TGF‑β‑remmers, zou de basis kunnen vormen voor toekomstige behandelingen die niet alleen symptomen behandelen, maar ook de structuur en functie van de blaas behouden bij mensen met een neurogene blaas.
Bronvermelding: Ge, Q., Zhang, J., Fan, Z. et al. Wnt11 mediates fibroblast–smooth muscle cell interaction to promote neurogenic bladder fibrosis in rats. Commun Biol 9, 194 (2026). https://doi.org/10.1038/s42003-026-09647-2
Trefwoorden: neurogene blaas, fibrose, Wnt11, gladde spiercellen, TGF-β-signaalverlening