Clear Sky Science · nl
Tbr2-afhankelijke parallelle routes reguleren de ontwikkeling van verschillende ipRGC-subtypen
Hoe onze ogen tijd en vorm waarnemen
Naast het vormen van beelden houden onze ogen ook geruisloos de biologische klok op schema, regelen ze de pupilwijdte en helpen ze de algemene helderheid te meten. Een kleine populatie speciale netvlieszenuwcellen, intrinsiek photosensitieve retinale ganglioncellen (ipRGC’s) genoemd, voert veel van dit werk uit. Ze reageren op licht met een pigment dat melanopsine heet en sturen signalen diep naar de hersenen. Deze studie stelt een fundamentele vraag met grote implicaties: hoe splitst één vroege groep ontwikkelende zenuwcellen zich in meerdere onderscheidende ipRGC-typen, elk met een andere taak?
Één hoofdschakelaar, veel lichtgevoelige celtypen
In het muizennetvlies ontstaan alle zes bekende ipRGC-subtypen uit een vroege populatie ganglioncellen die het gen Tbr2 inschakelen. Dit gen werkt als een hoofdschakelaar en zet programma’s aan die nodig zijn om ipRGC’s te maken en het melanopsinegen Opn4 actief te houden. Maar één hoofdschakelaar alleen verklaart niet hoe zes verschillende ipRGC-varianten ontstaan, elk met een unieke vorm, lichtrespons en hersendoelen. De auteurs gebruikten RNA-sequencing van ontwikkelende muizenretina’s om te zoeken naar genen waarvan de activiteit afhankelijk is van Tbr2. Uit een kleine set kandidaten staken twee genen bovenuit: Irx1 en Tbx20, beide bekende regulatoren van celidentiteit in andere delen van het lichaam. 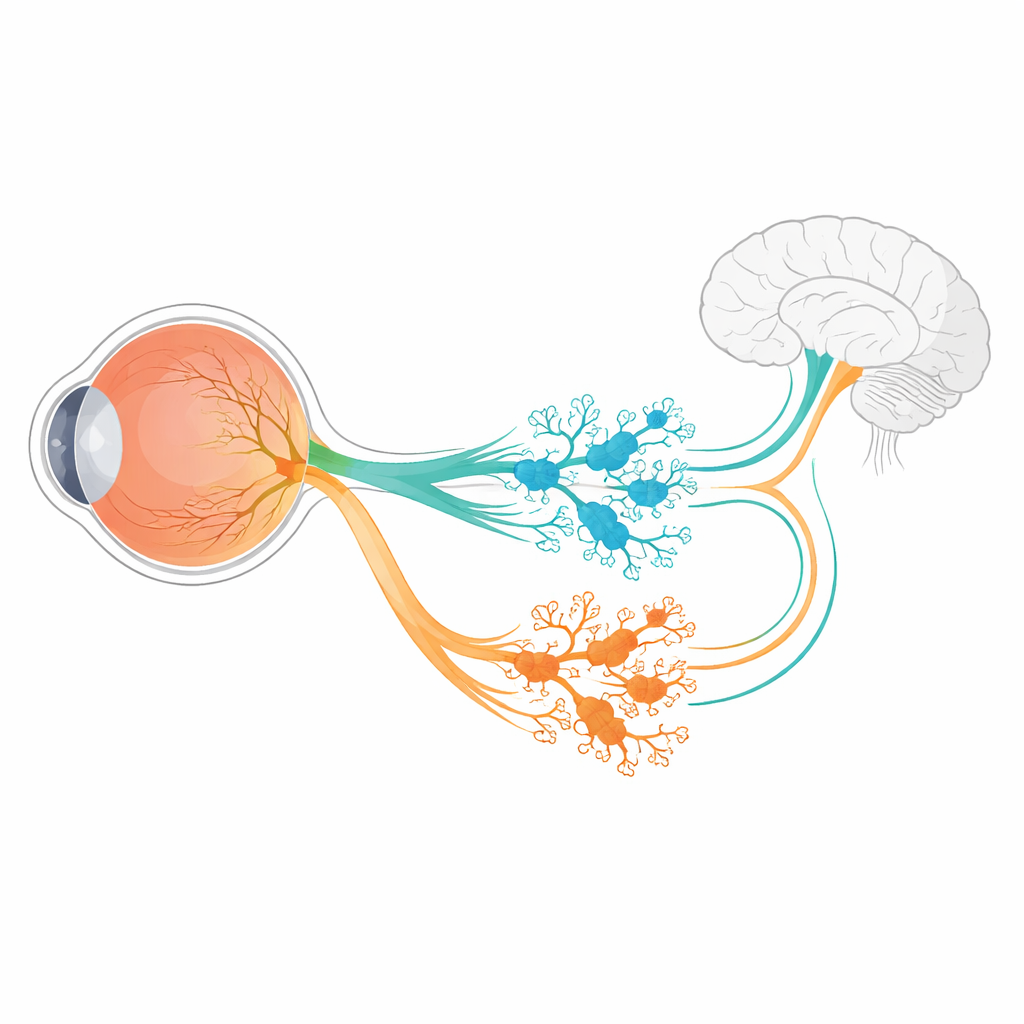
Twee vertakkende paden binnen het netvlies
Met nieuw geconstrueerde muizelijnen die Irx1- en Tbx20-producerende cellen markeren met fluorescerende of enzymatische markers, volgden de onderzoekers waar en wanneer deze factoren worden aangezet. Ze vonden dat Irx1 en Tbx20 rond de midden-embryonale periode in overlappende groepen jonge ganglioncellen verschijnen, maar snel uitvloeien naar vrijwel gescheiden sets in de volwassenheid. Irx1 komt vooral voor in drie ipRGC-typen aangeduid als M3, M4 en M5, terwijl Tbx20 geconcentreerd is in M1-, M2- en M6-cellen, met slechts kleine overlap in sommige M3- en M5-cellen. Gedetailleerde beeldvorming, elektrische opnamen en hersentracering toonden aan dat elke factor een onderscheidende verzameling ipRGC’s markeert met karakteristieke dendritische indelingen, lichtreacties en projectiepatronen naar specifieke hersengebieden die betrokken zijn bij klokinstelling, reflexen en visuele verwerking.
Schakelaars die lichtgevoeligheid en celdoverleving afstemmen
Vervolgens onderzochten ze wat er gebeurt wanneer elke factor wordt verwijderd. Toen Irx1 in het ontwikkelende netvlies werd uitgeschakeld, bleven aantal en basisstructuur van Irx1-gemarkeerde ipRGC’s grotendeels intact, maar daalden hun melanopsineniveaus scherp. Met andere woorden, Irx1 bleek essentieel om het Opn4-lichtsensitieve programma volledig aan te zetten in M3-, M4- en M5-cellen, maar niet om die cellen in eerste instantie te vormen. Tbx20 gedroeg zich anders. Het verwijderen van Tbx20 verlaagde niet alleen de Opn4-expressie, maar halveerden ook ruwweg het aantal Tbx20-positieve ipRGC’s en verminderde later de overleving van deze cellen. Dit wijst erop dat Tbx20 helpt bij zowel het opbouwen als het onderhouden van bepaalde ipRGC-subtypen, vooral M1, M2 en M6, en tegelijkertijd hun melanopsine-gebaseerde lichtgevoeligheid ondersteunt. 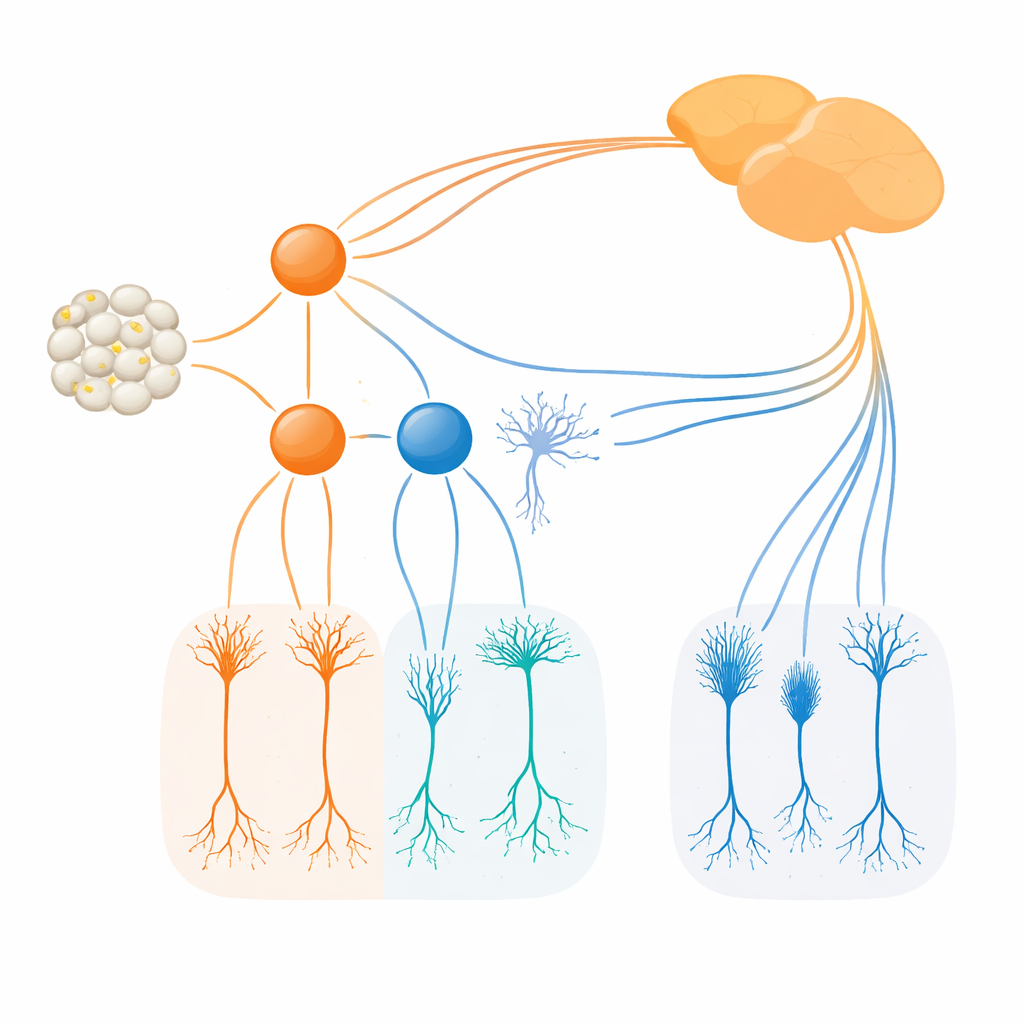
De timing van de splitsing in verschillende celgroepen
Door genetische reporters gedurende korte perioden op nauwkeurige embryonale dagen te activeren, konden de auteurs cellen die Irx1 of Tbx20 tot expressie brachten ‘timestampen’ en hun lot volgen tot in de volwassenheid. Deze experimenten toonden aan dat Tbx20-gemarkeerde cellen zich iets eerder aan hun uiteindelijke ipRGC-identiteiten binden dan Irx1-gemarkeerde cellen, waarbij de meeste beslissingen net voor de geboorte vastliggen. Tijdens een korte periode kunnen zowel Irx1 als Tbx20 in sommige cellen samen tot expressie komen, en dubbele knockout-muizen die beide genen missen, vertoonden een veel sterkere afname van melanopsine-positieve ipRGC’s dan elk enkel mutant. Dit suggereert dat de twee paden tijdelijk samenwerken en daarna uiteenlopen om verschillende subsets ipRGC’s langs afzonderlijke ontwikkelingsroutes te leiden.
Wat dit betekent voor begrip van visie en gezondheid
Voor niet-specialisten is de belangrijkste boodschap dat één vroeg gen, Tbr2, niet alleen werkt. In plaats daarvan stroomt het in twee parallelle controlepaden, één gecentreerd rond Irx1 en de ander rond Tbx20. Deze paden bepalen welk type ipRGC een jonge cel zal worden, stemmen af hoe sterk deze licht waarneemt en bepalen of hij verbinding maakt met hersengebieden voor lichaamklokregulatie, pupilreflexen of andere visuele rollen. Het werk biedt een helderder bedradingsschema voor hoe onze interne “lichtmeters” zijn opgebouwd en belicht specifieke genetische stappen die betrokken kunnen zijn wanneer deze cellen verloren gaan of niet goed functioneren, met mogelijke relevantie voor slaapstoornissen, seizoensgebonden stemmingsveranderingen en ziektes die het netvlies beschadigen.
Bronvermelding: Kiyama, T., Chen, CK., Altay, H.Y. et al. Tbr2-dependent parallel pathways regulate the development of distinct ipRGC subtypes. Commun Biol 9, 347 (2026). https://doi.org/10.1038/s42003-026-09645-4
Trefwoorden: retinale ganglioncellen, melanopsine, neurale ontwikkeling, circadiane ritmes, transcriptiefactoren