Clear Sky Science · nl
Structurele analyse toont aan dat watermoleculen zelf‑activatie van GPR99 mede mogelijk maken
Waarom deze receptor belangrijk is voor ontsteking
Onze luchtwegen en andere weefsels signaleren voortdurend chemische aanwijzingen die op infectie of irritatie wijzen. Een van die sensoren, een eiwit genaamd GPR99 dat in celmembranen zit, vormt zich tot een belangrijke schakelaar bij ontstekingsziekten zoals astma en neuskassen. Deze studie verklaart, tot op atomaire nauwkeurigheid, hoe GPR99 zichzelf kan inschakelen zonder een externe chemische trigger — en hoe kleine clusters watermoleculen daarbij helpen — wat aanknopingspunten biedt voor het ontwerpen van nieuwe ontstekingsremmende medicijnen.
Een ingebouwde aan‑schakelaar in een celsensor
GPR99 behoort tot een grote familie van membraaneiwitten die berichten van buiten naar binnen de cel doorgeven, vaak door van vorm te veranderen en partner‑eiwitten, zogenaamde G‑eiwitten, te rekruteren. In tegenstelling tot de meeste van deze receptoren is GPR99 ongewoon actief, zelfs wanneer er geen signaalmolecuul gebonden is. De auteurs tonen aan dat een flexibele lus aan de buitenzijde van GPR99, bekend als de tweede extracellulaire lus, fungeert als een interne sleutel: zij vouwt zich in de gebruikelijke bindplaats, bootst een activerend signaal na en schakelt de receptor zo zelfstandig in.
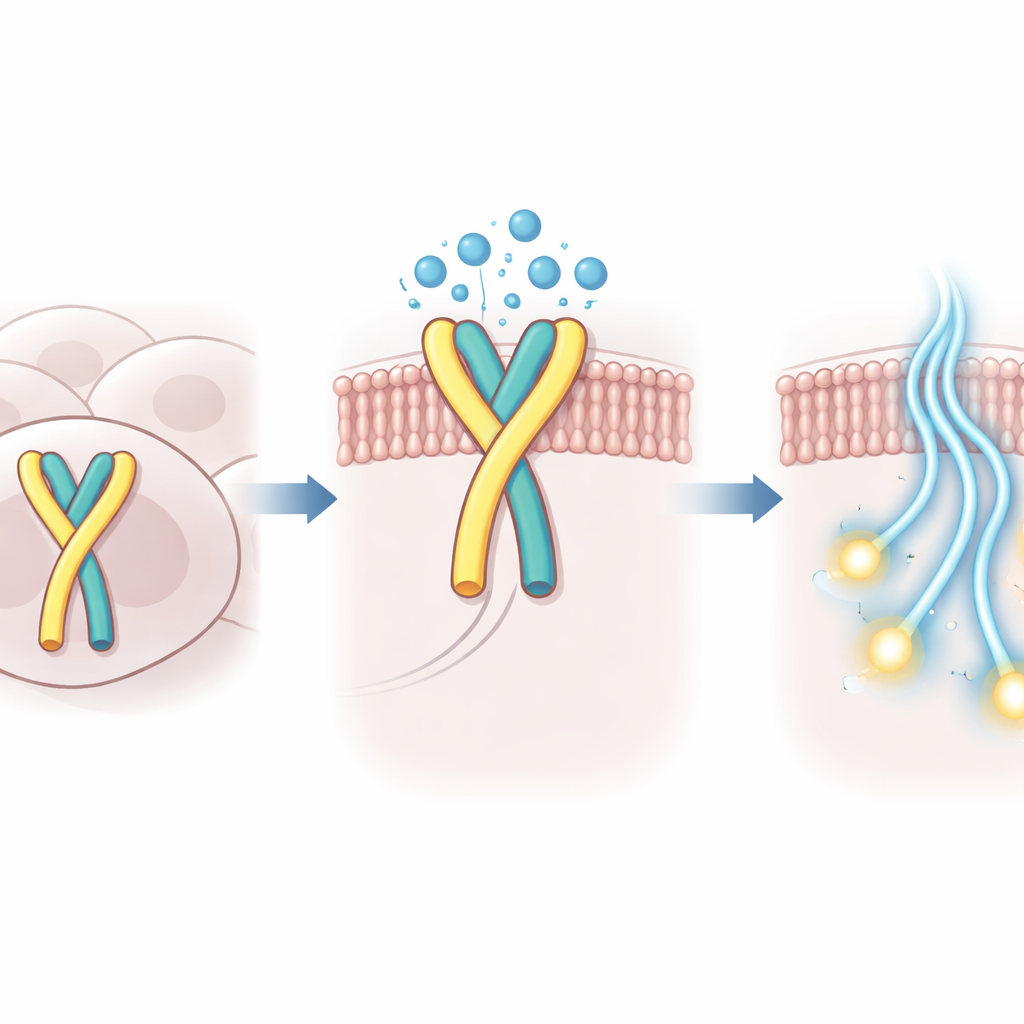
Hoe water helpt om de schakel vast te houden
Met behulp van cryo‑elektronmicroscopie met hoge resolutie brachten de onderzoekers de driedimensionale structuur in kaart van menselijk GPR99 gebonden aan zijn G‑eiwitpartner in deze zelf‑geactiveerde staat. In de bindingsholte waar normaal externe moleculen zitten, zagen ze niet alleen de ingestopte lus maar ook een kleine cluster geordende watermoleculen. Deze watermoleculen vormen een polaire brug tussen de lus en het omringende eiwit, compenseren voor de minder diepe insluiting van de lus en stabiliseren de actieve vorm van de receptor. Wanneer sleutelaminozuren in de lus of in de aangrenzende pocket werden gewijzigd zodat deze watergemedieerde contacten verzwakten, daalde de ingebouwde activiteit van GPR99 sterk in celgebaseerde tests.
Het herschikken van het innerlijk voor constant signaleren
Het team vergeleek hun zelf‑geactiveerde structuur met andere familieleden, waaronder een nauw verwante receptor die het stofwisselingsbijproduct succinaat bindt en een actieve vorm van GPR99 gebonden aan het metaboliet 2‑oxoglutaraat. Ze ontdekten dat GPR99, in afwezigheid van enige externe ligand, al volledig gepositioneerd is in een actieve conformatie: verschillende geconserveerde “microschakelaars” binnen zijn helicale kern nemen vormen aan die normaal alleen voorkomen wanneer deze receptoren gestimuleerd worden. Kritieke posities die gewoonlijk helpen receptoren in een uit‑toestand te houden, zijn bij GPR99 vervangen of anders gericht, waardoor interne remmingen verzwakken en de open configuratie wordt bevorderd die de G‑eiwitpartner verwelkomt.
Het doorgeven van het bericht naar het celinterieur
Aan de binnenzijde van het membraan toont de structuur hoe GPR99 het Gq‑type G‑eiwit vastgrijpt dat zijn signaal doorgeeft. Een helicale staart van het G‑eiwit nestelt in een holte die is geopend door de naar buiten zwaaiende beweging van een van GPR99’s helices, en vormt een netwerk van polaire en hydrofobe contacten met de binnenlussen en staart van de receptor. Mutaties die dit interface verstoren verminderen ook de signalering, wat bevestigt dat de zelf‑activatie veroorzaakt door de buitenlus en de watercluster efficiënt gekoppeld is aan intracellulaire partners. Samen verbinden deze structurele momentopnames veranderingen aan het buitenoppervlak van de receptor met de golven van calcium‑signalering die ze binnen cellen opwekt.
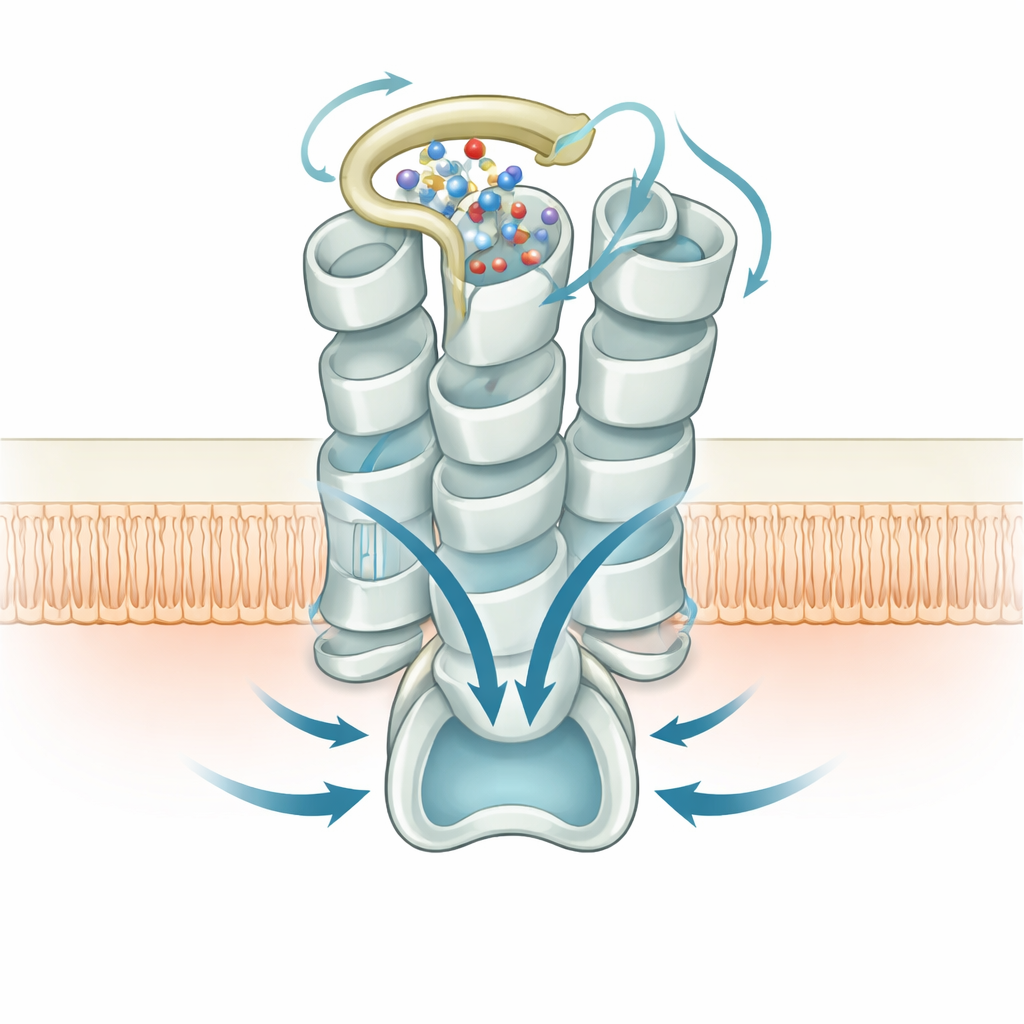
Gevolgen voor ademhaling en verder
De auteurs suggereren dat GPR99’s ingebouwde activiteit, versterkt door structurele watermoleculen, weefsels van de luchtwegen in een "stand‑by"‑modus kan houden — gereed om slijm vrij te geven en een immuunreactie op te zetten zodra ontstekingslipiden of metabole veranderingen optreden. Omdat GPR99 zeer actief is, zelfs zonder externe signalen, en omdat zijn activatie afhankelijk is van een specifieke lus‑en‑water‑opstelling, bieden deze structurele inzichten concrete doelwitten voor geneesmiddelenontwerpers. Kleine moleculen die deze interne schakel of zijn waternetwerk verstoren, zouden overmatige ontsteking kunnen dempen, terwijl verbindingen die de interactie verfijnen mogelijk GPR99’s gevoeligheid voor therapeutisch gebruik kunnen benutten.
Bronvermelding: Xiao, M., Bao, X., Guo, Y. et al. Structural analysis reveals that water molecules mediate self-activation of GPR99. Commun Biol 9, 342 (2026). https://doi.org/10.1038/s42003-026-09644-5
Trefwoorden: GPR99, GPCR‑activatie, structurele biologie, ontsteking, watergemedieerde signalering