Clear Sky Science · nl
Structureel mechanisme van anti-MHC-I-antistof dat remmende NK-celreceptoren blokkeert in tumorimmuniteit
De stilstaande kankerdoders van het lichaam ontgrendelen
Ons immuunsysteem beschikt over krachtige wachters, de natural killer (NK)-cellen, die kankercellen en door virussen geïnfecteerde cellen kunnen herkennen en vernietigen. Tumoren slagen er echter vaak in deze wachters tot zwijgen te brengen. Dit artikel onthult, op atomaire schaal, hoe een speciaal ontworpen antilichaam die “demper” kan wegnemen en NK-cellen weer kan wekken zodat ze tumoren effectiever aanvallen. Het werk combineert geavanceerde structurele biologie met muisonderzoek om te laten zien hoe één antilichaam bestaande kankerimmunotherapieën kan aanvullen.
De immuun-ID-tags op onze cellen
Elke cel in ons lichaam toont moleculaire “ID-tags” aan het oppervlak, de MHC klasse I-moleculen. Deze tags helpen immuuncellen om normaal weefsel te onderscheiden van gevaarlijke cellen die kankercelachtig zijn geworden of door virussen zijn geïnfecteerd. NK-cellen scannen voortdurend deze tags. Wanneer ze normale patronen waarnemen, geven remmende receptoren op NK-cellen een kalmerend signaal dat een aanval voorkomt. Tumoren houden deze tags vaak zichtbaar en gebruiken ze als een beschermend schild: zolang het remmende signaal aanwezig is, houden NK-cellen zich koest en kan de kanker groeien.
Een antilichaam dat het schild vastgrijpt
De onderzoekers bestudeerden een monoklonaal antilichaam genaamd B1.23.2 dat sterk bindt aan veel menselijke MHC klasse I-varianten op tumorcellen. Met cryo-elektronmicroscopie en röntgendiffractie brachten ze precies in kaart hoe dit antilichaam op het MHC-oppervlak plaatsneemt. B1.23.2 hecht zich aan een geconserveerde richel van het MHC-molecuul—een α2-helix—zonder het lichte ketenpartner te raken en waarbij het alleen zwak het gepresenteerde peptide voelt. Dit betekent dat het antilichaam een breed scala aan menselijke MHC-A-, -B- en -C-moleculen met zeer hoge affiniteit kan herkennen, terwijl het relatief ongevoelig is voor de specifieke kleine eiwitfragmenten die het MHC presenteert.
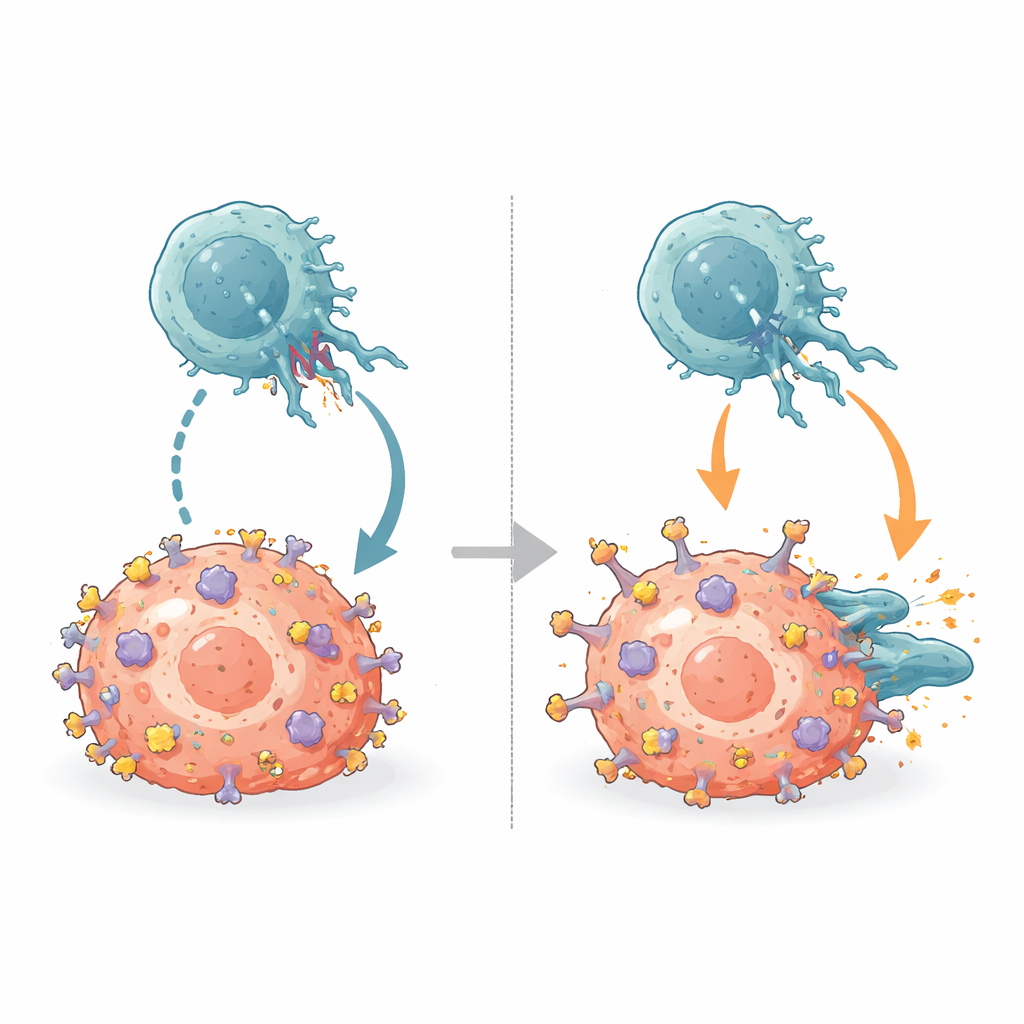
De immuunremmen voorbijstreven
NK-cellen dragen remmende receptoren genaamd KIRs die normaal gesproken docken op dezelfde α2-richel van MHC. Door de nieuwe antilichaam–MHC-structuren te vergelijken met bekende KIR–MHC-structuren, liet het team zien dat B1.23.2 fysiek het exacte stukje MHC bezet dat KIRs nodig hebben om zich vast te grijpen. Het bindingsoppervlak van het antilichaam en de KIR-voetafdrukken overlappen zo uitgebreid dat beide niet tegelijk kunnen binden. B1.23.2 bindt bovendien sterker aan MHC dan KIRs, waardoor het deze moleculaire touwtrekwedstrijd wint. Als gevolg daarvan, wanneer het antilichaam tumorcel-MHC-moleculen bedekt, kunnen KIRs op NK-cellen hun remmende signalen niet langer afgeven, wat het evenwicht verschuift naar activatie van NK-cellen.
De pasvorm verfijnen en brede dekking
Hoewel B1.23.2 vooral het geconserveerde MHC-oppervlak richt, vonden de auteurs dat kleine verschillen in het MHC-gebonden peptide subtiel de antilichaamsterkte kunnen afstemmen. Door systematisch één aminozuurpositie in het peptide te verwisselen, toonden ze bescheiden veranderingen in binding aan—meestal binnen ongeveer tienvoudig—zonder het algemene herkenningsvermogen te verliezen. Ze onderzochten ook waarom bepaalde veel voorkomende MHC-typen, zoals HLA-A*02:01, binding ontlopen. Door sleutelcontactresiduen van een reagerende MHC-variant in HLA-A*02:01 te transplantaren, maakten ze versies die het antilichaam nu wel kon herkennen, waarmee precies werd bevestigd welke posities het kritieke dockingoppervlak vormen. Deze inzichten suggereren dat toekomstige antilichaamvarianten ontworpen kunnen worden om nog meer MHC-typen te dekken of bewust andere te vermijden.
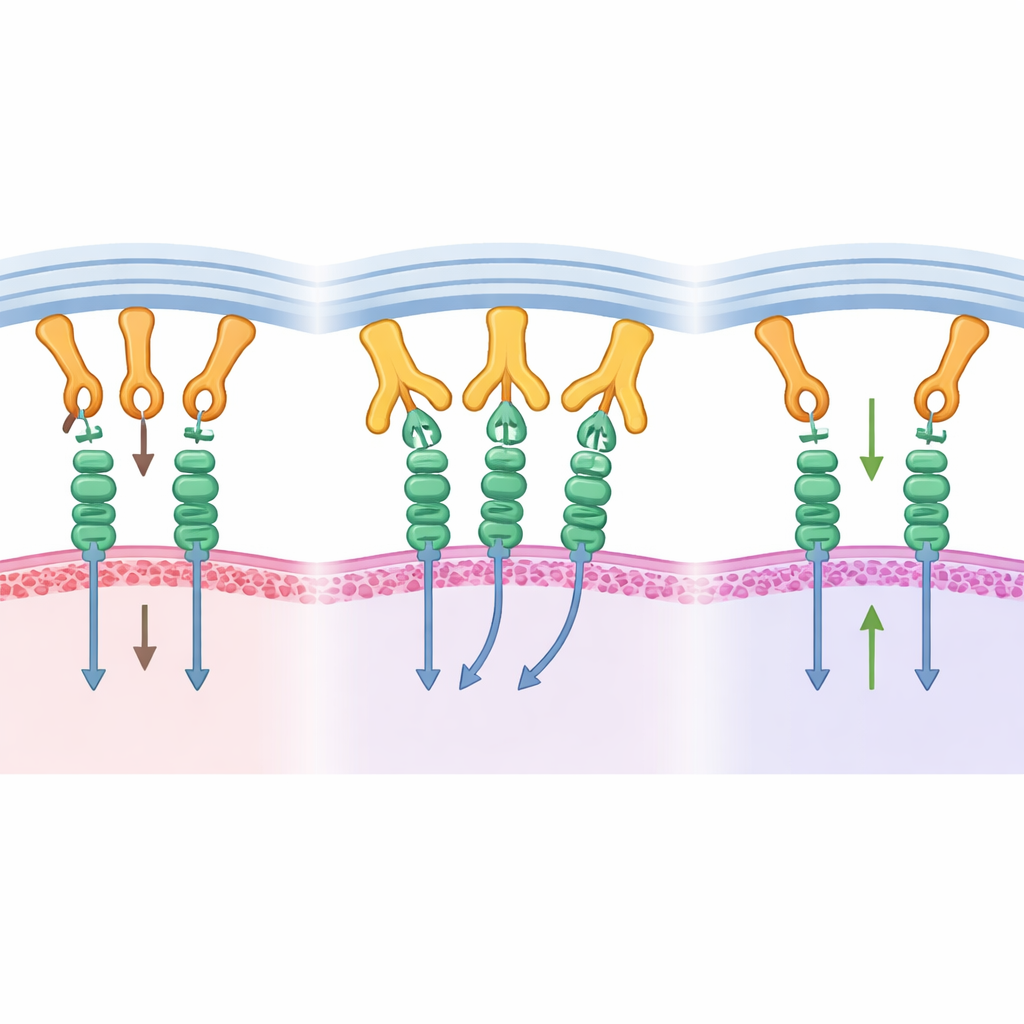
Structureel inzicht omzetten in tumorcontrole
Helpt deze moleculaire blokkade daadwerkelijk bij het bestrijden van tumoren? Om dat te testen gebruikten de onderzoekers een gehumaniseerd muismodel met een menselijke alvleesklierkanker. Ze ontwierpen een vorm van B1.23.2 die niet via zijn eigen Fc-staart kan signaleren, zodat eventuele effecten voornamelijk van het blokkeren van de MHC–KIR-interactie zouden komen. Wanneer muizen het antilichaam ontvingen samen met humane NK-cellen, groeiden tumoren veel langzamer. NK-cellen vertoonden verhoogde proliferatie, hogere activiteit van groeisen en signaalroutes, en grotere productie van ontstekingsmoleculen die geassocieerd zijn met het doden van kankercellen. Binnen de tumoren toonden NK-cellen meer activerende receptoren, wat consistent is met het vrijgekomen zijn van constante remmende input.
Wat dit kan betekenen voor toekomstige kankertherapieën
In eenvoudige termen laat deze studie zien hoe een enkel antilichaam zich tussen tumorcellen en de remmen van het immuunsysteem kan schuiven en het „val niet aan”-signaal kan stoppen dat NK-cellen normaal stilhoudt. Door de interactie op atomaire resolutie in kaart te brengen en de effecten in dieren te bevestigen, biedt het werk een blauwdruk voor een nieuwe klasse behandelingen: antilichamen die binden aan de ID-tags van de tumor in plaats van aan de immuunreceptoren zelf. Zulke middelen zouden gecombineerd kunnen worden met bestaande checkpointremmers of celtherapieën om zowel NK-cellen als T-cellen te mobiliseren, waardoor het immuunsysteem een extra aanvalshoek krijgt tegen moeilijk te behandelen kankers.
Bronvermelding: Jiang, J., Panda, A.K., Natarajan, K. et al. Structural mechanism of anti-MHC-I antibody blocking of inhibitory NK cell receptors in tumor immunity. Commun Biol 9, 350 (2026). https://doi.org/10.1038/s42003-026-09641-8
Trefwoorden: natural killer-cellen, MHC klasse I, kanker-immunotherapie, monoklonale antilichamen, remmende receptoren