Clear Sky Science · nl
LukS-PV gericht op C5aR remt EMT bij hepatoom via de BCL6/HDAC6/HSPD1-as
Een bacterieel wapen als kankerbestrijder
Hepatoom, de meest voorkomende vorm van leverkanker, is vaak dodelijk omdat het van de lever uitzaait naar andere organen. Dit artikel onderzoekt een onverwachte bondgenoot tegen die uitzaaiing: een eiwit, LukS-PV, dat oorspronkelijk deel uitmaakt van een toxine van de bacterie Staphylococcus aureus. De onderzoekers laten zien hoe dit eiwit zich kan binden aan een specifiek receptor op leverkankercellen en, in plaats van normaal weefsel te schaden, cruciale stappen uitschakelt die kankercellen in staat stellen los te komen, te reizen en nieuwe tumoren te vormen.
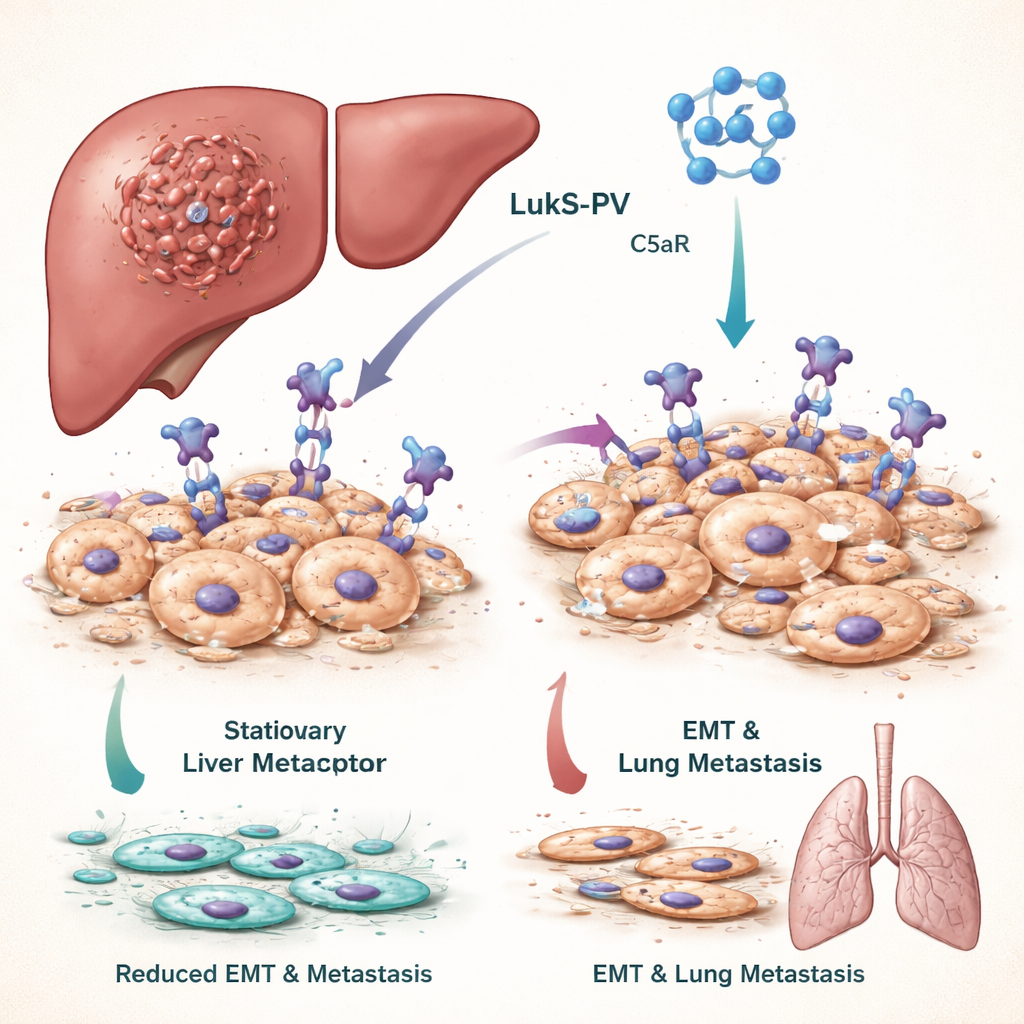
Waarom het stoppen van vormveranderende kankercellen belangrijk is
Om te kunnen uitzaaien moeten kankercellen in de lever een ingrijpende verandering in vorm en gedrag ondergaan, de zogenoemde epitheel–mesenchymale transitie (EMT). Bij EMT veranderen dicht opeengepakte cellen die normaal op hun plek blijven in flexibeler, mobielere en invasievere cellen, waardoor ze in bloedvaten kunnen binnendringen en zich in verre organen zoals de longen kunnen vestigen. Patiënten van wie de tumoren sterke EMT-activiteit vertonen hebben doorgaans slechtere vooruitzichten. Het team concentreerde zich op een signaalroute aangedreven door een molecuul genaamd C5a en diens receptor C5aR, die op veel kankercellen ongewoon veel aanwezig is en bekendstaat als bevorderlijk voor EMT en metastase.
Een toxinecomponent die een kankersignaal target
Panton–Valentine leukocidine, een toxine van Staphylococcus aureus, bevat een component genaamd LukS-PV die van nature C5aR herkent en bindt. Eerder werk van de auteurs toonde aan dat een recombinante, niet-pore-vormende versie van LukS-PV de groei van verschillende kankers kan remmen zonder duidelijke toxiciteit in proefdieren. In deze studie behandelden ze leverkankercellijnen met LukS-PV en observeerden dat de cellen minder migrerend en minder invasief werden. Moleculaire tests toonden aan dat merkers van stationaire, well-behaved cellen toenamen, terwijl merkers van agressieve, mobiele cellen afnamen. In muizen die met leverkankercellen waren geïnjecteerd leidde behandeling met LukS-PV tot veel minder tumorknobbels in de longen, wat wijst op verminderde metastaseringscapaciteit.
Een kettingreactie in tumorcellen blokkeren
Dieper gravend ontdekten de onderzoekers een keten van controle-eiwitten binnen de kankercellen die LukS-PV verstoort. Eerst bindt LukS-PV aan C5aR op het celoppervlak en blokkeert zo effectief het pro-metastatische signaal van C5a. Deze demping van C5aR-signaalverlaging verlaagt de niveaus van een eiwit genaamd BCL6, een transcriptiefactor die normaal gesproken bepaalde genen in de kern aanzet. Een van de doelwitten van BCL6 is HDAC6, een enzym dat kleine chemische labels, acetylgroepen, van andere eiwitten verwijdert. Als BCL6 overvloedig aanwezig is, stijgen de HDAC6-niveaus en raakt de cel vatbaarder voor EMT en beweging. De interferentie van LukS-PV met C5aR vermindert BCL6, wat op zijn beurt de productie van HDAC6 terugdringt en dit pro-metastatische programma vertraagt.
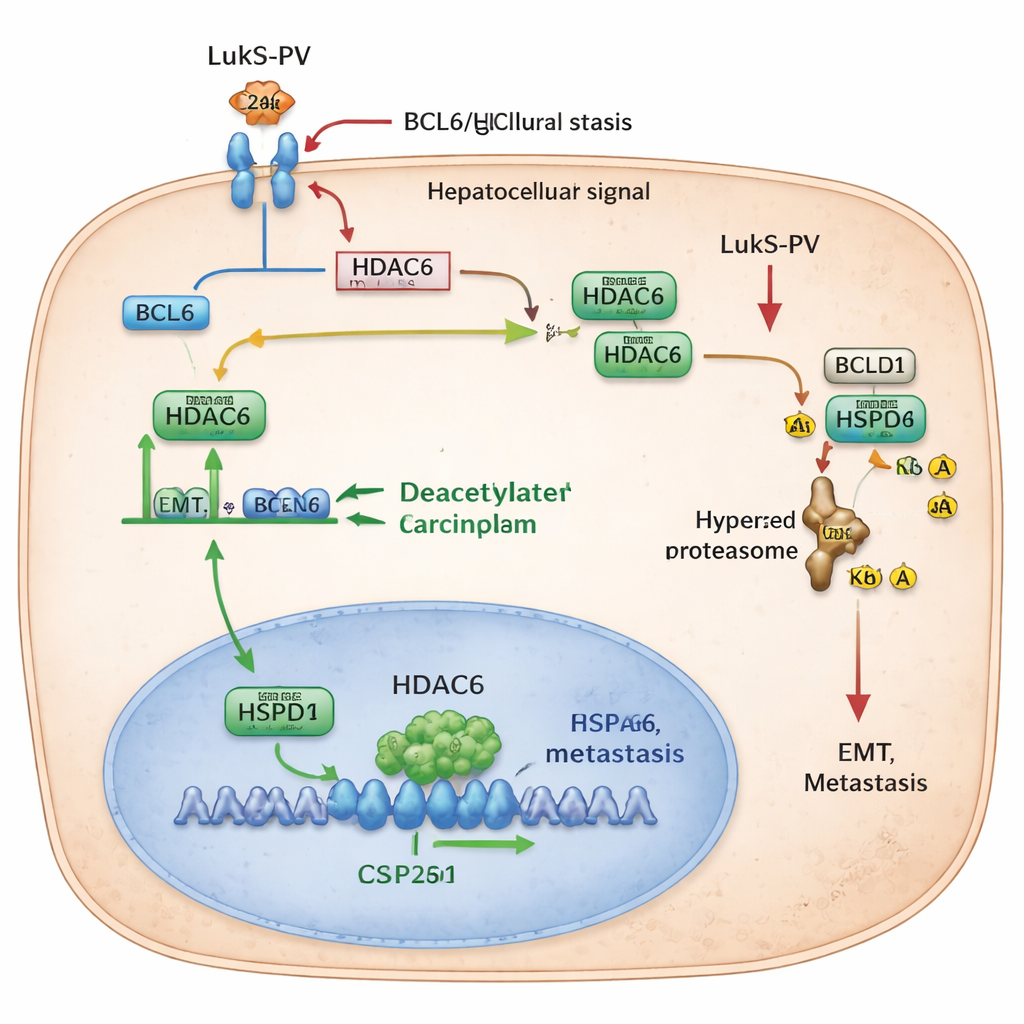
Een chaperonne bestempelen voor afbraak
Het team identificeerde vervolgens een belangrijke partner van HDAC6, HSPD1, ook bekend als HSP60, een "chaperonne"-eiwit dat andere eiwitten helpt vouwen en stabiel te blijven. In leverkanker zijn de HSPD1-niveaus hoger dan in het omliggende normale weefsel en dit wordt gekoppeld aan een slechtere overleving van patiënten. De onderzoekers ontdekten dat HDAC6 fysiek interacteert met HSPD1 en acetylgroepen van twee specifieke posities daarop verwijdert. Wanneer deze acetyllabels worden verwijderd, wordt HSPD1 stabieler en bevordert het EMT en metastase. Wanneer HDAC6 wordt verminderd—hetzij door genetische ingrepen hetzij door behandeling met LukS-PV—wordt HSPD1 meer geacetyleerd. Deze hypergeacetyleerde vorm wordt door het afvalverwerkende systeem van de cel herkend, met ubiquitine gemarkeerd en afgebroken. Naarmate HSPD1-niveaus dalen, verliezen kankercellen een deel van hun vermogen om te migreren, invaseren en de longen te koloniseren.
Van complexe routes naar een eenvoudige conclusie
Voor niet-specialisten is de kernboodschap dat de auteurs een dominoreactie binnen leverkankercellen in kaart hebben gebracht: een oppervlaktereceptor (C5aR) verhoogt een regelaar (BCL6), die een enzym (HDAC6) doet toenemen dat een chaperonne (HSPD1) beschermt tegen afbraak. Samen helpen deze factoren kankercellen van vorm te veranderen, te bewegen en uit te zaaien. LukS-PV, een bacterieel eiwit dat in het laboratorium herbestemd is, onderbreekt deze reeks direct aan het celoppervlak, wat uiteindelijk leidt tot de afbraak van HSPD1 en een rem op metastase. Hoewel dit nog experimenteel onderzoek is, suggereert het dat medicijnen gemodelleerd naar LukS-PV—of gericht op BCL6, HDAC6 of HSPD1—nieuwe manieren kunnen bieden om te voorkomen dat levertumoren uitzaaien en zo de vooruitzichten voor patiënten te verbeteren.
Bronvermelding: Ding, P., Shi, L., Xu, X. et al. LukS-PV targeting C5aR inhibits EMT in hepatocellular carcinoma via the BCL6/HDAC6/HSPD1 axis. Commun Biol 9, 314 (2026). https://doi.org/10.1038/s42003-026-09640-9
Trefwoorden: hepatocellulair carcinoom, metastase, epitheliaal mesenchymale transitie, HDAC6, bacteriële toxinetherapie