Clear Sky Science · nl
Extracellulaire matrix afgeleid van mesenchymale stamcellen voor regeneratie van bewegingsapparaatweefsel
De lichamen helpen hun eigen geraamte te herbouwen
Nu mensen langer leven en ook op hogere leeftijd actief blijven, worden verwondingen en slijtage aan botten, gewrichten, spieren en pezen een belangrijke oorzaak van pijn en invaliditeit. Dit artikel onderzoekt een nieuwe klasse van “slimme” reparatiematerialen die zijn gekweekt uit onze eigen stamcellen — speciale ondersteunende structuren genaamd mesenchymale stamcel–afgeleide extracellulaire matrix (mECM). Deze natuurlijke steigers zouden op termijn het lichaam kunnen helpen beschadigde musculoskeletale weefsels veiliger en effectiever te herstellen dan veel huidige behandelingen.
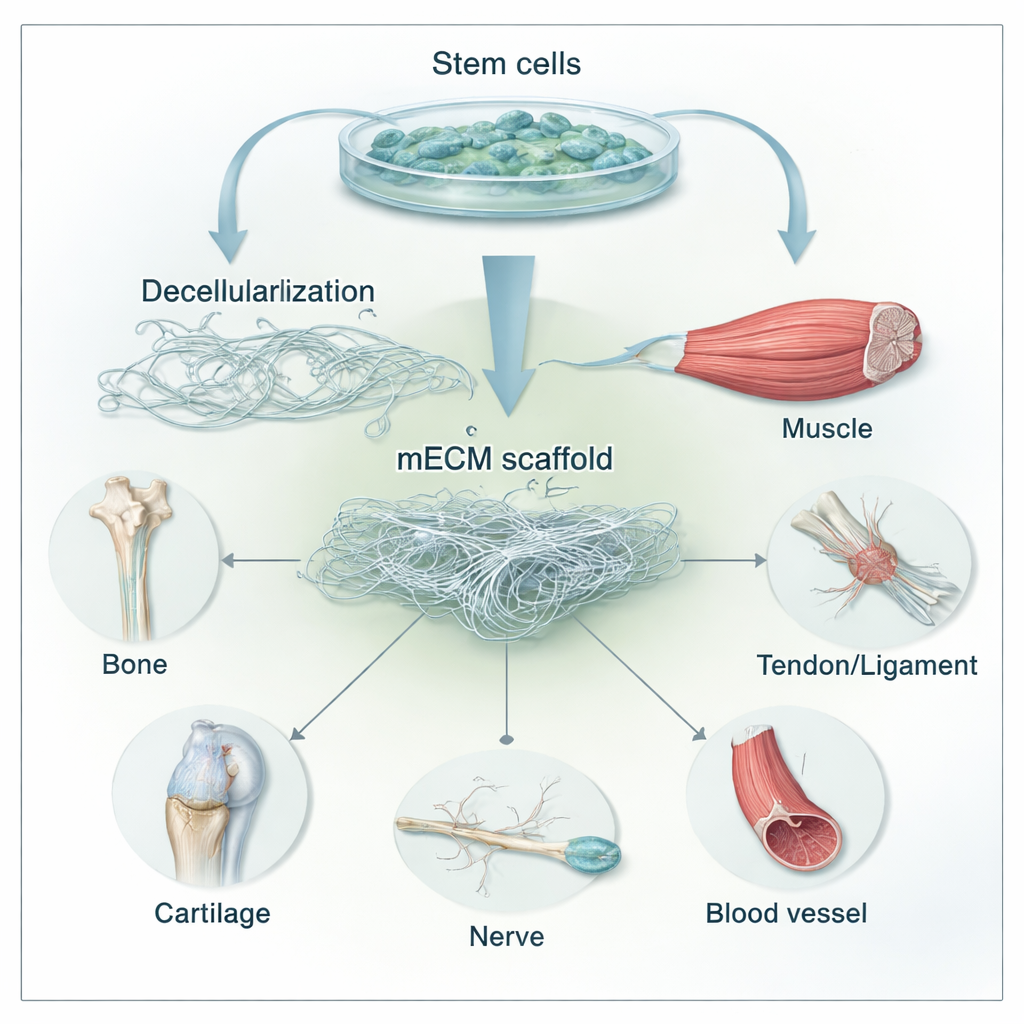
Het verborgen bouwskelet van het lichaam
Elke cel in het lichaam leeft binnen een ondersteunend netwerk dat bekendstaat als de extracellulaire matrix, of ECM. Het is niet slechts passief kleefmiddel: de vezels, poriën en gebonden moleculen geven continu signalen aan cellen over hoe ze moeten groeien, bewegen en rijpen. Bij veroudering en ziekte verstijft en rafelt deze matrix en verliest ze haar veerkracht, waardoor ons vermogen om bot en kraakbeen te herstellen direct afneemt. Wetenschappers hebben geleerd cellen uit weefsels zoals huid, darm of kraakbeen te verwijderen, zodat er “gedecellulariseerde” ECM-steigers overblijven die geïmplanteerd kunnen worden om genezing te begeleiden. Maar deze uit weefsels afkomstige materialen variëren van donor tot donor, kunnen nog immuunreacties oproepen en zijn lastig aan te passen voor verschillende patiënten of verwondingen.
Op maat gemaakt reparatiemateriaal kweken uit stamcellen
De review richt zich op ECM die niet uit hele organen komt, maar uit mesenchymale stamcellen (MSC’s), veelzijdige cellen die in beenmerg, vet, navelstreng en andere weefsels voorkomen. In het laboratorium mogen MSC’s zich verspreiden over een oppervlak en hun eigen matrix aanleggen — een delicaat driedimensionaal web van collageen, fibronectine, laminine, suikers en groeifactoren. De cellen worden daarna voorzichtig verwijderd met milde detergenten en enzymen, zodat een celvrije mECM overblijft. Omdat de ECM-moleculen sterk geconserveerd zijn tussen soorten en geen DNA of andere sterke immuunstimulerende componenten bevatten, worden deze steigers vaak goed verdragen. Belangrijk is dat onderzoekers de samenstelling en stijfheid van mECM kunnen afstemmen door de bron van de stamcellen te kiezen (bijvoorbeeld beenmerg versus vet) en door de cellen vooraf te conditioneren met verschillende signalen vóór decellularisatie.
Hoe deze levende steiger met cellen communiceert
Wanneer verse cellen opnieuw worden aangebracht op mECM, gedragen ze zich heel anders dan op vlak plastic. Studies tonen aan dat mECM de celgroei bevordert terwijl het cellen helpt “jonger” te blijven, de aanvang van cellulaire veroudering vertraagt en hun vermogen om in bot of kraakbeen te differentiëren behoudt. Jonge mECM, met zachtere mechanica en rijkere hyaluronzuurinhoud, blijkt bijzonder krachtig in het verjongen van oudere cellen. Specifieke componenten, zoals type I collageen en fibronectine, beïnvloeden of cellen veroudering weerstaan, botresorberende osteoclasten vormen of reageren op ontsteking. De matrix activeert ook interne signaalroutes die gekoppeld zijn aan levensduur en stressbestendigheid, waaronder SIRT1 en NF-κB, en kan immuuncellen kantelen naar een rustiger, weefselherstellend stadium. Kort gezegd fungeert mECM zowel als fysiek nest als biochemisch instructiehandboek voor cellen.
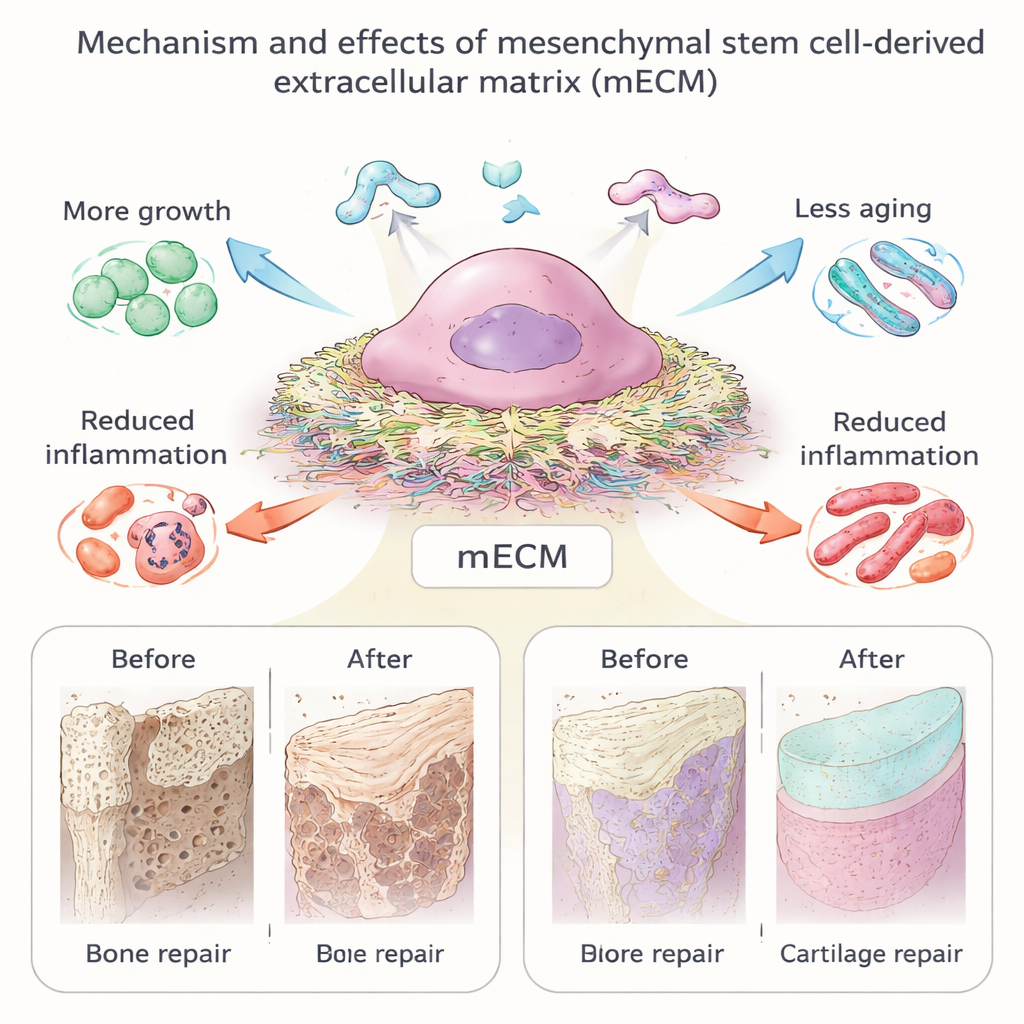
Bot, kraakbeen, spier, pees, zenuwen en bloedvaten repareren
Aangezien mECM weefsels die het moet herstellen nauw nabootst, is het in veel vormen getest: dunne vellen rond implantaten, poeders gemengd in hydrogel en microsferen, en coatings op synthetische steigers. Bij botherstel krijgen cellen die op mECM zijn gekweekt botvormend vermogen en helpen ze bij dieren sterker, beter doorbloed weefsel op te bouwen, zelfs zonder zware medicamenteuze cocktail. In kraakbeen ondersteunt mECM de vorming van glad, hyalïn-achtig kraakbeen en helpt het chondrocyten (kraakbeencellen) te voorkomen dat ze in littekenachtige toestanden afdwalen — vooral wanneer de matrix afkomstig is van jonge of vroeg-gedifferentieerde stamcellen. Vroege studies in spier en pees suggereren dat stamcel-afgeleide matrices gastheercellen kunnen aantrekken, littekenvorming verminderen en nieuwe vezels beter uitlijnen. In zenuwen en bloedvaten versnelt mECM, geïntegreerd in geleidingsbuizen of nanovezels, de hergroei van zenuwen en stimuleert het de vorming van nieuwe vaten, wat wijst op een brede regeneratieve potentie.
Van laboratoriumbank naar behandelingen in de praktijk
Ondanks bemoedigende resultaten is mECM nog niet klaar voor routinematig klinisch gebruik. Het veld mist nog gestandaardiseerde recepten om veilig cellen te verwijderen terwijl delicate matrixdetails behouden blijven, en de exacte “actieve ingrediënten” die celgedrag aansturen zijn slechts gedeeltelijk begrepen. Verschillende bronnen en leeftijden van stamcellen produceren merkbaar verschillende matrices, wat vragen oproept over welke combinaties het beste zijn voor elk type verwonding. Het opschalen van mECM-productie is kostbaar en technisch veeleisend, en wetenschappers moeten aantonen dat grote, langdurige implantaten veilig, stabiel en mechanisch sterk genoeg zijn voor dragende locaties zoals gewrichten en pezen. De auteurs betogen dat vooruitgang in proteomica, bio-informatica en biofabricage cruciaal zal zijn om deze levende steigers in kaart te brengen, te standaardiseren en te industrialiseren. Als deze obstakels overwonnen kunnen worden, zou patiëntspecifieke mECM een nieuwe gouden standaard kunnen worden voor het van binnenuit herstellen van het lichaamsskelet.
Bronvermelding: Lv, S., Wang, J., Chen, J. et al. Mesenchymal stem cell-derived extracellular matrix for musculoskeletal tissue regeneration. Commun Biol 9, 147 (2026). https://doi.org/10.1038/s42003-026-09638-3
Trefwoorden: extracellulaire matrix, mesenchymale stamcellen, bot- en kraakbeenherstel, weefseltechniek, regeneratieve geneeskunde