Clear Sky Science · nl
Periodieke geforceerde celmigratie veroorzaakt gedeeltelijk omkeerbare chromatineherschikking in kankercellijnen
Hoe opgeperste kankercellen zich herinneren dat ze onder druk stonden
Kankercellen die zich van een tumor losscheuren moeten door nauwe openingen in weefsels en bloedvaten kruipen. Om dat te doen persen ze hun zachte binnenkant — en vooral hun kern, waarin het DNA huist — door ruimtes die soms kleiner zijn dan de kern zelf. Deze studie onderzoekt wat er met de verpakking van het DNA gebeurt tijdens die herhaalde knellingen en stelt een cruciale vraag: veert de kern gewoon terug naar normaal, of houdt hij een soort “mechanisch geheugen” vast dat de verspreiding van kanker zou kunnen bevorderen?
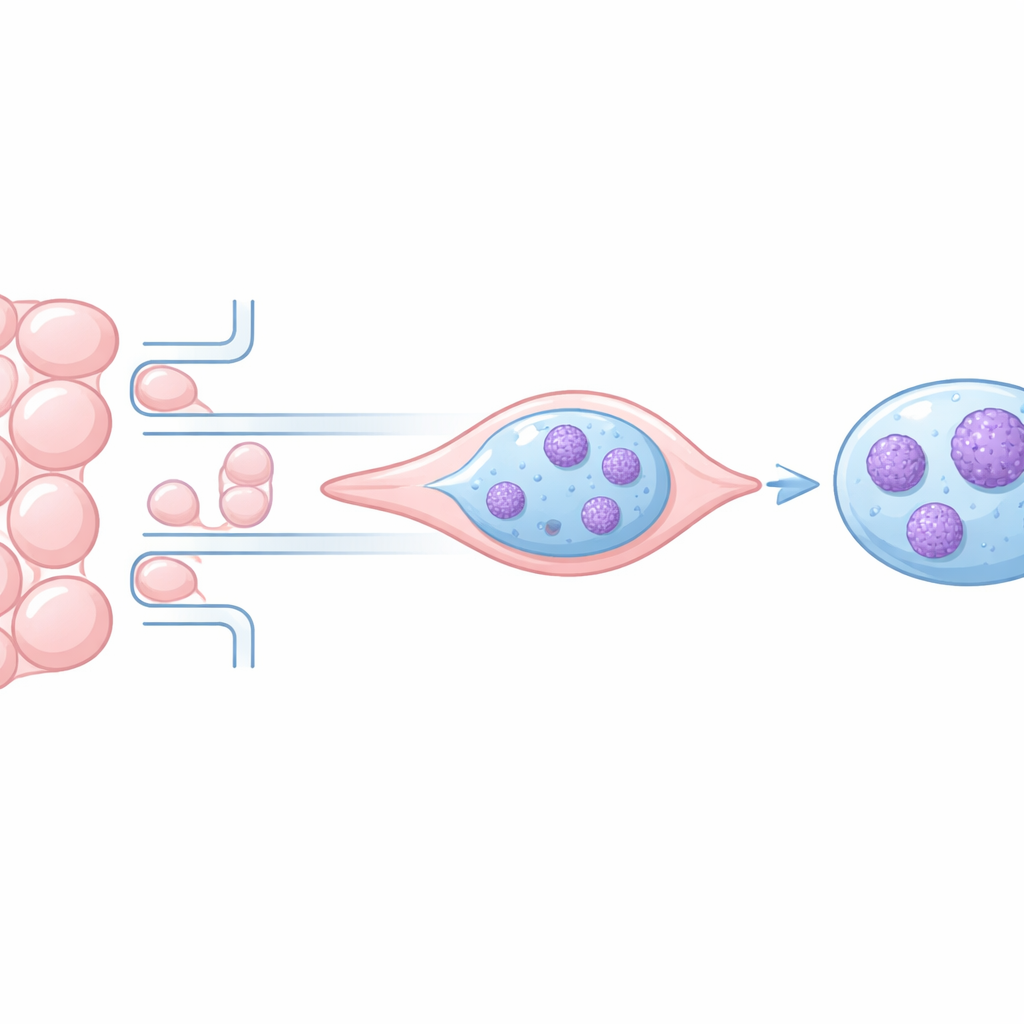
Waarom DNA-opslag ertoe doet als cellen bewegen
Binnen de kern is DNA gewikkeld rond eiwitten en gevouwen tot chromatine, die losjes of sterk gecondenseerd kan zijn. Lossere regio’s zijn vaak actief en herbergen genen die frequent gebruikt worden, terwijl sterk opgeborgen gebieden vaker stil zijn. Wanneer cellen door nauwe ruimten migreren, vervormt de kern; eerder onderzoek toonde dat dit chromatine tijdelijk kan compacteren en zelfs DNA kan beschadigen. Het was echter onduidelijk of die veranderingen volledig terugdraaiden of blijvende sporen nalieten die kunnen beïnvloeden hoe agressief kankercellen worden.
Een klein doolhof om individuele kankercellen door te persen
De onderzoekers bouwden een op maat gemaakte microfluïdische chip — een transparant apparaat met tientallen microscopische kanalen die afwisselend brede en smalle segmenten bevatten. Twee verschillende kankercellijnen, beide zo aangepast dat hun chromatine oplicht onder de microscoop, werden aangemoedigd door deze kanalen te kruipen met behulp van een chemische lokstof. Hoogresolutie-tijdopnamen maakten het team in staat elke celkern te volgen terwijl deze bewoog, de grootte van de kern te meten en heldere, sterk gecondenseerde chromatineclusters frame voor frame in meer dan 100 individuele cellen in kaart te brengen.
Wat er met de kern gebeurt onder druk
Elke keer dat een cel een nauwe vernauwing binnenkwam, kromp de projectie-oppervlakte van de kern abrupt, wat een omkeerbare afname van het nucleaire volume weerspiegelt. Tegelijkertijd steeg het aandeel van de kern ingenomen door sterk gecondenseerde chromatine — vaak twee- tot driedubbel — en daalde vervolgens terug naar het uitgangsniveau zodra de cel in een breder segment kwam. Dit patroon herhaalde zich over meerdere opeenvolgende vernauwingen en in beide kankercellijnen, wat suggereert dat de totale hoeveelheid dichte chromatine een flexibele, kortdurende reactie op mechanische stress is in plaats van een permanente verandering. Een nadere blik op de fluorescerende patronen onthulde echter dat zowel pixels met zeer hoge als zeer lage intensiteit tijdens het persen toenamen, wat duidt op een complexere interne herschikking dan een simpele uniforme compactie.
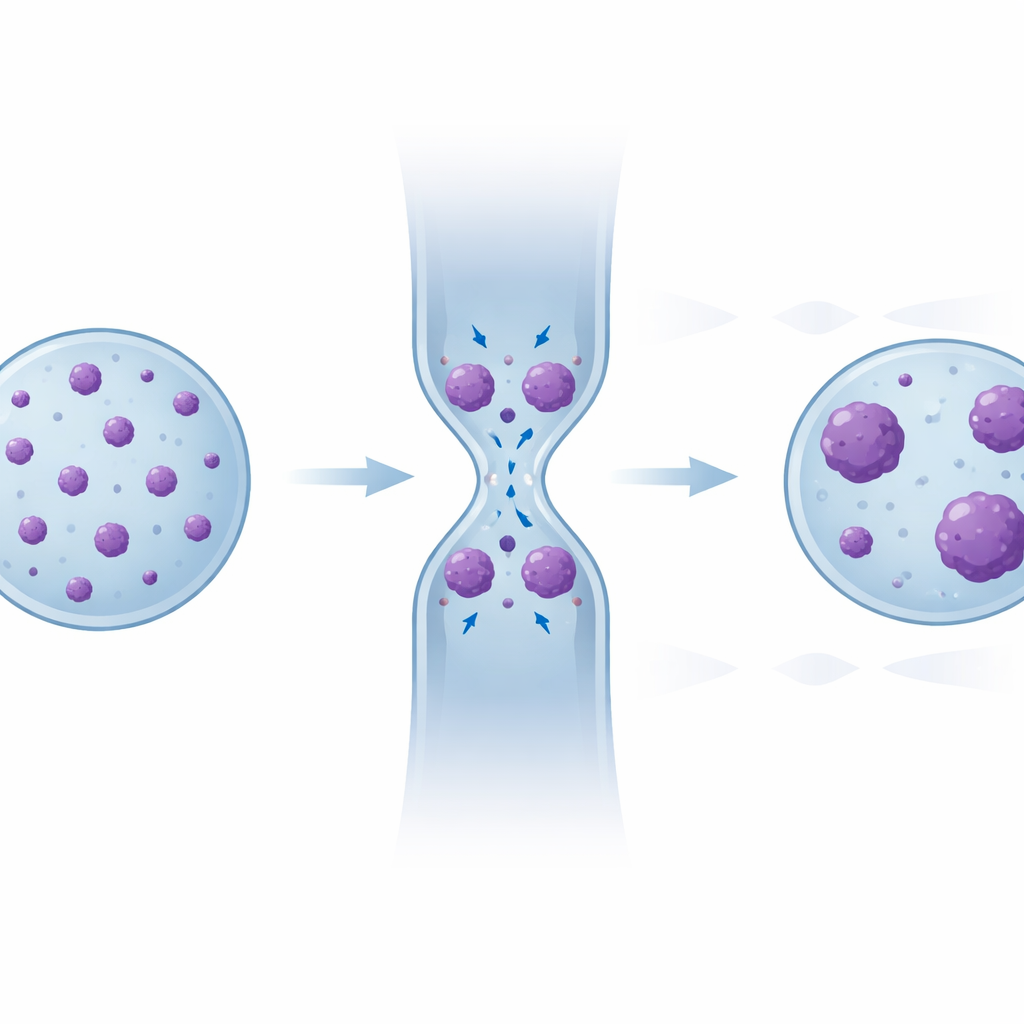
Verborgen geheugen in het patroon van DNA-clusters
Om die verborgen reorganisatie te ontdekken, onderzocht het team elke individuele gecondenseerde chromatinecluster — de grootte en het aantal clusters per kern — voor, tijdens en na de confinering. Tijdens het persen leken kleine clusters samen te vloeien tot grotere. Nadat de kern zich ontspande, keerde het totale gecondenseerde gebied terug naar het oorspronkelijke niveau, maar het patroon niet: vergeleken met de begintoestand hadden cellen die meerdere vernauwingen hadden doorgemaakt over het algemeen minder clusters, met een verschuiving naar grotere afmetingen. Statistische vergelijkingen bevestigden dat de distributies in latere “herstel”regio’s steeds meer leken op die tijdens confinering. Immunofluorescentiekleuring toonde verder aan dat veel van deze dichte regio’s overlapten met bekende “stille” chromatinemarkers, en een computermodel van chromatine als een interactief polymeer reproduceerde deze gedeeltelijke maar niet volledige ontspanning louter op basis van de fysica van plakkerige DNA-segmenten die door vervorming bij elkaar worden gebracht.
Wat dit betekent voor de verspreiding van kanker en toekomstige therapieën
In gewone bewoordingen laat de studie zien dat wanneer kankercelkernen herhaaldelijk worden geperst, hun DNA-verpakking zich gedraagt als een stressbal met een geheugen. De kern kan in omvang terugveren en de totale hoeveelheid strakke verpakking kan zich herstellen, maar het gedetailleerde patroon van dichte DNA-klompen keert niet volledig terug naar de oorspronkelijke staat. Na vele perscycli heeft de kern minder, grotere dichte regio’s, wat mogelijk verandert welke genen makkelijker of moeilijker toegankelijk zijn. Dit “mechanische geheugen” zou kankercellen kunnen helpen toekomstige vervormingen beter te verdragen tijdens het binnendringen van nieuwe weefsels. Het begrijpen en uiteindelijk targeten van deze koppeling tussen fysieke krachten en DNA-organisatie kan nieuwe manieren openen om metastase te beperken door te verstoren hoe kankercellen zich aanpassen aan mechanische stress.
Bronvermelding: Blazquez-Romero, M.d.V., Mendivil-Carboni, M., Sarasquete-Martinez, M. et al. Periodic confined cell migration drives partially reversible chromatin reorganization in cancer cell lines. Commun Biol 9, 366 (2026). https://doi.org/10.1038/s42003-026-09637-4
Trefwoorden: geforceerde celmigratie, chromatinecondensatie, nucleaire mechanica, mechanisch geheugen, kankeruitzaaiing