Clear Sky Science · nl
PTBP1 ondersteunt spermatogenese bij muizen door cytoskeletorganisatie te bevorderen via de mTORC2–PKCα-route in Sertoli-cellen
Waarom deze studie van belang is voor mannelijke vruchtbaarheid
Manlijke onvruchtbaarheid lijkt vaak ondoorgrondelijk, maar in de kern hangt het af van een goed getunede samenwerking tussen zich ontwikkelende zaadcellen en de “voedende” cellen die hen ondersteunen. Deze studie zoekt naar een van de verborgen moleculaire hulpverleners in die voedende cellen en laat zien hoe het falen daarvan de zaadcelproductie kan stilleggen. Inzicht in deze verborgen regellaag kan wijzen op nieuwe diagnostische mogelijkheden of behandelingen voor bepaalde vormen van mannelijke onvruchtbaarheid.
De ondersteunende cellen die sperma mogelijk maken
Zaadcellen worden geproduceerd in lange, gekronkelde buisjes in de testis die seminiferous tubuli heten. Deze buisjes worden bekleed door Sertoli-cellen, een gespecialiseerd type ondersteunende cel dat zich ontwikkelende kiemcellen omhult, van voeding voorziet en hen begeleidt terwijl ze delen en rijpen tot zaadcellen. Sertoli-cellen bouwen ook een beschermende wand, de bloed–testisbarrière, die vroege stadia van kiemcellen scheidt van het immuunsysteem. Om dit te doen vertrouwen ze op een intern geraamte van actinefilamenten en microtubuli dat voortdurend wordt heringericht naarmate golven van kiemcellen door de tubuli trekken. Als dit geraamte verstoord raakt, lekt de barrière en kunnen rijpende kiemcellen losraken of afsterven, wat de vruchtbaarheid bedreigt.
Een kleine RNA-manager met een grote taak
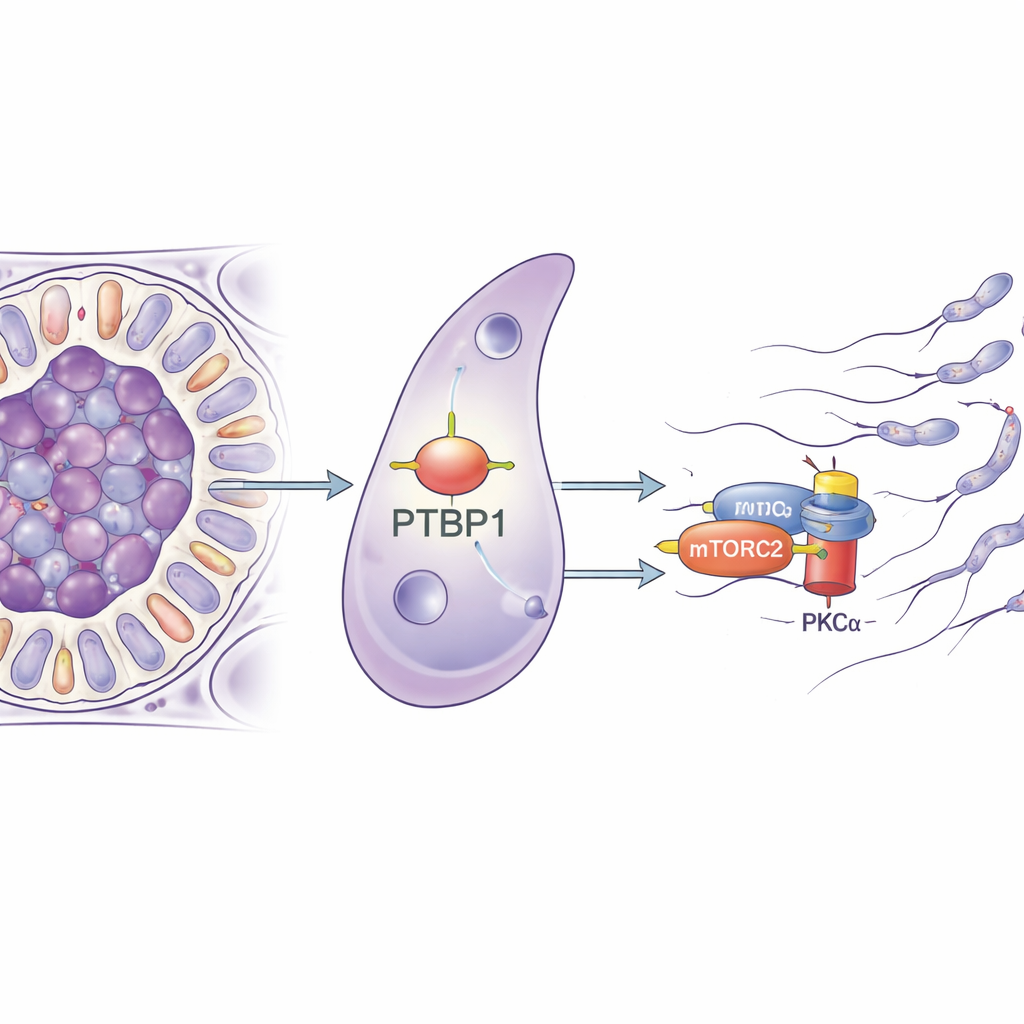
De onderzoekers concentreerden zich op een eiwit genaamd PTBP1, vooral bekend om zijn rol in het beheren van RNA-moleculen in cellen — het bepaalt hoe genen worden gespliced, hoe stabiel hun boodschappen zijn en hoe efficiënt ze in eiwit worden omgezet. PTBP1 is overvloedig aanwezig in zowel kiemcellen als Sertoli-cellen, en eerder werk toonde aan dat het verwijderen ervan uit kiemcellen de zaadproductie belemmert. In deze studie verwijderde het team PTBP1 specifiek alleen uit Sertoli-cellen bij muizen. In eerste instantie leken de jonge dieren normaal, maar toen ze de seksuele volwassenheid bereikten krimpten hun testes, daalde het aantal zaadcellen in de epididymis sterk en kon geen van de mannetjes nageslacht verwekken, wat wijst op een volledig verlies van vruchtbaarheid.
Wanneer het cellulaire geraamte instort
Microscopisch onderzoek van de testes van deze muizen liet zien dat de spermatogenese halverwege stokte. Veel tubuli bevatten lege ruimten, abnormale klonten versmolten kiemcelkernen en een tekort aan volledig verlengde zaadcellen. De kernen van Sertoli-cellen, die normaal tegen de buitenwand van de tubuli aanliggen, waren vaak naar het centrum verplaatst, wat suggereert dat deze ondersteunende cellen hun grip op de omliggende structuur verloren. Kleuring voor belangrijke junctiebestanddelen en structurele eiwitten bevestigde dat de bloed–testisbarrière verzwakt was en dat de gebruikelijke strakke bundels actinefilamenten waren vervangen door gedesorganiseerde, te intense strengen die van de basis naar het centrum van de tubulus lopen. Een tracer-molecuul dat normaal aan de ‘bloedzijde’ van de barrière blijft, lekte in plaats daarvan diep de tubuli in, wat de barrièrebeschadiging direct aantoont.
Het falen terugvoeren naar een signaleringsknooppunt
Om te begrijpen hoe een RNA-bindend eiwit zulke mechanische problemen kan veroorzaken, zuiverde het team Sertoli-cellen en analyseerde welke genen hun activiteit veranderden wanneer PTBP1 ontbrak. Veel van de aangetaste genen waren betrokken bij de regulatie van het cellulaire skelet en bij cel–cel adhesie, wat wijst op een brede herinrichtingsdefect. De onderzoekers trokken vervolgens de RNA-moleculen naar beneden die fysiek aan PTBP1 binden en vonden dat het zich hecht aan het boodschapper-RNA voor Rictor, een kernonderdeel van een signaleringscomplex genaamd mTORC2. Dit complex activeert op zijn beurt een enzym genaamd PKCα dat actinefilamenten vormgeeft. In Sertoli-cellen zonder PTBP1 daalde de hoeveelheid RICTOR-eiwit en was PKCα veel minder actief, hoewel het onderliggende Rictor-RNA nauwelijks veranderde. Dit suggereert sterk dat PTBP1 Sertoli-cellen helpt genoeg RICTOR-eiwit te maken uit zijn RNA-bericht, en zo de mTORC2–PKCα-route draaiende houdt.
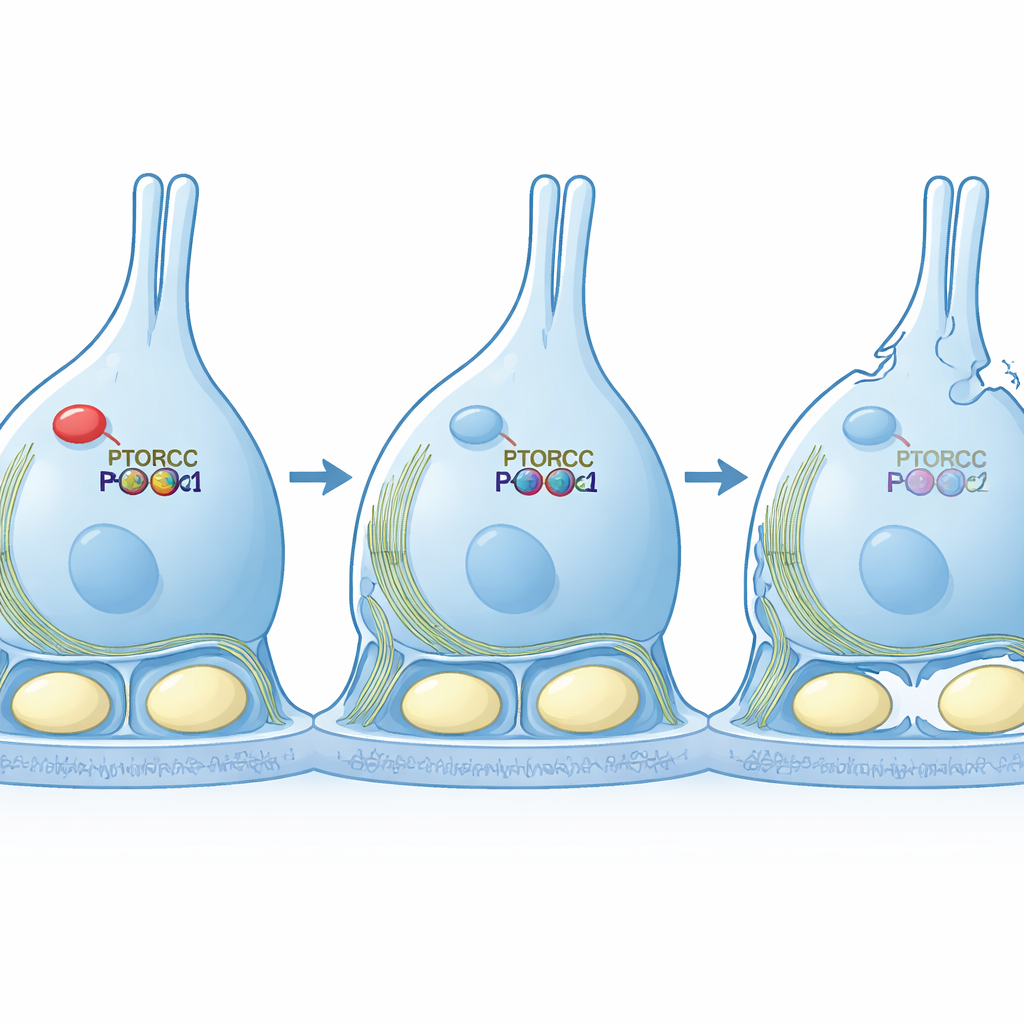
Het geraamte redden door het signaal te herstellen
Het team stapte vervolgens over naar celcultuurmodellen om causaliteit te testen. Toen ze PTBP1 verlaagden in een Sertoli-achtig cellijn, trokken de cellen uit tot lange, dunne vormen en lieten ze een verstoord actinenetwerk zien — kenmerken van verzwakte mTORC2-signalisatie. Belangrijker nog, wanneer ze deze cellen dwongen een permanent actieve versie van PKCα te produceren, herwonnen de cellen hun normale, compacte vorm en meer ordelijke actinestructuren, zelfs toen RICTOR zelf laag bleef. Dit red-experiment toont aan dat de belangrijkste taak van PTBP1 in deze context is het op peil houden van de mTORC2–PKCα-route zodat het interne geraamte van de cel georganiseerd blijft.
Wat dit betekent voor het begrip van onvruchtbaarheid
In eenvoudige bewoordingen onthult dit werk een keten van afhankelijkheid in de testis: PTBP1 helpt Sertoli-cellen een belangrijk signaleringsknooppunt te bouwen; dat knooppunt ordent hun interne skelet; en een intact skelet stelt hen in staat zich vast te houden aan en ontwikkelende zaadcellen te beschermen. Breek de keten bij PTBP1 en Sertoli-cellen verliezen hun structuur, faalt de beschermende barrière en stort de zaadontwikkeling in, wat resulteert in mannelijke onvruchtbaarheid. Hoewel dit onderzoek bij muizen is gedaan, komen dezelfde moleculen ook bij mensen voor, wat de mogelijkheid vergroot dat subtiele defecten in RNA-regulatie binnen Sertoli-cellen ten grondslag kunnen liggen aan sommige onverklaarde gevallen van mannelijke onvruchtbaarheid en een nieuwe set moleculaire doelwitten voor toekomstig onderzoek biedt.
Bronvermelding: Ozawa, M., Taguchi, J., Mori, H. et al. PTBP1 supports mouse spermatogenesis by facilitating cytoskeletal organization through the mTORC2–PKCα pathway in Sertoli cells. Commun Biol 9, 341 (2026). https://doi.org/10.1038/s42003-026-09636-5
Trefwoorden: mannelijke vruchtbaarheid, Sertoli-cellen, spermatogenese, cytoskelet, RNA-bindende eiwitten