Clear Sky Science · nl
Negatieve regulatie van het NF-κB-pad door de ubiquitine-ligase Nedd4-1(NE)
Waarom het uitschakelen van ontsteking ertoe doet
Ons immuunsysteem vertrouwt op snelle uitbarstingen van ontsteking om infecties te bestrijden en verwondingen te genezen, maar diezelfde mechanismen kunnen weefsels beschadigen en kanker bevorderen als ze te lang aanblijven. Dit artikel onderzoekt hoe humane en andere primaatcellen dat gevaar vermijden door een recent gekarakteriseerde ingebouwde "rem" die een van de centrale alarmsystemen van het lichaam tot rust brengt zodra het zijn werk heeft gedaan.
Een centraal alarmschakelaar in onze cellen
Centraal in dit verhaal staat NF-κB, een familie eiwitten die fungeert als een hoofdschakelaar voor honderden genen betrokken bij ontsteking, celdoodoverleving en immuniteit. Wanneer cellen stresssignalen waarnemen, zoals het ontstekingsmolecuul TNFα, zet een keten van gebeurtenissen NF-κB los van zijn eiwit"chaperonnes" in het cytosol en stelt het in staat naar de kern te verplaatsen, waar het pro-inflammatoire en pro-survival genen activeert. Omdat dit pad zo krachtig is, moeten cellen zowel de activering als de uitschakeling nauwkeurig afstemmen. Het niet kunnen uitzetten ervan is in verband gebracht met chronische ontstekingsziekten en veel vormen van kanker.
Een primaat-specifieke rem op het alarm
De onderzoekers richtten zich op Nedd4-1, een lid van een grote familie enzymen die andere eiwitten labelen met een klein molecuul dat ubiquitine wordt genoemd. Deze markering geeft vaak aan dat eiwitten afgebroken of verplaatst moeten worden binnen de cel, en herstructureert zo signaalnetwerken. Een eerder ontdekte splice-variant van Nedd4-1, genoemd Nedd4-1(NE), komt alleen in primaten voor en draagt een lange extra segment aan het N-uiteinde dat zijn locatie in de cel en zijn herkenningsprofiel verandert. In tegenstelling tot de standaardvorm van Nedd4-1, die via andere partners de NF‑κB-activiteit juist kan verhogen, vond het team dat Nedd4-1(NE) het tegengestelde effect heeft: het dempt NF‑κB-signalisatie, vooral na langdurige blootstelling aan TNFα.
Twee manieren om NF-κB in bedwang te houden
Om te achterhalen hoe deze rem werkt, gebruikten de auteurs proximiteitsetikettering en eiwit pull‑down-methoden om te zien welke moleculen fysiek geassocieerd zijn met Nedd4-1(NE). Ze identificeerden sleutelcomponenten van het NF‑κB-pad, waaronder de kinase IKKβ en het NF‑κB-voorlopereiwit NF‑κB1 (ook p105 genoemd). Vervolgexperimenten toonden aan dat Nedd4-1(NE) ubiquitine-tags toevoegt aan IKKβ, wat leidt tot afbraak daarvan. Met minder IKKβ is het gebruikelijke doelwit IκBα niet langer even efficiënt gefosforyleerd en vernietigd. Daardoor blijft IκBα stabieler en houdt het de actieve NF‑κB-subunit p50 vast in het cytosol, waardoor deze niet de kern kan binnengaan om ontstekingsgenen aan te zetten.
Een adaptor-gestuurde overdracht naar de rem
Nedd4-1(NE) werkt ook verder stroomafwaarts door de niveaus van NF‑κB1 zelf te beperken. Hier werkt het enzym niet alleen: het werkt samen met een ander ubiquitine-labelend eiwit genaamd KPC1. KPC1 helpt bij de verwerking van de NF‑κB1-voorloper p105 naar de actieve p50-vorm en bevindt zich in cellulaire compartimenten die late endosomen worden genoemd, waar Nedd4-1(NE) ook aanwezig is. Het team toonde aan dat Nedd4-1(NE) KPC1 kan ubiquitineren en dat dit gemodificeerde KPC1 fungeert als adaptor, die NF‑κB1 naar Nedd4-1(NE) op late endosomen recruteert. Dit drieledige complex bevordert de destabilisatie van zowel p105 als p50, waardoor opnieuw de hoeveelheid NF‑κB die de kern kan bereiken, afneemt.
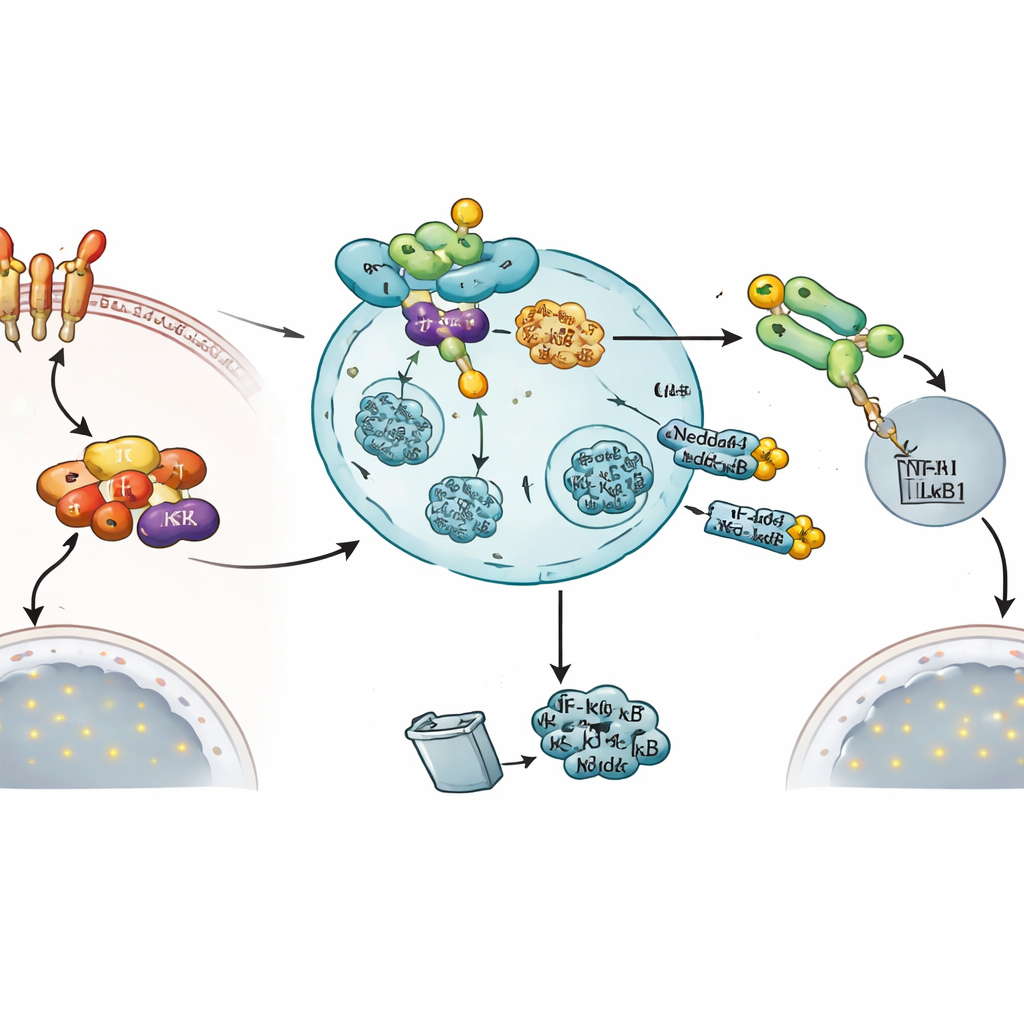
Een ingebouwde negatieve terugkoppeling om het signaal te beëindigen
Opmerkelijk is dat het signaal dat NF‑κB activeert ook deze rem lijkt te induceren. Wanneer cellen werden behandeld met TNFα, steeg het niveau van Nedd4-1(NE)-messenger RNA sterk, terwijl de standaardvorm van Nedd4-1 niet veranderde. Functionele metingen ondersteunden het idee dat Nedd4-1(NE) een uitschakelklep is: het verhogen van actief Nedd4-1(NE) verminderde de verplaatsing van NF‑κB1 naar de kern, verlaagde de activiteit van een NF‑κB-responsief rapportergen en verminderde de expressie van een door NF‑κB gereguleerd ontstekingsgen, TNFAIP3. Gezamenlijk schetsen deze bevindingen een negatieve terugkoppellus waarin de activering van het NF‑κB-pad uiteindelijk Nedd4-1(NE) opdrijft, dat vervolgens twee kritieke knooppunten—IKKβ en NF‑κB1—richt om de ontstekingsreactie af te remmen.
Wat dit betekent voor gezondheid en ziekte
Voor een algemeen publiek is de kernboodschap dat onze cellen een extra, primaat-specifiek veiligheidsmechanisme hebben ingebouwd om te voorkomen dat ontstekingssignalen uit de hand lopen. Door selectief kerncomponenten van het NF‑κB-systeem te labelen en te verlagen, helpt Nedd4-1(NE) de reactie op TNFα te beëindigen en kan het bijdragen aan langdurige immuunevenwichtigheid. Inzicht in deze ingebouwde rem zou nieuwe wegen kunnen openen voor de behandeling van ziekten waarbij NF‑κB chronisch overactief is, zoals auto-immuunziekten en bepaalde kankers, door manieren te suggereren om dit natuurlijke uitschakelproces te imiteren of te versterken.
Bronvermelding: Persaud, A., Kefalas, G., Shteiman, A. et al. Negative regulation of the NF-κB pathway by the ubiquitin ligase Nedd4-1(NE). Commun Biol 9, 374 (2026). https://doi.org/10.1038/s42003-026-09634-7
Trefwoorden: NF-kB signalering, ontsteking, ubiquitine-ligase, Nedd4-1(NE), TNF alfa