Clear Sky Science · nl
Notch3 reguleert de fenotypische plasticiteit van pericyten bij colorectale kanker
Waarom de bloedvaten rond tumoren ertoe doen
Colorectale kanker is een van de meest voorkomende en dodelijke vormen van kanker wereldwijd, maar de meeste therapieën richten zich rechtstreeks op kankercellen en negeren vaak het omliggende ondersteunende systeem dat tumorgroei faciliteert. Dit artikel richt zich op een minder bekende groep ondersteunende cellen, pericyten, die zich om kleine bloedvaatjes heen wikkelen. Door te onthullen hoe een signaalwisselaar genaamd Notch3 het gedrag van pericyten verandert, tonen de auteurs aan hoe de bloedtoevoer van de tumor kan worden geduwd richting lekkende, chaotische vaten die de kanker bevoordelen, of juist naar meer normale vaten die de ziekte kunnen vertragen en de behandeling kunnen verbeteren. 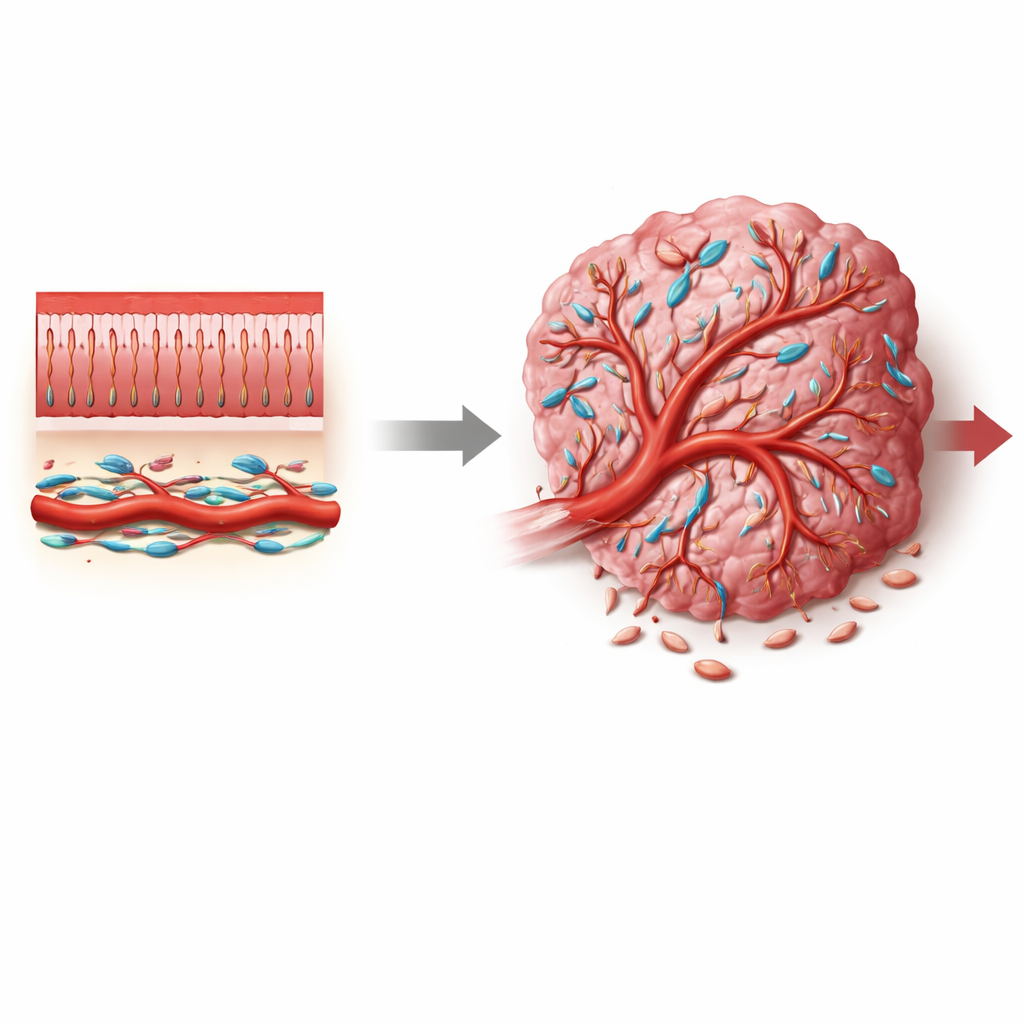
De verborgen helpers rond tumorvaten
Bloedvaten zijn meer dan alleen holle buisjes. In gezonde weefsels worden kleine vaten stevig omarmd door pericyten—gespecialiseerde cellen die vaatwanden stabiliseren, de bloedstroom regelen en lekkage beperken. In tumoren zien deze pericyten er echter vaak anders uit en gedragen ze zich anders: ze kunnen losraken, zich vermenigvuldigen of hun identiteit veranderen, wat bijdraagt aan de abnormale, lekkende vasculatuur die kenmerkend is voor kanker. In colorectale tumoren, waar de micro-omgeving vol zit met fibroblasten, immuuncellen en vaatcellen, was het onduidelijk waar tumor-geassocieerde pericyten vandaan komen, welke toestanden ze aannemen en welke moleculaire signalen hen richting tumortegundragende rollen duwen.
Pericyten volgen terwijl tumoren ontstaan
Om pericyten in de tijd te volgen gebruikten de onderzoekers muismodellen van colitis-geassocieerde colorectale kanker waarin ze bepaalde celtypes genetisch konden “labelen” en hun lot konden observeren. Ze toonden aan dat de pericyten die in tumoren worden aangetroffen grotendeels voortkomen uit normale, weefsels-residente pericyten die zich uitbreiden en prolifereren naarmate de kanker zich ontwikkelt, in plaats van van verre bronnen zoals het beenmerg te komen. Met geavanceerde single-cell RNA-sequencing brachten ze tienduizenden stroma-cellen uit muizen tumoren en normaal colon in kaart en vonden ze dat pericyten significant verrijkt zijn in de tumor-micro-omgeving. Ze identificeerden ook vergelijkbare pericyt-uitbreiding in meerdere menselijke colorectale-kanker datasets, wat benadrukt dat dit geen puur muizenspecifiek verschijnsel is.
Een moleculaire schakelaar die pericytgedrag verandert
Het team vroeg vervolgens welke signalen het gedrag van pericyten in tumoren bepalen en ontdekte dat Notch3—een receptor die cellen in staat stelt met hun buren te communiceren—bijzonder actief is in tumorpericyten. Computationele analyse van celschikking en -communicatie suggereerde dat pericyten zowel Notch-gerelateerde signalen zenden als ontvangen, vooral via partners op vaatcellen. Door Notch3 kunstmatig aan te zetten in pericyten zagen de onderzoekers dat deze cellen meer gingen prolifereren maar minder contractiele eiwitten uitdrukten die normaal geassocieerd zijn met vaatstabiliserend gedrag. De tumorbloedvaten in deze muizen werden groter, lekkender en bekleed met meer delende endotheelcellen, wat wijst op minder stabiele vasculatuur. Omgekeerd reduceerde verwijdering van Notch3 de proliferatie van endotheelcellen, verkleinde de vatdiameter en verminderde lekkage, wat een verschuiving naar meer genormaliseerde bloedvaten suggereert zonder de vroege tumoraantallen of -grootte drastisch te veranderen. 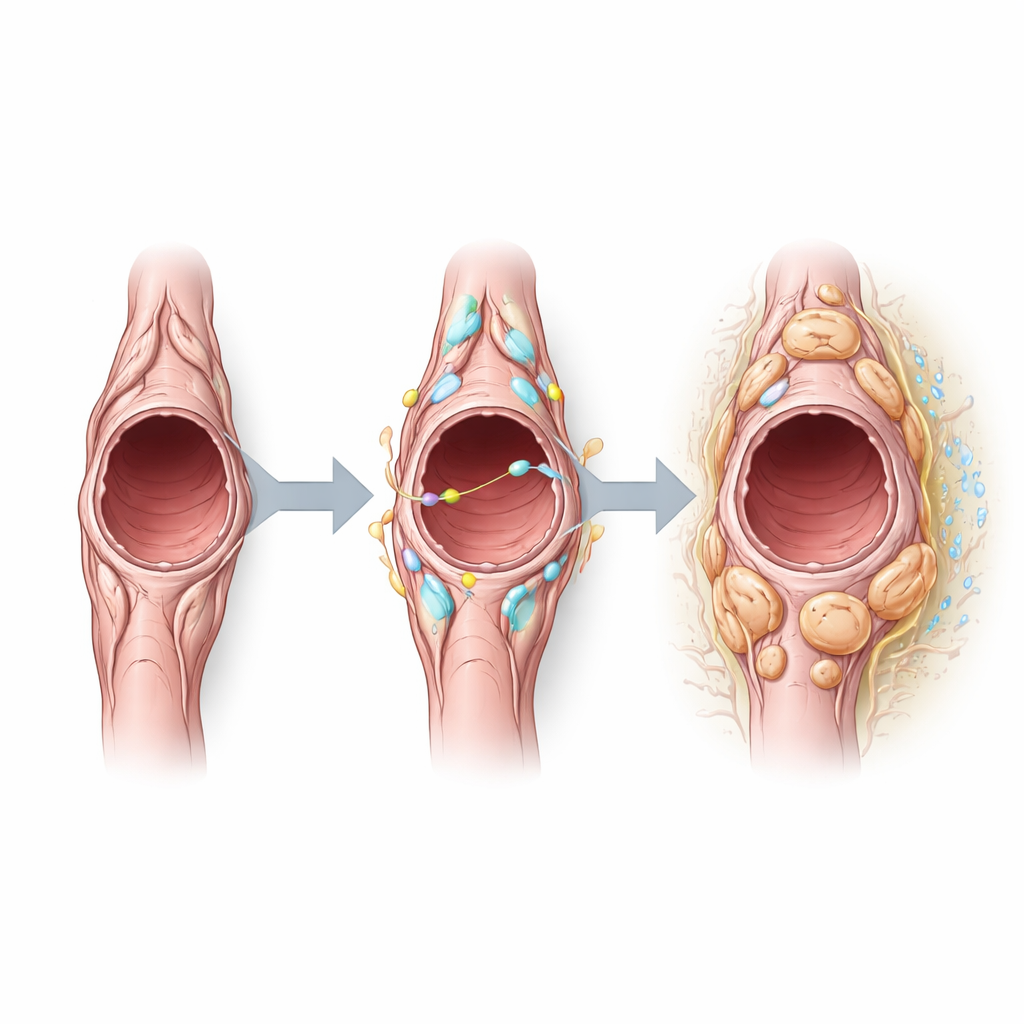
De vele gezichten van pericyten in tumoren
Buiten eenvoudige aan/uit-veranderingen toonde de studie aan dat tumorpericyten in meerdere uiteenlopende toestanden bestaan. Sommige subgroepen vertoonden kenmerken van sterk contractiele cellen, anderen produceerden grote hoeveelheden extracellulaire matrix, sommige toonden inflammatoire eigenschappen en een subset droeg zelfs signaturen die gewoonlijk in endotheelcellen worden gezien. Notch3-activiteit was niet gelijk verdeeld: ze was verrijkt in een “synthetische” of matrix-producerende pericytenpopulatie en laag in de meer contractiele subset. Trajectanalyse suggereerde dat pericyten kunnen verschuiven van een contractiele toestand naar een synthetische, proliferatieve toestand naarmate Notch3-activiteit toeneemt. Bij onderzoek van menselijke colorectale-kanker data vonden de auteurs een vergelijkbaar spectrum aan pericyt-toestanden en zagen ze opnieuw hogere activiteit van een Notch3-doelgen in tumor-geassocieerde en prolifererende pericyten, wat de muisresultaten weerspiegelt.
Van vat-chaos naar therapeutische kansen
Al met al schetst het werk Notch3 als een sleutelknop die de identiteit van pericyten afstemt en daarmee de structuur en functie van tumorbloedvaten beïnvloedt. Hoge Notch3-activiteit duwt pericyten naar een proliferatieve, minder contractiele toestand die geassocieerd is met vergrote, lekkende vaten die tumorgroei bevorderen. Lage Notch3-activiteit hangt samen met meer contractiele pericyten, rustiger endotheelcellen en meer genormaliseerde vasculatuur die de tumorgroei kan remmen en de medicijnafgifte kan verbeteren. Door specifiek Notch3 in pericyten te targeten, zouden toekomstige therapieën tumorvaten weg kunnen sturen van chaos en richting stabiliteit, wat een nieuw invalshoek biedt om gevorderde colorectale kanker in combinatie met bestaande middelen te behandelen.
Bronvermelding: Chalkidi, N., Stavropoulou, A., Arvaniti, VZ. et al. Notch3 regulates pericyte phenotypic plasticity in colorectal cancer. Commun Biol 9, 343 (2026). https://doi.org/10.1038/s42003-026-09629-4
Trefwoorden: colorectale kanker, tumormicro-omgeving, pericyten, Notch3-signaaltransductie, tumorbloedvaten