Clear Sky Science · nl
Endotheliale TRIM47 reguleert de integriteit van de bloed‑hersenbarrière en cognitie via de KEAP1/NRF2‑signaleringsweg bij muizen
Waarom het beschermen van de kleine bloedvaten in de hersenen belangrijk is
Cerebrale kleinevatenziekte is een stille boosdoener in de hersenen. Ze beschadigt de allerkleinste bloedvaten, vergroot het risico op een beroerte en knaagt langzaam aan geheugen en denkvermogen, terwijl artsen nog steeds effectieve behandelingen missen die de onderliggende biologische oorzaken aanpakken. Deze studie onderzoekt één specifiek eiwit, TRIM47, dat voorkomt in de cellen die de bloedvaten van de hersenen bekleden, en stelt een eenvoudige maar cruciale vraag: helpt het de beschermende bloed–hersenbarrière intact te houden, en heeft dat gevolgen voor de cognitie?
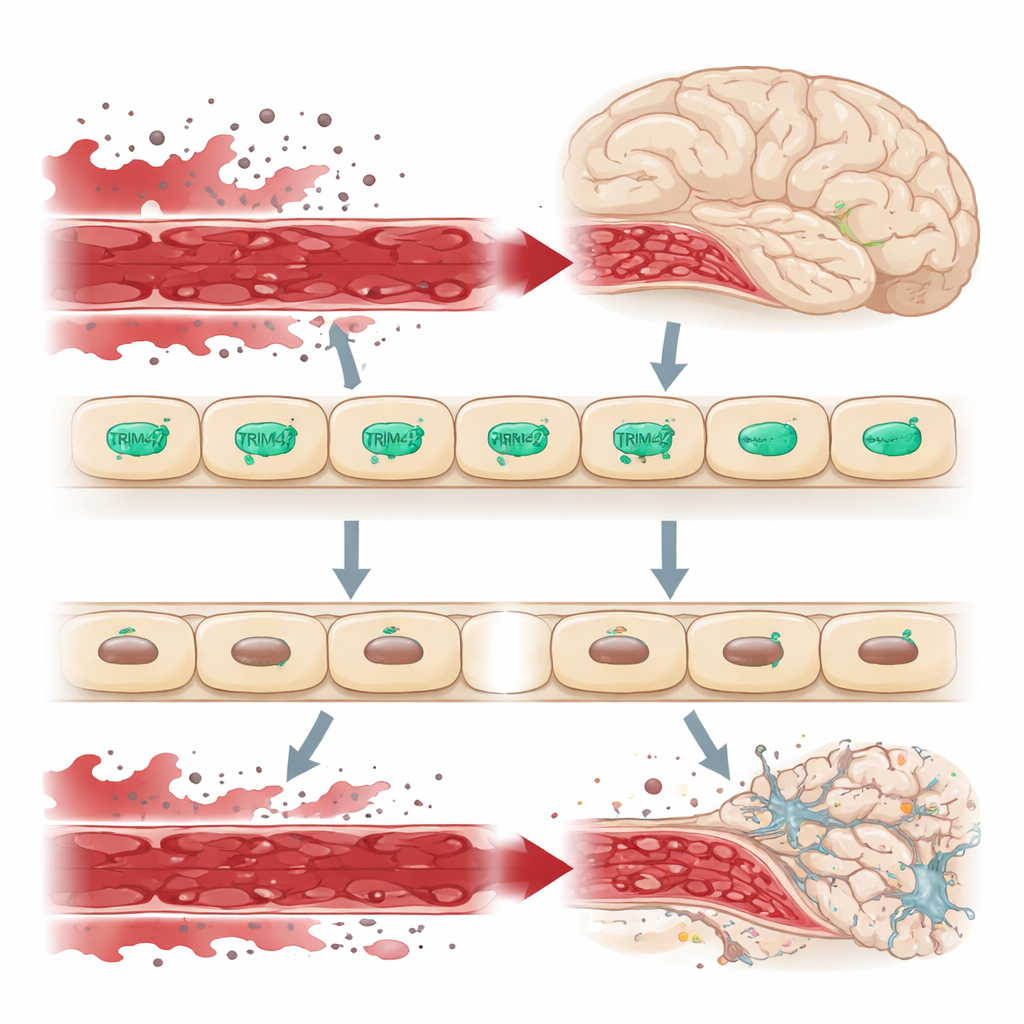
Een poortwachter aan de grens van de hersenen
De hersenen zijn afgeschermd van de rest van de bloedbaan door de bloed–hersenbarrière, een strak afgesloten bekleding van endotheelcellen die streng controleert wat de hersenweefsels binnenkomt. Als deze barrière gaat lekken, sijpelen schadelijke bloedbestanddelen de hersenen binnen, wat zenuwcellen en ondersteunende cellen belast en bijdraagt aan aandoeningen zoals dementie. Genetische studies in grote menselijke cohorten wezen naar een DNA‑gebied waarin het TRIM47‑gen ligt als een risicoregion voor cerebrale kleinevatenziekte. TRIM47 is vooral actief in hersenendotheelcellen, wat suggereert dat het een belangrijke bewaker van deze barrière kan zijn.
Hoe TRIM47 cellen beschermt tegen oxidatieve stress
De auteurs bestudeerden eerst menselijke hersenendotheelcellen in het laboratorium en verlaagden TRIM47‑niveaus met RNA‑interferentie. Dit veroorzaakte brede veranderingen in genactiviteit, waarbij het meest aangetaste netwerk rond NRF2 draaide, een hoofdregelaar van de cellulaire antioxidatieve verdediging. Onder normale omstandigheden wordt NRF2 in toom gehouden door het eiwit KEAP1, dat het naar afbraak dirigeert. Het team liet zien dat TRIM47 aan KEAP1 bindt en helpt voorkomen dat NRF2 wordt afgebroken. Met TRIM47 kan NRF2 zich ophopen, naar de kern verplaatsen en genen inschakelen die reactieve zuurstofsoorten ontgiften. Wanneer TRIM47 ontbreekt, dalen NRF2‑niveaus, zijn antioxidantgenen minder actief en worden endotheelcellen kwetsbaarder voor oxidatieve stress.
Van lekkende vaten naar geheugenproblemen bij muizen
Om te onderzoeken hoe dit mechanisme in een levende hersen werkt, maakten de onderzoekers muizen die het Trim47‑gen in het hele lichaam misten, en een andere lijn waarin Trim47 alleen in endotheelcellen kon worden verwijderd. Volwassen dieren van beide modellen ontwikkelden duidelijke tekorten in ruimtelijk leren en geheugen; ze faalden in taken zoals het Y‑maze en het Morris watermaze ondanks normale bewegingsmogelijkheden. Onderzoek van hun hersenen toonde aan dat de bloed–hersenbarrière was gaan lekken: kleine fluorescerende tracers en bloedproteïnen ontsnapten uit vaten naar het omliggende weefsel. Belangrijke "afdichtende" eiwitten die strakke en adherens‑junctions tussen endotheelcellen vormen, vooral Claudin‑5 en Occludin, waren verminderd. Nabijgelegen astrocyten, de stervormige ondersteunende cellen die snel op letsel reageren, raakten geactiveerd, ook al waren er in dit stadium weinig aanwijzingen voor brede ontsteking of verlies van neuronen.
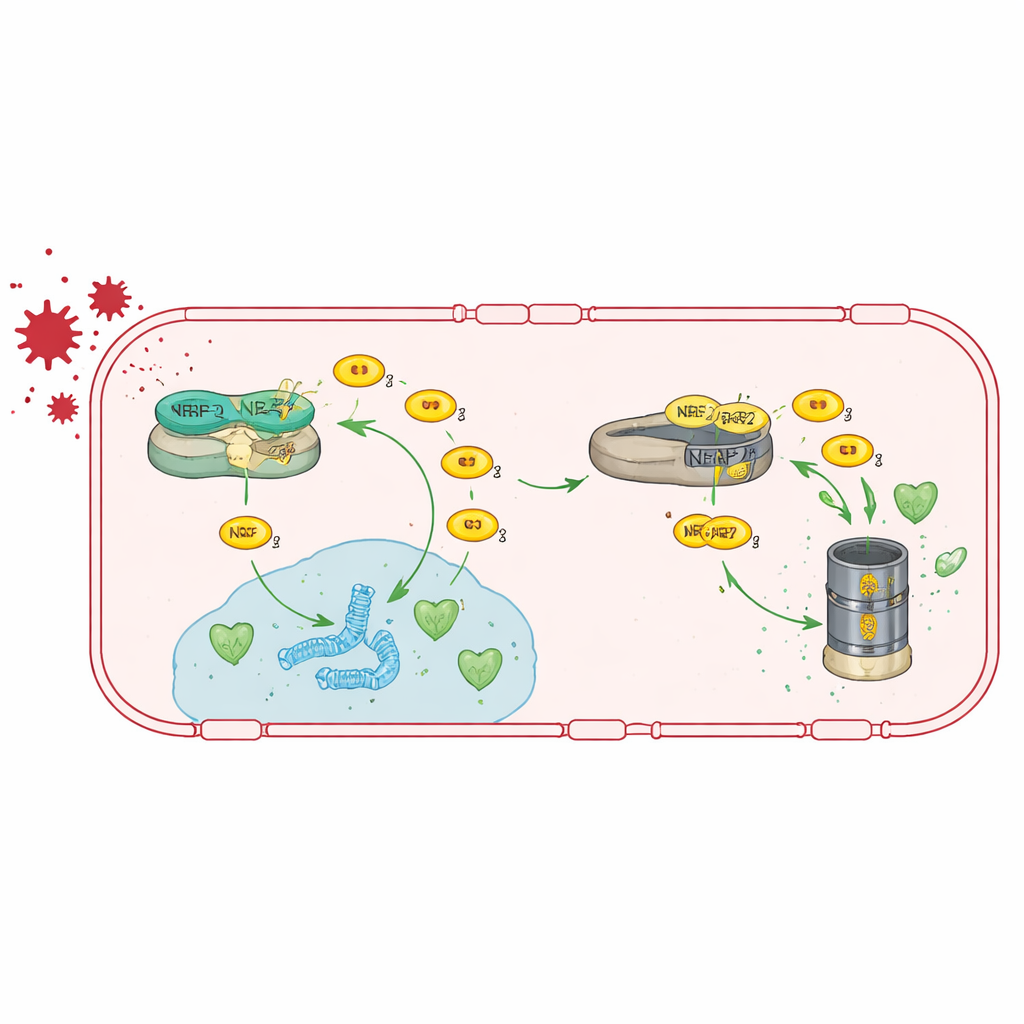
De antioxidantroute weer inschakelen
Aangezien TRIM47 vooral werkt door NRF2‑activiteit te versterken, testte het team of ze het tekort konden omzeilen door NRF2 rechtstreeks te stimuleren. Ze voedden Trim47‑deficiënte muizen met een dieet dat tert‑butylhydrochinon (tBHQ) bevatte, een verbinding die bekendstaat om NRF2 te stabiliseren en zijn doelgenen aan te zetten. Deze behandeling herstelde de activiteit van antioxidantgenen in hersenendotheelcellen, bracht de expressie van junctiongenen terug naar bijna normaal en verminderde het lekken van de bloed–hersenbarrière. Opmerkelijk genoeg normaliseerde het ook de activatie van astrocyten en herstelde het de prestaties van de dieren in geheugentests, wat suggereert dat het versterken van deze antioxidantroute zowel vasculaire als cognitieve problemen kan omkeren, althans bij muizen.
Aanwijzingen uit menselijk bloed en wat hierop volgt
Om hun muisonderzoeken te koppelen aan menselijke ziekte, analyseerden de onderzoekers eiwitten gerelateerd aan de NRF2‑route in bloedmonsters van duizenden mensen die hersen‑MRI’s hadden gekregen. De niveaus van meerdere door NRF2 gereguleerde eiwitten waren gekoppeld aan beeldvormingsmarkers van kleinevatenziekte, zoals vergrote perivasculaire ruimtes en veranderingen in witte stof. Dit ondersteunt het idee dat veranderde TRIM47–NRF2‑signalering relevant is bij mensen, niet alleen bij experimentele dieren, en dat deze eiwitten mogelijk als biomarkers voor ziekte‑ernst of progressie kunnen dienen.
Wat dit betekent voor hersengezondheid
Samengevat schetst het werk TRIM47 als een moleculaire bodyguard die helpt dat hersenbloedvaten bestand zijn tegen oxidatieve schade door het NRF2‑antioxidantsysteem te stabiliseren. Wanneer TRIM47 ontbreekt of niet goed functioneert, verzwakt de bloed–hersenbarrière, hoopt subtiel hersenletsel zich op en begint het geheugen achteruit te gaan. Het reactiveren van de NRF2‑route kan de barrière herstellen en de cognitie bij muizen terugbrengen, waarmee deze signaalas een veelbelovend therapeutisch doelwit wordt voor vasculaire vormen van dementie. Hoewel tBHQ zelf niet geschikt is als medicijn voor mensen, zouden veiligere NRF2‑versterkende verbindingen of strategieën die de beschermende rol van TRIM47 nabootsen op termijn de hersengezondheid kunnen helpen behouden door de kleinste, meest kwetsbare vaten te versterken.
Bronvermelding: Delobel, V., Grenier, C., Boulestreau, R. et al. Endothelial TRIM47 regulates blood-brain barrier integrity and cognition via the KEAP1/NRF2 signalling pathway in mice. Commun Biol 9, 399 (2026). https://doi.org/10.1038/s42003-026-09628-5
Trefwoorden: cerebrale kleinevatenziekte, bloed–hersenbarrière, TRIM47, NRF2‑route, vasculaire dementie