Clear Sky Science · nl
Een pad tussen subunits is vereist voor entropisch-gestuurde en negatief cooperatieve binding van cyclische nucleotiden in het HCN2-kanaal
Hoe de kleine pacemaker-schakelaar van het hart chemische signalen waarneemt
Elke hartslag en veel ritmes in de hersenen hangen af van microscopische kanalen die in de membranen van onze cellen openen en sluiten. Deze kanalen, HCN-pacemakerkanalen genoemd, worden niet alleen door elektrische spanning geregeld maar ook door kleine signaalmoleculen die cyclische nucleotiden heten. Deze studie stelt een bedrieglijk eenvoudige vraag met verstrekkende gevolgen: hoe binden deze kleine moleculen op een gecoördineerde manier aan het HCN2-kanaal, en hoe kunnen subtiele fouten in dat proces bijdragen aan aandoeningen zoals epilepsie?
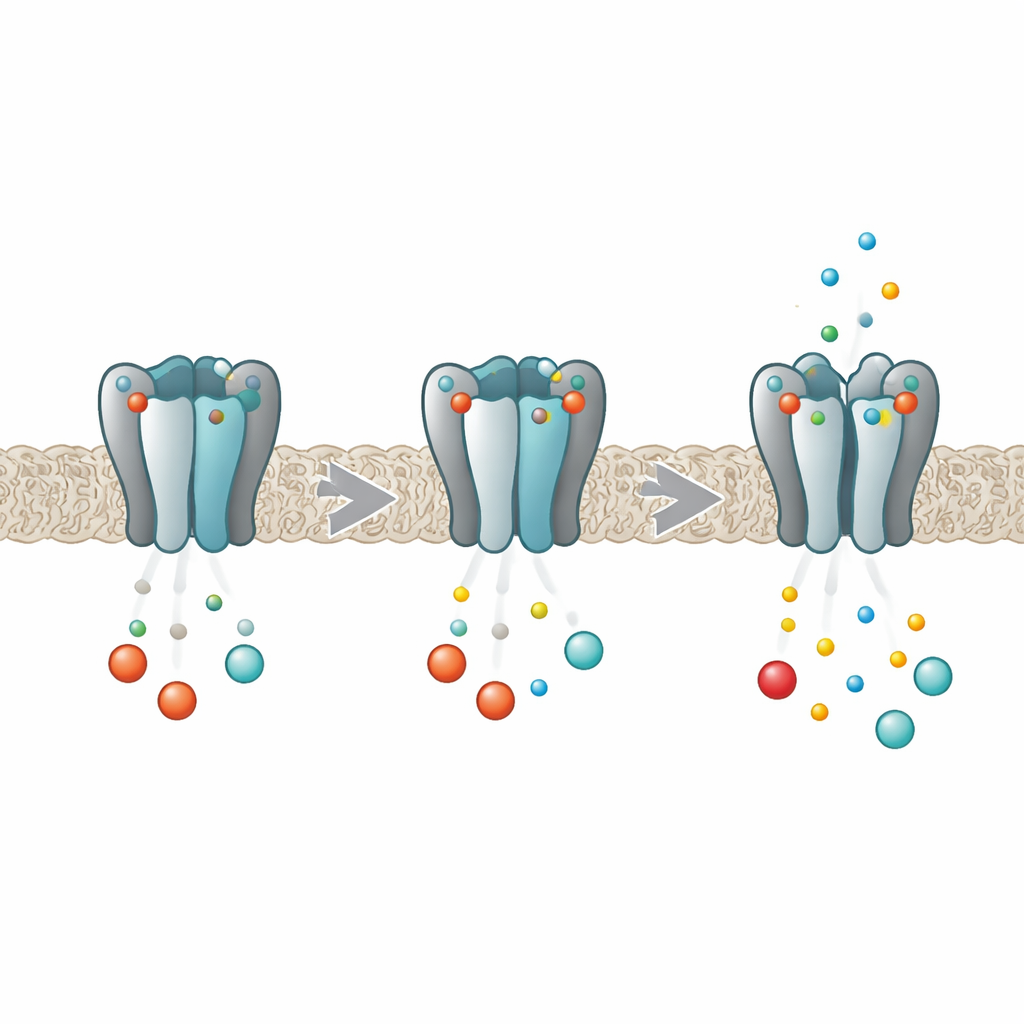
Een moleculaire dimmer voor de ritmes van het lichaam
HCN-kanalen werken als dimmers voor elektrische activiteit in hart- en hersencellen. Elk kanaal is opgebouwd uit vier identieke proteïnesubunits die samen een centraal poreus kanaal vormen waar ionen doorheen stromen. Diep in elke subunit bevindt zich een pocket die cyclische nucleotiden zoals cAMP en cGMP kan binden. Wanneer deze boodschappers binden, vergemakkelijken ze het openen van het pore, waardoor de pacemakerstroom toeneemt. Eerder werk toonde dat bij de HCN2-variant de binding zich niet onafhankelijk in elke pocket voordoet; in plaats daarvan beïnvloeden de vier sites elkaar zodanig dat het eerste molecuul makkelijker bindt dan de volgende, een gedrag dat bekendstaat als negatieve cooperativiteit. Het nieuwe werk wilde precies uitzoeken hoe de vier subunits met elkaar communiceren tijdens dit proces.
Subunits die hun buren aanvoelen
De onderzoekers combineerden computersimulaties met laboratoriummetingen aan geïsoleerde delen van het HCN2-kanaal. Met lange moleculaire dynamica-simulaties observeerden ze hoe de staartregio van het kanaal—het deel dat de cyclische nucleotidepockets en de zogeheten C-linker bevat die met het pore verbindt—buigt en wiebelt naarmate verschillende aantallen cAMP- of cGMP-moleculen zijn gebonden. Ze vonden dat wanneer een boodschapper zich in één subunit verankerde, dit niet slechts die subunit stabiliseerde. In plaats daarvan veranderde het subtiel de stabiliteit van de buren, soms maakte het ze stijver, soms flexibeler, ook al verschilde de algehele eiwitstructuur nauwelijks. Deze invloed van buur op buur hing af van hoeveel sites bezet waren en waar die sites rond de ring lagen, wat overeenkomt met wat je zou verwachten bij negatieve cooperativiteit.
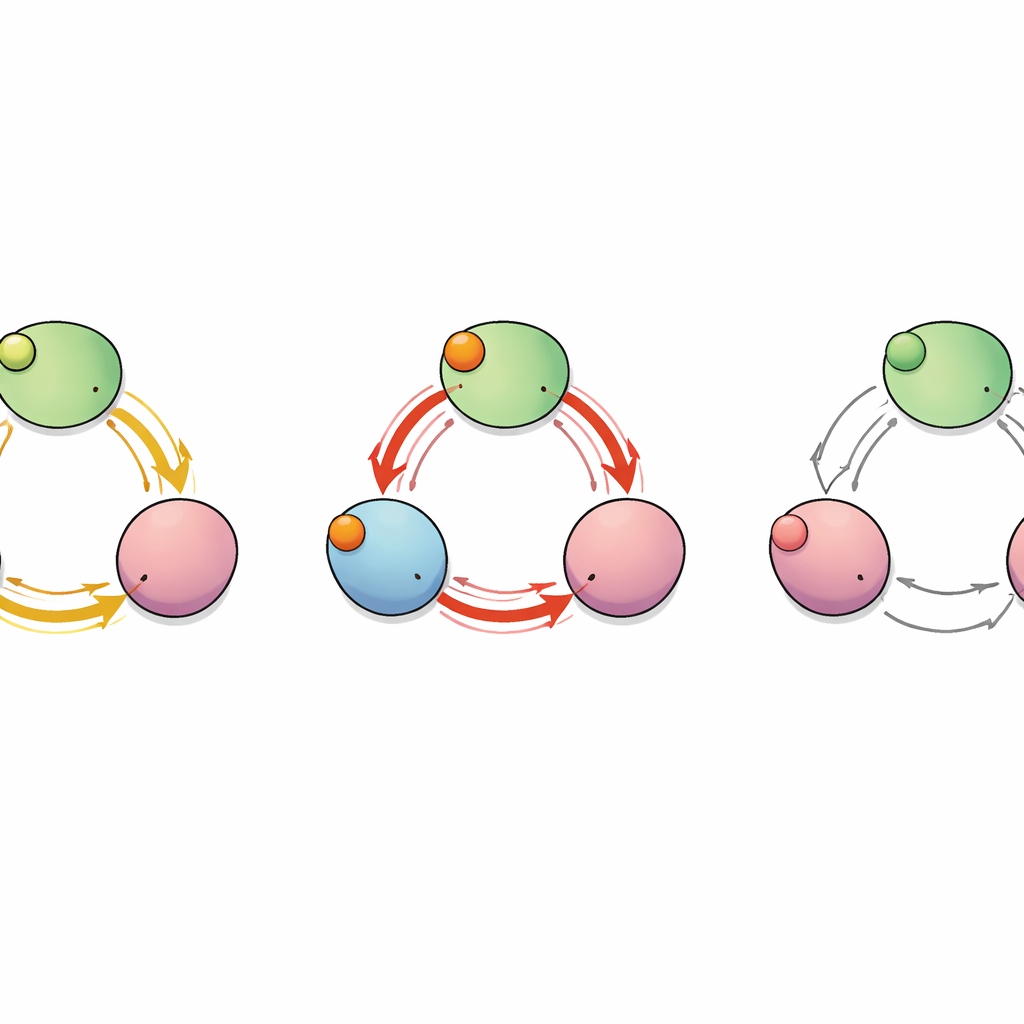
Een verborgen route tussen subunits
Om in kaart te brengen hoe het "signaal" van binding door het eiwit reist, behandelde het team het kanaal als een netwerk van interacterende aminozuren. Ze berekenden welke residuen tijdens de simulaties in een gecorreleerde manier bewogen en gebruikten grafentheoretische hulpmiddelen om de kortste en meest efficiënte communicatiepaden te identificeren van de bindingspockets naar de C-linkersegmenten die het pore aansturen. Deze analyse toonde verschillende mogelijke routes, maar twee sprongen eruit: één die binnen een enkele subunit bleef en een andere die van de ene subunit naar zijn buur sprong. Langs dit inter-subunitpad fungeerde één residu—glutamaat op positie 488 (E488)—als een kritisch knooppunt waar veel van de kortste paden doorheen liepen, wat suggereert dat het een sleutelrelaispunt voor cooperatieve binding kan zijn.
Mutaties die het gesprek verbreken
De auteurs gingen vervolgens over tot experimenten met gezuiverde kanaalstaarten om het belang van dit pad te testen. Ze veranderden E488 en het nabije tyrosine 459 (Y459), dat op de aangrenzende subunit ligt waar het pad aankomt. Met dynamische lichtverstrooiing bevestigden ze dat de gemuteerde proteïnen nog steeds tot vier-subunitcomplexen assembleerden, maar ze toonden niet langer de sterke ligand-geïnduceerde aanscherping tussen subunits die bij het normale eiwit werd gezien. Isotherme titratiekalorimetrie, die de kleine bindingswarmtes meet, onthulde een nog grotere verandering: wildtype HCN2 vertoonde twee duidelijke bindingsevenementen, één hoog-affiniteitstap die voornamelijk door een toename in entropie (grotere interne beweging) werd gedreven, gevolgd door drie lagere-affiniteitstappen. Daarentegen toonden mutants in E488 of Y459 slechts één enkel, bescheiden-affiniteit bindingspatroon dat deze gunstige entropische impuls miste en de kenmerkende negatieve cooperativiteit verloor.
Waarom subtiele entropieveranderingen ertoe doen
Gecombineerd schetst de studie het HCN2-kanaal als een dynamische ring van vier subunits verbonden door specifieke "gesprekspaden." Wanneer het eerste cyclische nucleotide bindt, verandert het de bewegingen van verre delen van de ring via E488 en Y459, waardoor latere bindingen minder gunstig worden en de reactie van het pore wordt bijgestuurd. Dit effect wordt niet aangedreven door grote structurele herschikkingen maar door veranderingen in interne flexibiliteit—entropiewijzigingen die onzichtbaar zijn in statische snapshots maar cruciaal voor de functie. Mutaties die de sleutelresiduen langs dit inter-subunitpad verstoren, leggen het gesprek stil, maken negatieve cooperativiteit ongedaan en worden in verband gebracht met aandoeningen zoals idiopathische gegeneraliseerde epilepsie. Voor een niet-specialistische lezer is de kernboodschap dat levensbelangrijke schakelaars in hart en hersenen steunen op verfijnd georkestreerde moleculaire "fluisteringen" tussen proteïnesubunits, en dat het begrijpen van die fluisteringen helpt verklaren hoe normale ritmes tot stand komen en wat er gebeurt wanneer ze ontsporen.
Bronvermelding: Costa, F., Ng, L.C.T., Chow, S.S. et al. An inter-subunit path is required for entropically-driven and negatively cooperative binding of cyclic nucleotides in the HCN2 channel. Commun Biol 9, 362 (2026). https://doi.org/10.1038/s42003-026-09626-7
Trefwoorden: HCN2-ionenkanaal, binding van cyclische nucleotiden, negatieve cooperativiteit, allosterische communicatie, epilepsie-mutatie