Clear Sky Science · nl
Een kleine molecule activeert SecA-afhankelijke secretie allosterisch
De exportterminal van bacteriën in overdrive zetten
Bacteriën overleven door constant eiwitten naar buiten te exporteren via kleine poorten in hun membranen. Deze exports helpen bij de bouw van celwanden, het uitscheiden van toxines en het aanpassen aan stress—processen die centraal staan in veel infecties. In deze studie wordt een kleine stof gerapporteerd, HSI#6 genoemd, die iets ongewoons doet: in plaats van deze exportmachinerie te blokkeren, zet het deze om in een hyperactieve, minder selectieve modus. Begrijpen hoe deze schakel werkt kan zowel nieuwe antibacteriële strategieën onthullen als de biotechnologie een manier bieden om eiwitsecretie op aanvraag te verhogen.
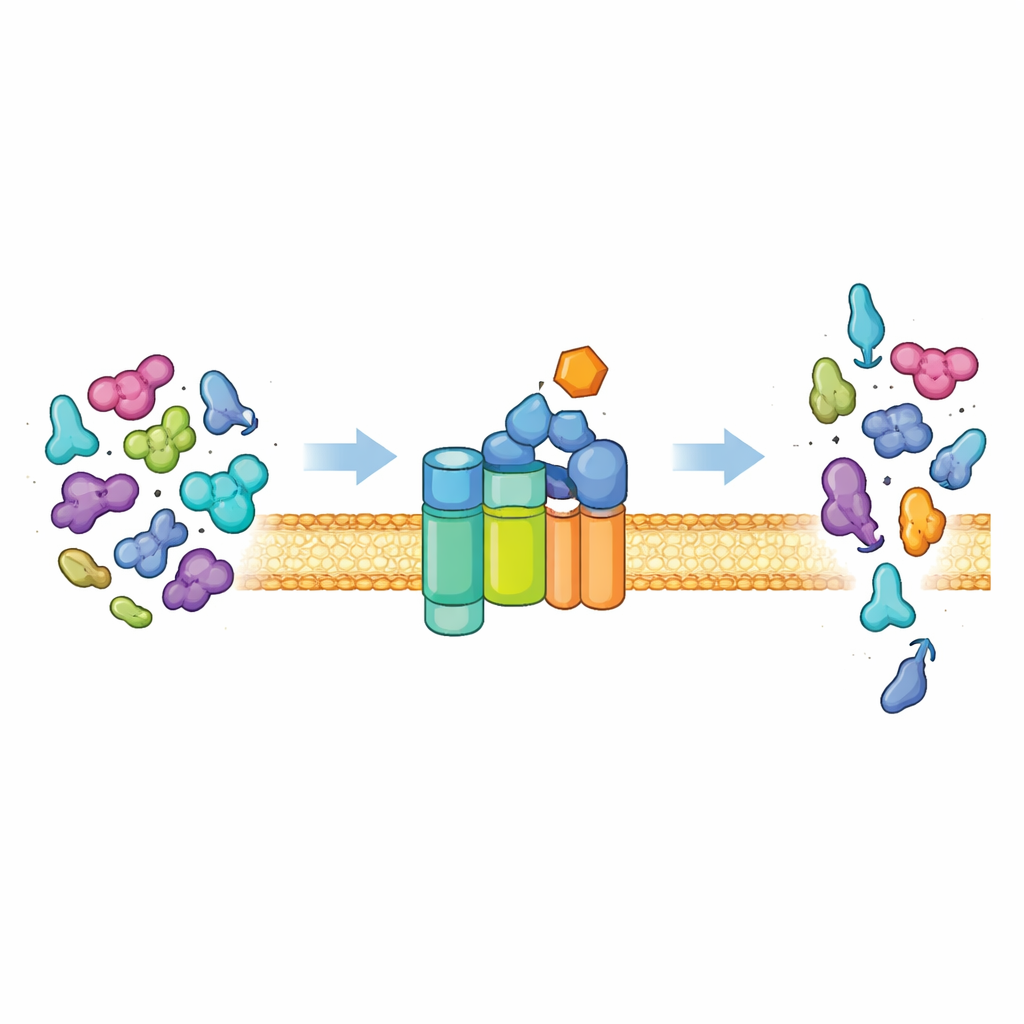
De eiwituitgangspoort van de cel
De meeste bacteriën exporteren eiwitten uit de cel via een universeel pad dat bekendstaat als het Sec-systeem. Centraal daarin staat een membraankanaal (SecYEG) en een motorisch eiwit (SecA) dat cellulaire brandstof (ATP) verbruikt om ongevouwen polypeptideketens door het kanaal te duwen. Onder normale omstandigheden is dit systeem kieskeurig. Het exporteert voornamelijk "pre-eiwitten" die speciale adreslabels dragen, bekend als signaalpeptiden, plus aanvullende kenmerken in hun hoofdstructuur. Deze kenmerken zijn nodig om SecA te schakelen van een rustige, weinig actieve toestand naar een krachtige motor. Alleen eiwitten die de juiste combinatie van signalen hebben, kunnen de volledige activiteit ontgrendelen, waardoor de cel het juiste vrachtgoed exporteert en gewone cytoplasmatische eiwitten veilig binnenhoudt.
Een kleine molecule die de motor wekt
De onderzoekers ontdekten HSI#6 in een screen naar verbindingen die bacteriële eiwitsecretie en groei beïnvloeden. Biochemische tests toonden aan dat HSI#6 direct aan SecA bindt met micromolaire affiniteit en verandert hoe efficiënt het ATP gebruikt. In oplossing zorgt het ervoor dat SecA ATP steviger vasthoudt; wanneer SecA aan het kanaal gebonden is, verbetert HSI#6 zowel ATP-binding als de snelheid van ATP-omzetting. Dit patroon is kenmerkend voor een allosterische activator: een molecule die op één plaats aan een eiwit bindt maar de activiteit op een andere, verder gelegen plaats verandert. In tegenstelling tot natuurlijke proteïnecliënten hoeft HSI#6 niet te fungeren als vracht om de motor te stimuleren—het stemt simpelweg de interne dynamiek van SecA bij zodat de hele translocase katalytisch geprimed raakt.
Van selectief filter naar promiscuuze nanomachine
Zodra HSI#6 gebonden is, eist het Sec-systeem niet langer de gebruikelijke exportlabels. In proeffles-experimenten verdubbelde de verbinding ruwweg de secretie van een standaard pre-eiwit en maakte het complex resistenter tegen natriumazide, een bekende SecA-remmer. Nog opvallender, HSI#6 stelde de normale, “wild-type” machinerie in staat om eiwitten te verplaatsen die helemaal geen signaalpeptiden hebben, evenals eiwitten die normaal in het cytoplasma verblijven. In levende bacteriële cellen werd hetzelfde effect gezien met behulp van alkaline fosfatase–gebaseerde reporters: wanneer cytoplasmatische eiwitten aan een secretoir enzym werden gefuseerd, veroorzaakte de aanwezigheid van HSI#6 een sterke stijging in uitgescheiden activiteit zonder de eiwitproductie te veranderen. Met andere woorden, HSI#6 koppelt export effectief los van de gebruikelijke identiteitstoetsen van cliënten en verandert het Sec-systeem in een breed werkende exportpomp voor elk voldoende ongevouwen eiwit.
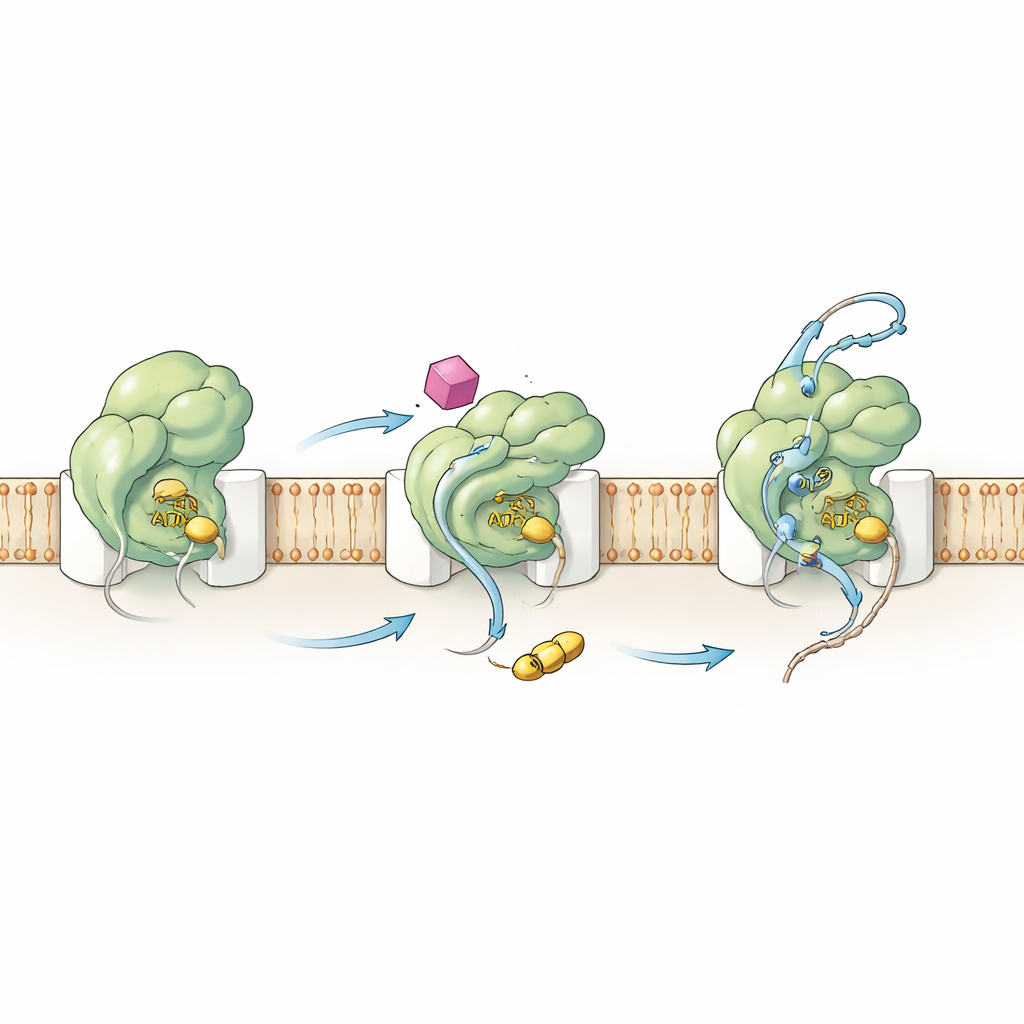
De motor van binnenuit herbedraden
Om te begrijpen hoe HSI#6 dit gedrag veroorzaakt, onderzocht het team zowel de chemie als de bewegingen van SecA. Kinetische metingen toonden aan dat de verbinding de sleutelstap van activatie naar een eerder stadium verschuift: het SecA–kanaalcomplex wordt katalytisch actief nog voordat een proteïnecliënt bindt. HSI#6 helpt SecA ook bij het loslaten van verbruikte brandstof (ADP), een normaal gesproken trage, beperkende stap, en ondersteunt daardoor snellere ATP-cycli. Met waterstof–deuterium-uitwisselings-massaspectrometrie brachten de auteurs in kaart hoe HSI#6 de flexibiliteit van verschillende SecA-regio’s herschikt. De verbinding versoepelt selectief delen van het eiwit die cliënten voelen en met het kanaal verbinden, terwijl een ondersteunende scaffold-regio juist verhardt en waarschijnlijk de bindingsplaats huisvest. Het resulterende bewegingspatroon lijkt op een reeds geactiveerde, "aan"-toestand van de translocase, wat suggereert dat HSI#6 een geactiveerde vorm stabiliseert—mogelijk zelfs een monomere SecA gebonden aan het kanaal—zonder dat er een cliënt aanwezig is.
Waarom dit belangrijk is voor geneeskunde en biotechnologie
Door aan te tonen dat een kleine molecule SecA allosterisch kan activeren en zijn normale cliëntselectiviteit kan wegnemen, onthult dit werk een nieuwe manier om een centraal bacterieel systeem te beheersen. Voor infectieziekten kan dergelijke geforceerde, ongecontroleerde secretie pathogenen verzwakken door energie weg te zuigen en hun fijn afgestemde exportprogramma’s te verstoren, waardoor HSI#6-achtige activatoren aantrekkelijke uitgangspunten zijn voor antibioticadesign—of als leidraad voor het ontwikkelen van toekomstige remmers die dezelfde regulerende kenmerken blokkeren. Voor de biotechnologie kan hetzelfde principe worden hergebruikt om de secretie van nuttige recombinante eiwitten te verbeteren, zonder de noodzaak voor ontworpen signaalpeptiden of complexe genetische aanpassingen. In wezen toont de studie aan dat de bacteriële eiwit-"exportterminal" chemisch kan worden geherprogrammeerd, wat nieuwe wegen opent om microben te bestrijden en ze als microscopische fabrieken te benutten.
Bronvermelding: Sedky, H., Hamed, M.B., Krishnamurthy, S. et al. A small molecule allosterically activates SecA dependent secretion. Commun Biol 9, 368 (2026). https://doi.org/10.1038/s42003-026-09623-w
Trefwoorden: bacteriële eiwitsecretie, SecA-translocase, allosterische activatie, kleine molecule-regulatoren, ontdekking van antibacteriële geneesmiddelen