Clear Sky Science · nl
LncRNA P4HA2-AS1 bevordert renale interstitiële fibrose via TRIM32-gemedieerde K63-ubiquitinylering van ULK1 en verstoring van autofagie
Waarom nieraandoeningen door littekenvorming ertoe doen
Chronische nierziekte treft honderden miljoenen mensen wereldwijd en sluipt vaak stilletjes voort totdat dialyse of een transplantatie de enige manier zijn om in leven te blijven. Centraal in deze achteruitgang staat een proces dat littekenvorming wordt genoemd, waarbij gezond nierweefsel geleidelijk wordt vervangen door stijf, niet-functioneel materiaal. Deze studie stelt een eenvoudige maar cruciale vraag: welke moleculaire schakelaars in niercellen sturen ze richting deze schadelijke littekenvorming, en kunnen die schakelaars worden teruggedraaid?
Een verborgen RNA-schakelaar in niercellen
Onze nieren filteren bloed met ingewikkelde netwerken van kleine tubuli. Wanneer deze tubuli beschadigd raken door een blokkade van de urineafvoer, hoge bloedsuiker of een plotseling verlies van bloedtoevoer, kunnen ze reageren door littekenweefsel tussen de cellen af te zetten. De onderzoekers doorzochten de nieren van muizen met verschillende soorten letsel en vergeleken die met gezonde nieren met behulp van RNA-sequencing, een techniek die uitleest welke genen aan staan. Ze ontdekten dat een weinig bekend molecuul, P4HA2-AS1 — een lang niet-coderend RNA dat geen eiwit produceert — consequent verhoogd was in beschadigde, littekenvormende nieren en in menselijke niercellen die in het laboratorium onder stress stonden. Dit RNA werd voornamelijk in het vloeistofgevulde deel van de cellen aangetroffen, wat suggereert dat het daar andere eiwitten kan reguleren. 
Het RNA omlaag brengen ter bescherming van de nier
Om te testen of P4HA2-AS1 slechts een bijstander is of een actieve veroorzaker van schade, verlaagde het team de niveaus ervan in muizen en in gekweekte menselijke niercellen. In een goed gevestigd muismodel waarbij één ureter wordt dichtgebonden om langdurige obstructie te veroorzaken, verminderde het verlagen van dit RNA via gerichte virale afgifte veel kenmerken van littekenvorming: tubuli bleven beter intact, er was minder collageen en andere litteken-eiwitten tussen de cellen, en markers voor nierfunctie in het bloed verbeterden. In kweekschalen van menselijke niercellen dempte het verkleinen van P4HA2-AS1 ook de reactie op een krachtige littekenstimulus, TGF-β, wat leidde tot minder productie van fibronectine, collageen en andere profibrotische factoren. Deze experimenten toonden aan dat dit RNA niet slechts een merker van schade is, maar actief het littekenproces voedt.
Autofagie: van huishouding naar schade
De onderzoekers vroegen vervolgens hoe dit RNA schade veroorzaakt. Hun genexpressie- en beeldvormingsgegevens wezen op autofagie, het ingebouwde recyclingsysteem van de cel dat versleten eiwitten en organellen afbreekt. Onder normale omstandigheden is autofagie een gezonde huishoudfunctie, maar wanneer die te lang en te sterk geactiveerd wordt, kan het beschadigde nieren naar schadelijke herstelprocessen en fibrose duwen. In gestreste niercellen verhoogde P4HA2-AS1 de doorstroming van materiaal via autofagie, wat leidde tot een ophoping van recyclingblaasjes. Wanneer het RNA werd geblokkeerd, daalde deze overactieve recycling weer richting normaal, zowel in cellen als in de nieren van geobstrueerde muizen. Muizen zonder ULK1, een centrale startende kinase voor autofagie, waren ook beschermd tegen littekenvorming, en bij deze dieren kon overexpressie van P4HA2-AS1 de schade niet langer verergeren, wat de effecten van het RNA stevig koppelt aan deze route.
Een moleculaire keten in drie delen
Dieper gravend gebruikten de onderzoekers biochemische 'vis'-technieken om eiwitten te identificeren die fysiek binden aan P4HA2-AS1. Één eiwit viel op: TRIM32, een enzym dat andere eiwitten markeert met kleine moleculaire "vlaggetjes" genaamd ubiquitine. Het RNA bindt aan TRIM32 en beschermt het tegen afbraak, waardoor de niveaus ervan in niercellen stijgen. Gestabiliseerd TRIM32 hecht op zijn beurt een specifiek type ubiquitineketen aan ULK1. In plaats van ULK1 naar vernietiging te sturen, werkt deze keten als een versterker en verhoogt het de capaciteit van ULK1 om autofagie te activeren. Wanneer de wetenschappers TRIM32 bij muizen verwijderden of het in niercellen stillegden, namen zowel littekenvorming als excessieve autofagie af. Het opnieuw inbrengen van TRIM32 in cellen waarin P4HA2-AS1 was geblokkeerd, herstelde gedeeltelijk de fibrotische respons, wat laat zien dat dit enzym een belangrijke schakel in de keten is. 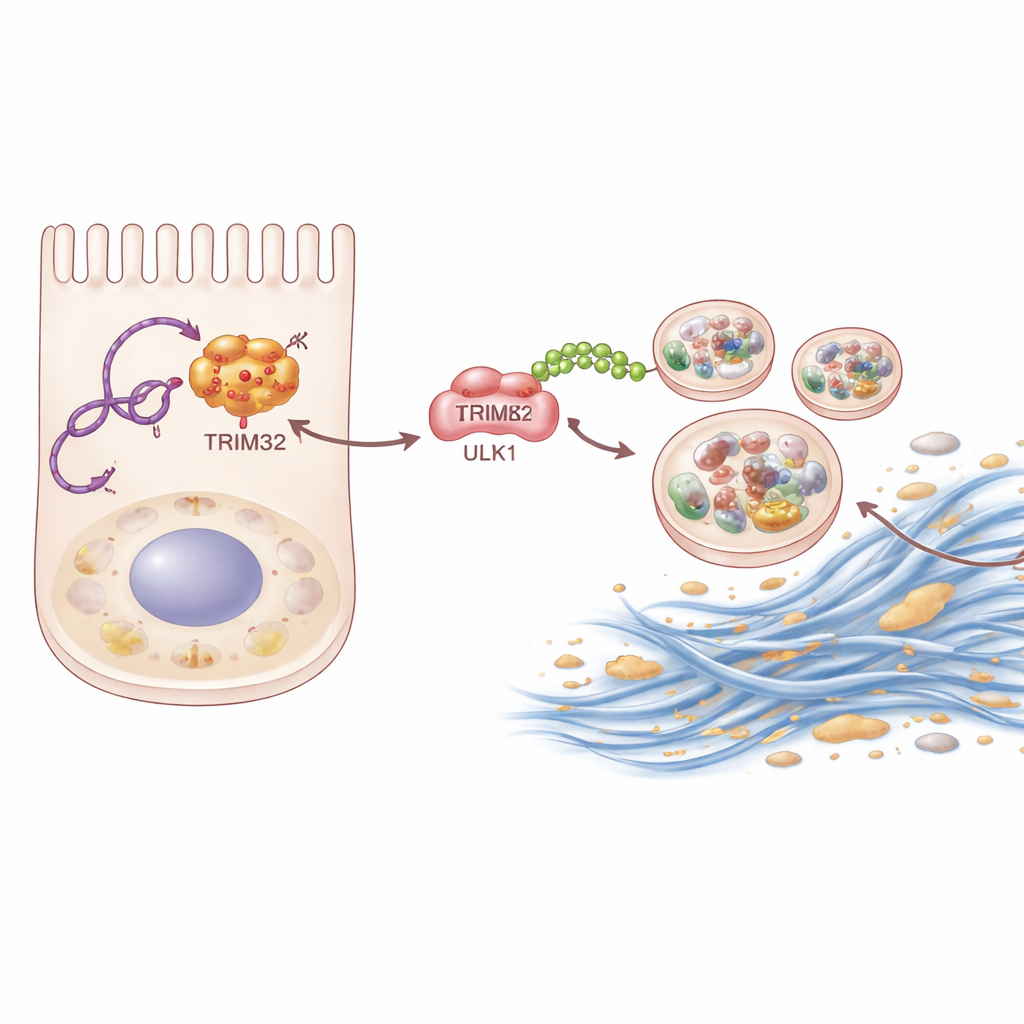
Nieuwe wegen naar soepelere nieren
Gezamenlijk onthult dit werk een eerder onbekende moleculaire route die lang niet-coderend RNA, eiwitmarkering en cellulaire recycling verbindt met de opbouw van nierlittekenweefsel. In beschadigde nieren stijgt P4HA2-AS1, stabiliseert TRIM32, versterkt ULK1 en drijft autofagie voorbij haar nuttige grens, wat uiteindelijk de ophoping van fibrotische eiwitten en functieverlies bevordert. Voor niet-specialisten is de belangrijkste boodschap dat nierfibrose geen onvermijdelijke zwarte doos is: ze wordt aangestuurd door identificeerbare schakelaars die mogelijk met geneesmiddelen te beïnvloeden zijn. Het richten op deze P4HA2-AS1–TRIM32–ULK1-as — door het rogue-RNA te verlagen, TRIM32 te temmen of ULK1-activiteit fijn af te stemmen — zou op een dag nieuwe behandelingen kunnen bieden om de progressie van chronische nierziekte te vertragen of te voorkomen.
Bronvermelding: Pan, Z., Xiao, F., Hu, W. et al. LncRNA P4HA2-AS1 drives renal interstitial fibrosis via trim32-mediated k63 ubiquitination of ULK1 and autophagic dysregulation. Commun Biol 9, 339 (2026). https://doi.org/10.1038/s42003-026-09618-7
Trefwoorden: chronische nierziekte, nierfibrose, autofagie, lange niet-coderende RNA, nierkanaaltjes