Clear Sky Science · nl
Remmer van reverse-transcriptase maken de productie van vruchtbare spermatiden uit foetale muizentesten in vitro mogelijk
Vroege kiemcellen omzetten in werkende sperma
Vruchtbaarheidsbehandelingen en fundamenteel onderzoek zijn beide afhankelijk van inzicht in hoe onrijpe kiemcellen in de testis veranderen in zaadcellen. Deze studie toont aan dat het nu mogelijk is om zeer vroege foetale muizentesten, genomen kort nadat het geslacht van het embryo is bepaald, volledig in een schaaltje deze transformatie te laten voltooien. Door de chemische omgeving en het zuurstofniveau zorgvuldig af te stemmen, produceerden de onderzoekers niet alleen rijpe, zaadcelachtige cellen, maar gebruikten ze die ook om gezonde, vruchtbare nakomelingen te genereren.
Waarom vroege testisontwikkeling moeilijk na te bootsen is
Het kweken van zaadcellen buiten het lichaam is eerder bereikt met testisweefsel van pasgeboren of oudere muizen, maar de efficiëntie was laag en pogingen met veel eerder foetaal weefsel faalden grotendeels. In dit vroege stadium bouwt de testis nog zijn interne architectuur op en ondergaan kiemcellen ingrijpende veranderingen in hoe hun DNA is verpakt en gemarkeerd. Het nabootsen van dit ingewikkelde choreografie in een kweek is uitdagend, en eerdere cultivaties bereikten zelden meer dan de vroege stappen wanneer begonnen werd met testen verzameld rond embryonale dag 12.5, kort na het vaststellen van het embryo‑geslacht.
Antivirale middelen lenen om ontwikkelende cellen te beschermen
Het team richtte zich op een verborgen obstakel: mobiele DNA-elementen genaamd retrotransposons, die zichzelf kunnen kopiëren en op nieuwe plekken in het genoom kunnen invoegen. In normale testen in het lichaam worden deze elementen sterk onderdrukt, vooral in kiemcellen. In kweek echter vonden de auteurs dat de activiteit van retrotransposons veel hoger was, terwijl de eigen verdedigingsgenen van de cellen stiller waren. Dit onevenwicht correleerde met slechte zaadcelontwikkeling. Omdat retrotransposons een reverse-transcriptase‑enzym gebruiken, vergelijkbaar met sommige virussen, testten de onderzoekers verschillende medicijnen die oorspronkelijk als reverse-transcriptaseremmers zijn ontworpen. Een specifieke mix van drie middelen, aangeduid als AEC, verdubbelde ongeveer het aandeel spermatogene cellen en verdrievoudigde meer dan het aandeel haploïde, zaadcelachtige cellen in gekweekte neonatale testen vergeleken met onbehandelde controles.
Van tiny foetale testen naar functioneel sperma
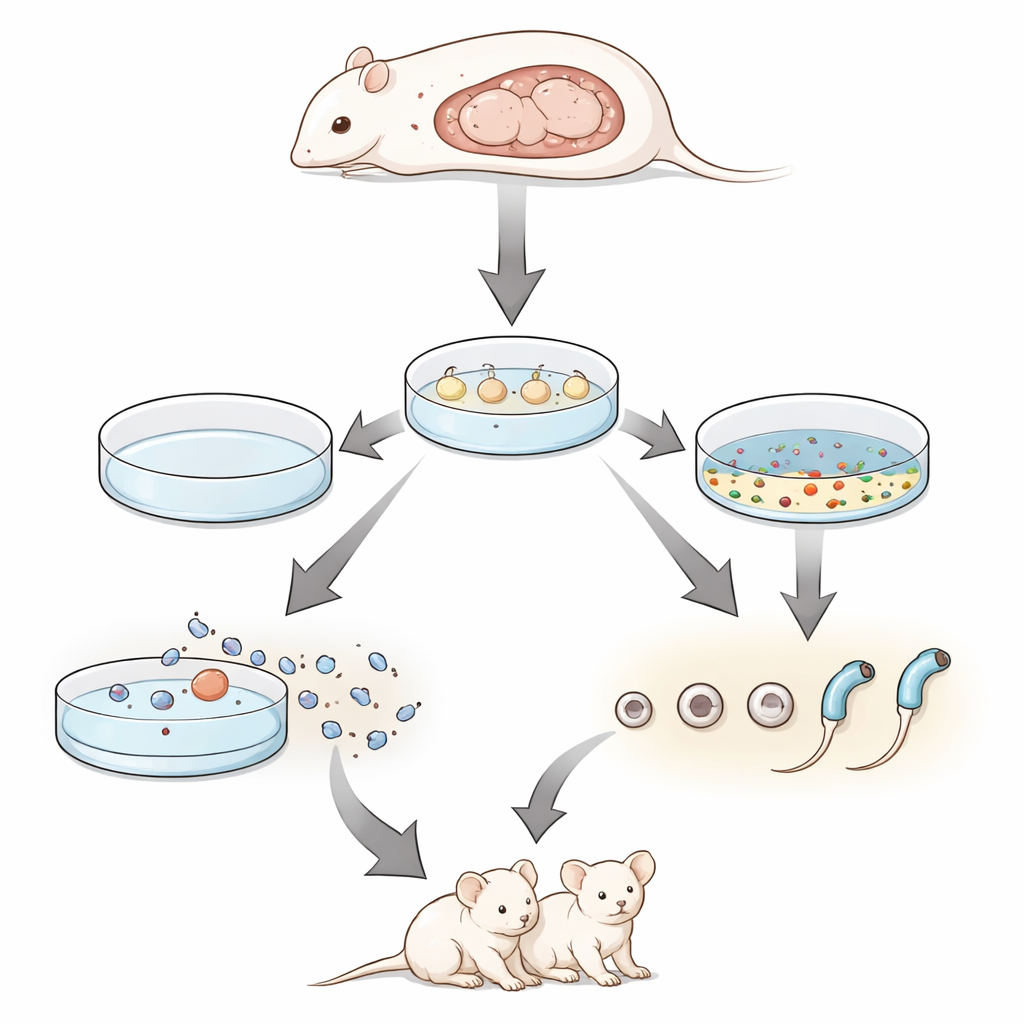
Gewapend met dit medicijncocktail richtten de wetenschappers zich op foetale testen. In weefsel dat iets voor de geboorte was genomen, bevorderden de remmers het verschijnen van gevorderde spermatiden. Nog opvallender was dat, wanneer zij testen kweekten van embryo’s op dag 12.5, een stadium waarvan nog nooit eerder is aangetoond dat het spermatogenese in vitro kan voltooien, ze nu ronde en verlengde spermatiden konden genereren. De grootste vooruitgang werd geboekt wanneer ze de remmix combineerden met een laag-zuurstof atmosfeer die beter de omstandigheden in het zich ontwikkelende lichaam nabootst. Onder deze hypoxische omstandigheden toonde ongeveer een derde van het weefseloppervlak merkers van gevorderde kiemcelontwikkeling, en er konden zaadcellen met staarten uit de cultuur worden teruggewonnen.
Testen of in het laboratorium gemaakte spermatiden echt werken
Om te achterhalen of deze in vitro‑afgeleide cellen werkelijk functioneel waren, gebruikte het team een techniek die round spermatid injection heet. Ze isoleerden ronde spermatiden uit de gekweekte foetale testen en injecteerden die in muizeieren die zacht waren geactiveerd. De resulterende embryo’s werden overgeplaatst naar pleegmoeders. Uit slechts twee gekweekte testisfragmenten leverde de procedure meerdere levende pups op, van wie velen een fluorescerend merkgene droegen dat hun gekweekte herkomst bevestigde. Toen deze eerstegeneratie‑dieren paren konden, produceerden ze normale worpen van gezonde nakomelingen in de tweede generatie, wat aantoont dat de in het lab afgeleide spermatiden niet alleen ontwikkeling tot de geboorte kunnen ondersteunen, maar ook volledige vruchtbaarheid kunnen doorgeven.
Hoe het blokkeren van mobiel DNA toekomstige therapieën mogelijk kan maken
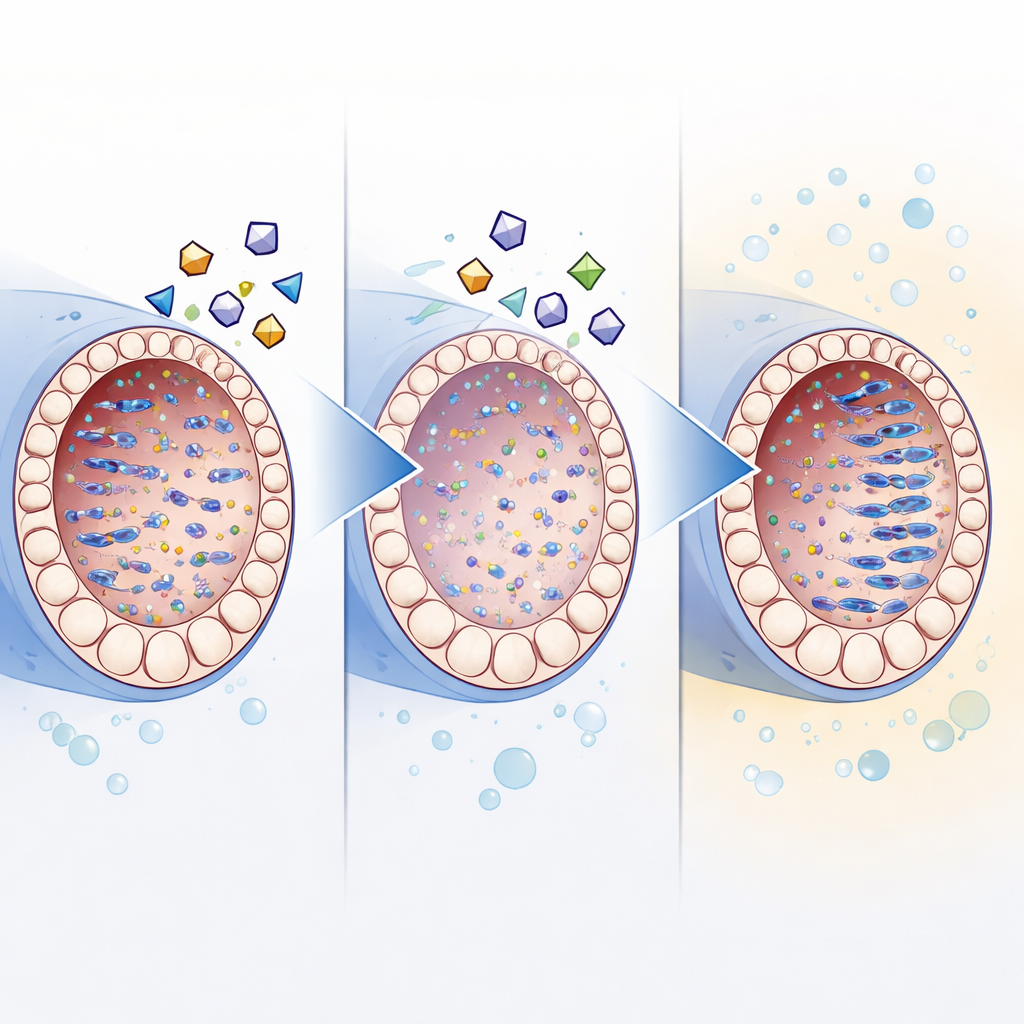
Verdere experimenten ondersteunden het idee dat reverse-transcriptase‑remmers vooral helpen door mobiel DNA in bedwang te houden. Vergeleken met leeftijdsgelijk testisweefsel in het lichaam, vertoonden gekweekte testen hogere niveaus van retrotransposon‑eiwitten en extra kopieën van hun DNA, samen met verminderde expressie van de natuurlijke stilleggingsmechanismen van de cellen. Het toevoegen van het remmencocktail verminderde deze accumulatie, terwijl het tegelijkertijd de rijping van kiemcellen verbeterde. Hoewel de medicijnen de algehele weefselgroei iets vertraagden, verbeterden pogingen om dit tegen te gaan met serumhoudende toevoegingen de zaadcelproductie niet, wat suggereert dat groei en juiste differentiatie zorgvuldig in balans moeten worden gehouden.
Wat dit betekent voor de voortplantingswetenschap
Dit werk laat zien dat zelfs zeer onrijpe foetale testen al alle ingrediënten bevatten die nodig zijn om een functionerende spermafabriek op te bouwen, mits de omgeving hun genomen beschermt en sleutelaspecten van het leven in de baarmoeder nabootst. Door antiviraleachtige medicijnen te combineren met lage zuurstof creëerden de onderzoekers een kweek systeem dat volledige spermatogenese uit een van de vroegste tot nu toe onderzochte stadia nabootst en nakomelingen oplevert die normaal groeien en zich voortplanten. Hoewel de studie bij muizen is en ver verwijderd van klinisch gebruik, opent het een krachtig venster op de vroegste stappen van de ontwikkeling van mannelijke kiemcellen en biedt het aanwijzingen die ooit kunnen helpen de vruchtbaarheid te behouden of te herstellen bij patiënten wiens voortplantingscellen vroeg in het leven beschadigd zijn geraakt.
Bronvermelding: Nishida, M., Ono-Sunagare, Y., Kato, S. et al. Reverse transcriptase inhibitors enable the generation of fertile spermatids from fetal mouse testes in vitro. Commun Biol 9, 329 (2026). https://doi.org/10.1038/s42003-026-09613-y
Trefwoorden: in vitro spermatogenese, kweek van foetale testis, reverse-transcriptase remmers, retrotransposons, mannelijke vruchtbaarheid