Clear Sky Science · nl
Obesitas schaadt spermatogenese via Leydig‑cel ferroptose geïnduceerd door lever‑afgeleide exosomale miR-122-5p
Waarom gewicht en vruchtbaarheid gekoppeld zijn
Obesitas wordt meestal besproken in termen van hartziekten en diabetes, maar het kan ook stilletjes de mannelijke vruchtbaarheid ondermijnen. Deze muizenstudie onthult een verrassende manier waarop een vetrijk dieet testosteron kan verlagen en de spermaproductie kan beschadigen: de lever stuurt kleine "berichtblaasjes" het bloed in die een bijzondere vorm van celdood in de hormoonproducerende cellen van de testes teweegbrengen. Inzicht in deze verborgen lever‑naar‑testis communicatie kan helpen verklaren waarom mannen met overgewicht vaak laag testosteron en onvruchtbaarheid ervaren, en kan richting geven aan nieuwe behandeldoelen.
Verborgen post tussen organen
Onze organen communiceren voortdurend met elkaar via hormonen en andere chemische boodschappers. Een vorm van deze communicatie gebruikt exosomen—nanometer‑grote blaasje die door cellen worden vrijgegeven en vetten, eiwitten en genetisch materiaal vervoeren. De onderzoekers begonnen met muizen die ofwel een normaal dieet ofwel een vetrijk dieet kregen dat obesitas, insulineresistentie en slechte suikercontrole veroorzaakte. Obese muizen hadden kleinere, minder actieve testes: hun spermaconcentraties, testosteronniveaus en de grootte en het aantal spermaproductie‑kanaaltjes waren allemaal verminderd. Bij onderzoek naar sleutelcelmarkers in de testes vonden ze minder testosteronproducerende Leydigcellen en minder vroege en late spermacellen, wat bevestigde dat de hele spermaproductielijn was aangetast. 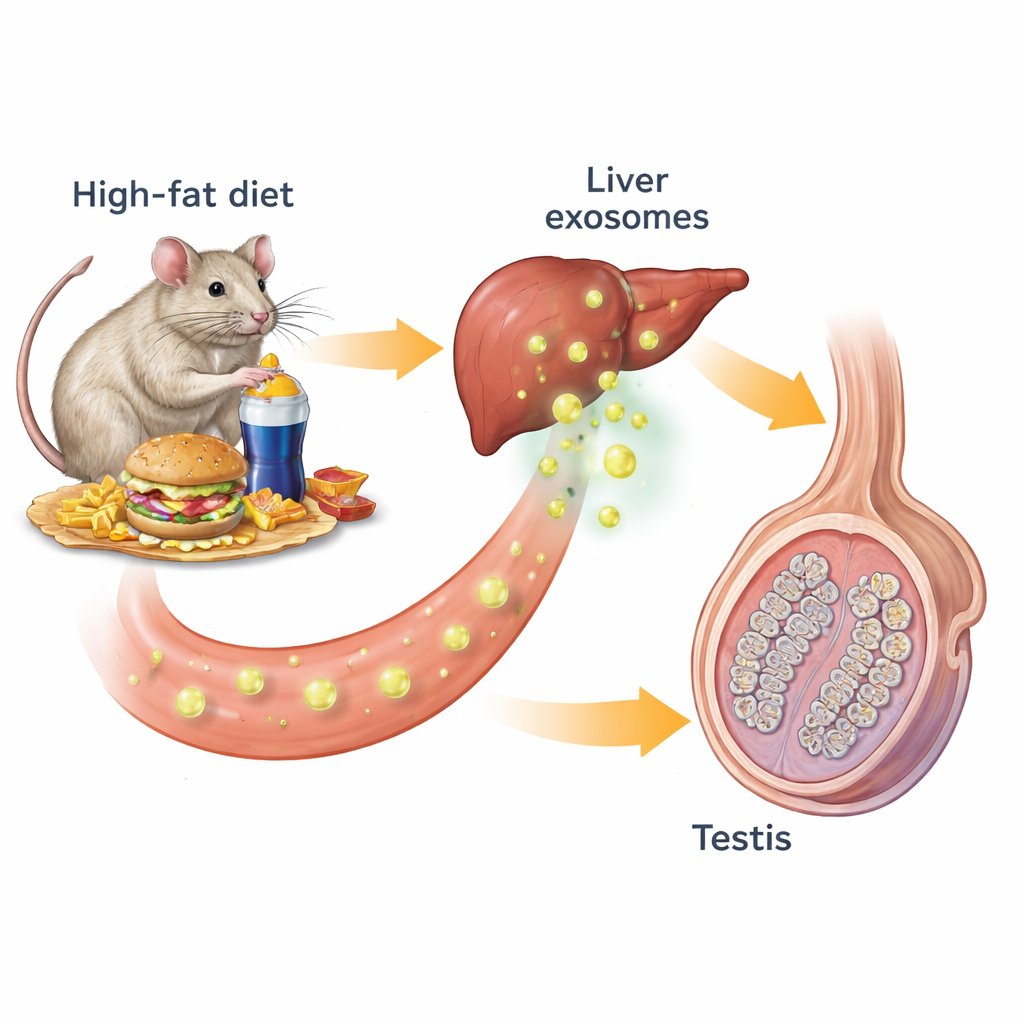
Exosomen verspreiden de schade
Om te testen of circulerende exosomen deze schade helpen veroorzaken, zuiverden de wetenschappers exosomen uit het bloed van obese en magere muizen. Injecteren van exosomen van obese muizen in gezonde, magere muizen was voldoende om veel van de problemen te reproduceren: de ontvangers vertoonden tekenen van metabole problemen, hun testosteronniveaus daalden en hun spermaconcentraties en testisstructuur verslechterden. Het blokkeren van exosoomafgifte bij obese muizen met een middel genaamd GW4869 keerde deze veranderingen grotendeels om, waarbij spermaconcentraties, testosteron en normale testisarchitectuur werden hersteld. Deze resultaten tonen aan dat exosomen in de bloedbaan niet slechts toeschouwers zijn; ze dragen actief schadelijke signalen van obesitas naar het voortplantingssysteem.
Een toxische vorm van celdood
Het team onderzocht vervolgens wat de exosomen precies met Leydigcellen deden. Ze concentreerden zich op ferroptose, een ijzer‑gedreven vorm van celdood die wordt gekenmerkt door ijzerophoping, oxidatieve schade aan vetten en beschadigde mitochondriën—de energiecentrales van de cel. In obese muizen en in gezonde muizen die exosomen van obese dieren kregen, toonden testes hogere niveaus van ijzer en malonaldehyde, een afbraakproduct van vetbeschadiging, evenals duidelijke mitochondriale schade onder de elektronenmicroscoop. Behandeling van obese muizen met een ferroptose‑remmend middel, Ferrostatin‑1, behield Leydigcellen, verhoogde testosteron en spermaconcentraties en verbeterde de mitochondriale gezondheid. In celkweek beschermde hetzelfde middel geïsoleerde Leydigcellen tegen dood en oxidatieve stress geïnduceerd door exosomen van obese dieren. Gezamenlijk laten deze experimenten zien dat ferroptose een sleutelverbinding vormt tussen obesitas en falende testosteronproductie.
Het leverbericht en de SCD2‑schakelaar
Om het bericht binnen exosomen op te sporen, sekveneerden de onderzoekers hun kleine RNA‑lading en vonden dat een specifieke microRNA, miR‑122‑5p, sterk verhoogd was in exosomen van obese muizen. Dit microRNA was vooral overvloedig in de lever en in lever‑afgeleide exosomen, en die leverexosomen konden worden gevolgd terwijl ze naar de testes trokken. Wanneer miR‑122‑5p experimenteel werd verlaagd in exosomen, waren Leydigcellen minder gevoelig voor ferroptose en verbeterde de testosteronproductie, ook al bleven de dieren metabool ongezond. Verdere testen toonden aan dat miR‑122‑5p direct een gen genaamd Scd2 uitschakelt, dat helpt bepaalde vetten om te zetten in vormen die cellen beschermen tegen oxidatieve schade. Het verminderen van Scd2 in Leydigcellen maakte ze kwetsbaarder voor ferroptose en verlaagde testosteron, terwijl het verhogen van Scd2 in obese muizen hormonenspiegels, spermaproductie en mitochondriale structuur gedeeltelijk herstelde. 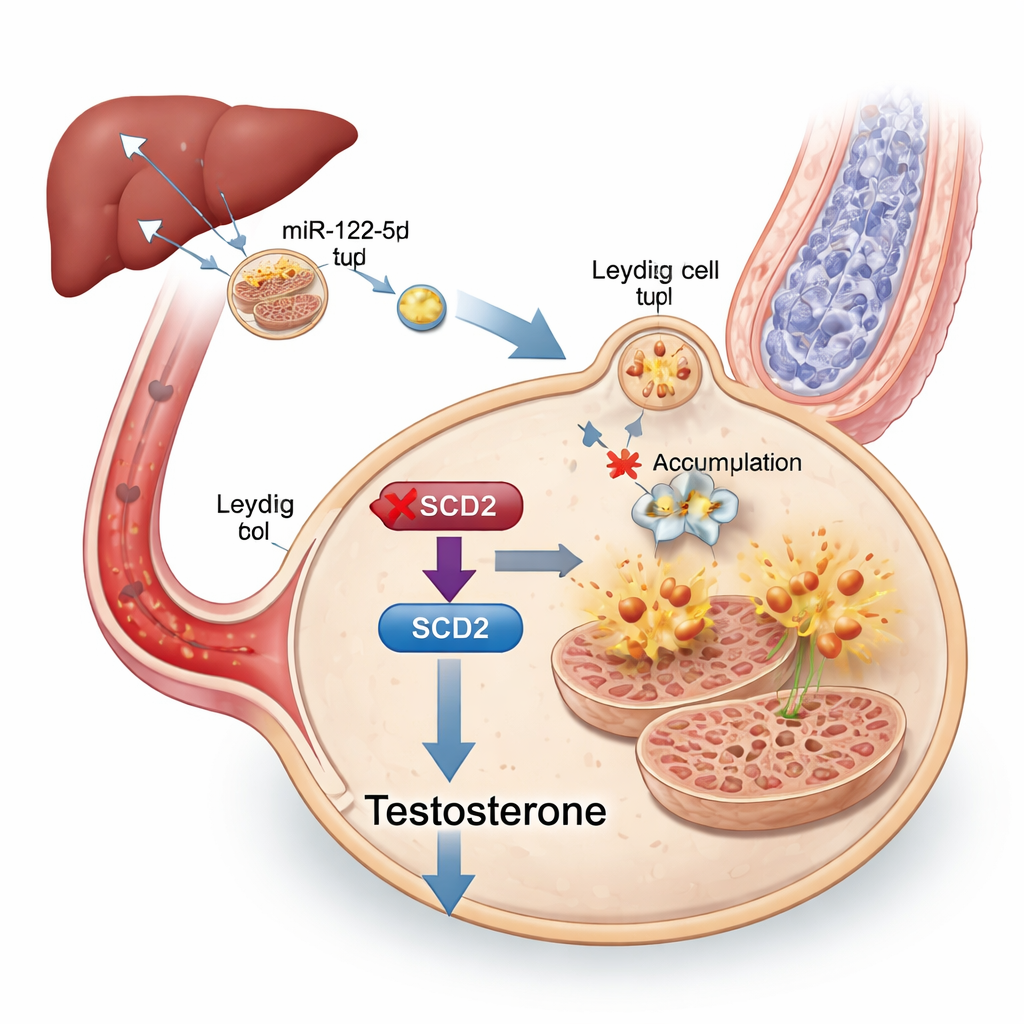
Wat dit betekent voor de menselijke gezondheid
In eenvoudige bewoordingen toont dit werk aan dat een vetrijk dieet de lever ertoe kan aanzetten exosomen te laden met een overmaat aan miR‑122‑5p. Deze exosomen reizen via het bloed naar de testes, waar het microRNA de Scd2 “vetverwerkings”‑schakelaar in Leydigcellen uitzet. Zonder Scd2 hopen deze cellen ijzer‑gedreven oxidatieve schade op, ondergaan ze ferroptose, maken ze minder testosteron en ondersteunen ze uiteindelijk minder gezonde zaadcellen. Hoewel dit onderzoek bij muizen is gedaan en nog bevestigd moet worden bij mensen, identificeert het lever‑afgeleide exosomen, miR‑122‑5p, ferroptose en Scd2 als veelbelovende biomarkers en potentiële medicijntargets voor de behandeling van door obesitas gerelateerde mannelijke onvruchtbaarheid—en benadrukt het weer een reden waarom langjarige vetrijke diëten de voortplantingsgezondheid stilletjes kunnen aantasten.
Bronvermelding: Wang, N., Zhang, B., Chen, T. et al. Obesity impairs spermatogenesis via Leydig cell ferroptosis induced by liver-derived exosomal miR-122-5p. Commun Biol 9, 318 (2026). https://doi.org/10.1038/s42003-026-09612-z
Trefwoorden: obesitas en mannelijke vruchtbaarheid, testosteron, exosomen, Leydigcellen, ferroptose