Clear Sky Science · nl
Herkenning en binding van glycolipiden door Siglec-6 berust op interacties met het celmembraan
Hoe onze cellen vriend van vijand onderscheiden
Het immuunsysteem scant voortdurend onze eigen cellen en beslist wanneer het rustig moet blijven en wanneer het moet aanvallen. Een belangrijk onderdeel van dit toezicht is het herkennen van suikergroepen op celoppervlakken. Deze studie toont aan dat een menselijke immuunreceptor, Siglec-6, niet alleen die suikers gebruikt maar ook het omliggende celmembraan zelf om bijzonder precieze beslissingen te nemen over wat hij bindt. Die ongewone strategie kan helpen verklaren hoe ons lichaam immuunsignalen fijn afstelt en kan nieuwe wegen openen voor gerichte therapieën.
Een suiker‑sensing poortwachter op immuuncellen
Siglecs zijn een familie receptoren die op immuuncellen zitten en siaalzuur‑houdende suikers herkennen, waardoor het immuunsysteem “zelf” van “niet‑zelf” kan onderscheiden. De meeste Siglecs vertrouwen op één, sterk geconserveerd bouwsteen—een arginine‑aminozuur—om zich aan deze suikers vast te hechten. Als die arginine wordt verwijderd, faalt de binding doorgaans. Siglec-6 is echter een buitenbeentje: eerder werk toonde aan dat het nog steeds aan sommige suikerdragende lipiden kan binden, zelfs wanneer deze sleutelarginine gemuteerd is. De nieuwe studie wilde uitzoeken hoe Siglec-6 wegkomt met het schijnbare breken van deze regel en wat dat betekent voor zijn rol op mestcellen, geheugen‑B‑cellen en menselijke placenta‑cellen.
De speciale lipiden waar Siglec-6 naar zoekt
Op celoppervlakken kunnen relevante suikers zowel op eiwitten als op lipiden worden getoond. Dit werk richt zich op een groep suikerdragende lipiden die gangliosiden worden genoemd, met name drie nauw verwante typen: GM1, GM2 en GM3. Alle drie steken ze een enkel siaalzuur‑afgekapte “kop” uit het membraan. Eerdere experimenten toonden aan dat Siglec-6 sterk bindt aan GM1 wanneer het deel uitmaakt van een membraan, maar nauwelijks aan GM2 of GM3, hoewel hun suikerkoppen erg op elkaar lijken. Met gedetailleerde computersimulaties van realistische membranen bevestigden de auteurs dat het siaalzuur in GM1 en GM3 evenzeer blootligt en toegankelijk is. Met andere woorden, simpele fysieke toegankelijkheid verklaart niet waarom GM1 speciaal is. In plaats daarvan bleek een aanvullende suiker aan de top van GM1—het terminale galactose—een cruciale rol te spelen bij het juist positioneren van Siglec-6 tegen het membraan.
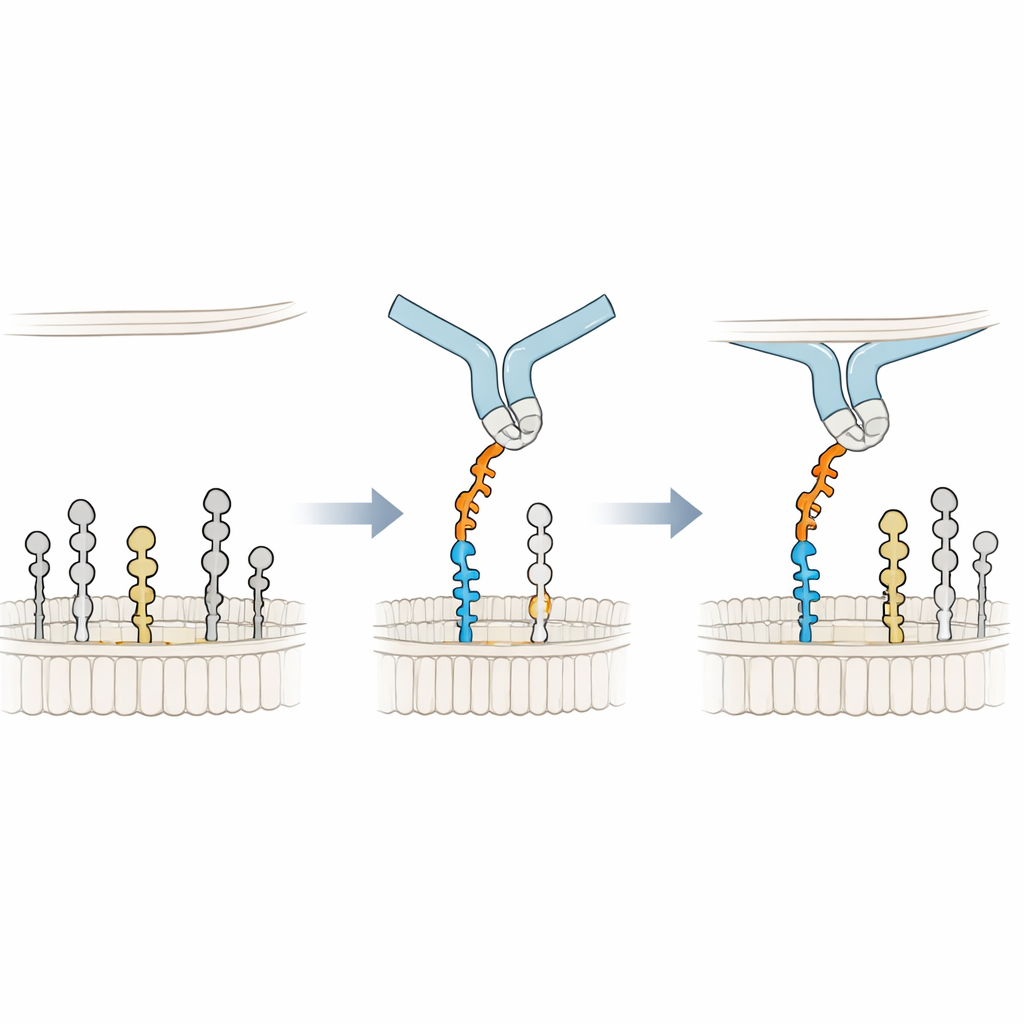
Leunen op het membraan voor een betere greep
Om het bindingsmechanisme op atomair niveau te begrijpen bouwden de onderzoekers 3D‑modellen van Siglec-6 dat GM1 in een membraan benadert en voerden lange moleculaire dynamics‑simulaties uit. Zij vonden dat Siglec-6 nog steeds zijn canonieke arginine (Arg122) gebruikt om contact te maken met het siaalzuur, maar dat dat contact in de tijd aan‑en‑uit flikkert. Wat het complex stabiel houdt is iets nieuws: een nabijgelegen tryptofaan (Trp127) duwt in het vette deel van het membraan, terwijl een aangrenzende lysine (Lys126) interactie aangaat met de geladen kopgroepen van omliggende lipiden. Deze “wig” in het membraan vult de gebruikelijke suiker–arginine‑interactie aan en leent als het ware bindingsenergie uit de lipideomgeving. Wanneer het terminale galactose van GM1 wordt verwijderd om GM2 na te bootsen, zwaait een flexibele lus in Siglec-6 in de lege ruimte, trekt de receptor weg van het membraan en verstoort deze membraan‑ondersteunde greep, wat het verlies van stabiele binding verklaart.
Experimenten die het mechanisme testen
Het team heeft deze computergestuurde inzichten daarna getest in levende celsystemen en biochemische proeven. Ze engineerden cellen om normale of gemuteerde Siglec-6 te expressen en maten hoe goed deze cellen bindden aan fluorescente liposomen en kleine lipidediscs die GM1 droegen. Het muteren van de canonieke arginine verminderde de binding slechts bescheiden wanneer GM1 in een membraan zat, wat bevestigt dat Siglec-6 in die context niet uitsluitend afhankelijk is van dit residu. Daarentegen maakte het muteren van Trp127 de binding aan GM1‑houdende liposomen vrijwel volledig onmogelijk, en het muteren van zowel Trp127 als Lys126 veegde de binding bijna geheel uit. Dezelfde mutants binden echter normaal aan GM1‑achtige suikers die buiten een membraan werden gepresenteerd, wat toont dat de basale structuur van Siglec-6 intact bleef. Native massaspectrometrie toonde verder aan dat Siglec-6 niet alleen aan GM1 kan binden, maar ook aan gewone fosfolipiden, en dat deze lipide‑interactie verdwijnt wanneer Trp127 wordt verwijderd. Opmerkelijk genoeg hecht Siglec-6 zich zelfs aan “naakte” liposomen zonder GM1, opnieuw afhankelijk van Trp127, wat suggereert dat het eerst het membraan kan aftasten en vervolgens vergrendelt wanneer het GM1 tegenkomt.
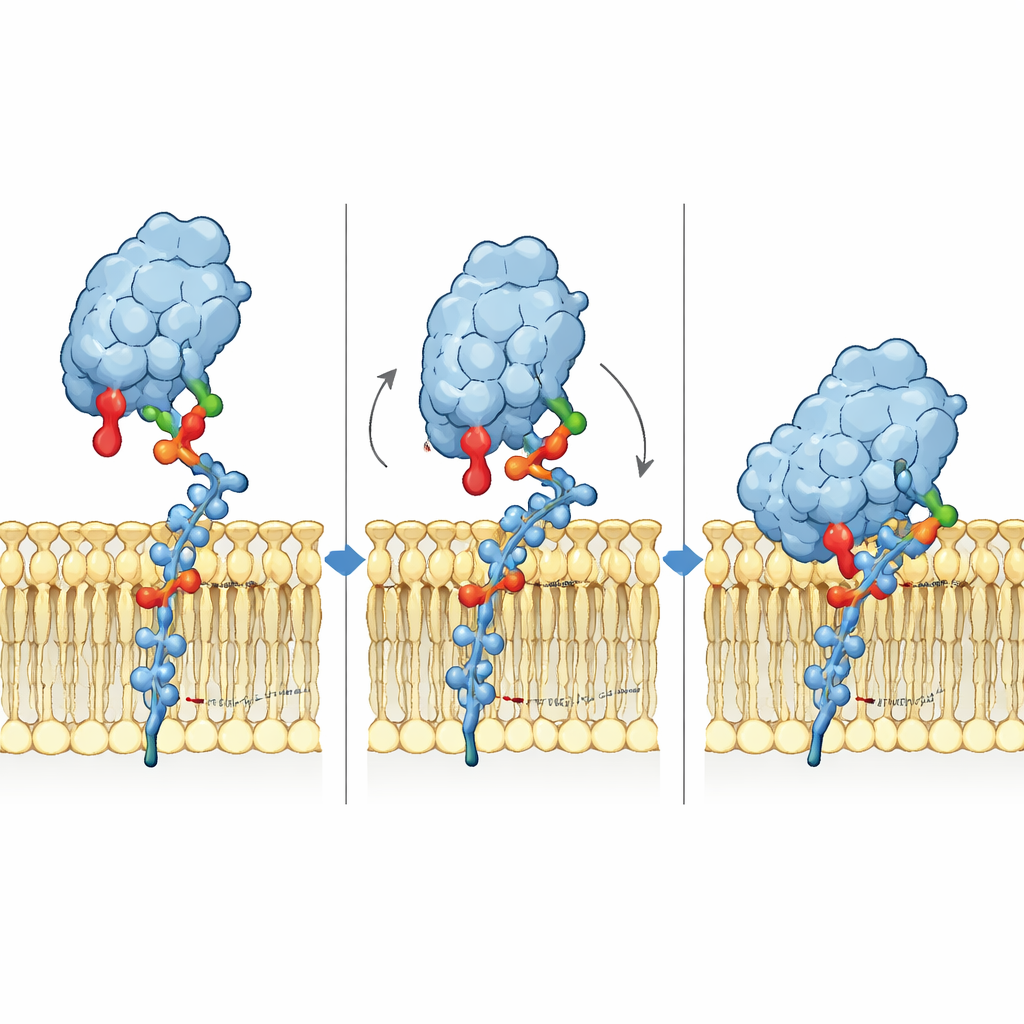
Vrije suikers vertellen een ander verhaal
Wanneer dezelfde drie gangliosiden werden getest als vrijzwevende suikerfragmenten in plaats van als onderdeel van een membraan, gedroeg Siglec-6 zich meer als zijn verwanten. In oplossing bond het zwak en vergelijkbaar aan GM1, GM2 en GM3, en nu was de canonieke arginine essentieel: het muteren van Arg122 verminderde de binding sterk, terwijl het muteren van Trp127 weinig effect had. Dit contrast laat zien dat Siglec-6 effectief van mechanisme wisselt afhankelijk van of het suikers in een membraan of in vrije vorm tegenkomt. In membranen vertrouwt het op een cooperatief partnerschap tussen de suikerkop, het terminale galactose van GM1 en direct membraankontact; in oplossing keert het terug naar het klassieke arginine‑gecentreerde herkenningsmotief.
Waarom dit ertoe doet voor immuuncontrole
Samengevat toont de studie Siglec-6 als een fijn afgestelde sensor die de fysieke context van het membraan gebruikt om zijn specificiteit aan te scherpen. Door zich deels te verankeren in de omliggende lipiden kan het selectief GM1 herkennen tussen zeer vergelijkbare gangliosiden, en verandert een algemene “siaalzuur‑lezer” in een zeer precieze detector van een specifiek oppervlakpatroon. Deze membraan‑ondersteunde strategie lijkt uniek onder de tot nu toe bestudeerde Siglecs en kan Siglec-6 helpen cellen te scannen op specifieke glycolipide‑handtekeningen die immuunreacties reguleren of specifieke weefsels markeren, zoals de menselijke placenta. Begrip van deze dubbele herkenningsmodus kan bijdragen aan het ontwerp van therapieën en diagnostische middelen die gebruikmaken van Siglec-6’s ongewone combinatie van suiker‑ en membraansensing.
Bronvermelding: D’Andrea, S., Schmidt, E.N., Bui, D. et al. Glycolipid recognition and binding by Siglec-6 hinges on interactions with the cell membrane. Commun Biol 9, 333 (2026). https://doi.org/10.1038/s42003-026-09609-8
Trefwoorden: Siglec-6, gangliosiden, celmembraan, herkenning van glycolipiden, immuunregulatie