Clear Sky Science · nl
Geïntegreerde analyse van GWAS en molQTLs onthult celspecifieke genetische varianten in het varkensimmuunsysteem
Waarom varkensimmuniteit ons allemaal aangaat
Varkens voeden een groot deel van de wereld en dienen daarnaast vaak als belangrijke modellen voor mensen in medisch onderzoek. Tegelijk kosten infectieziekten bij varkens boeren jaarlijks miljarden dollars en leiden ze tot intensief antibioticagebruik. In deze studie stellen de onderzoekers een simpele maar krachtige vraag: hoe beïnvloeden kleine DNA-verschillen de werking van varkensimmuuncellen, en kunnen we die effecten terugvoeren tot het gedrag van afzonderlijke celtypen in het bloed? Het begrijpen van die keten van oorzaak en gevolg kan fokstrategieën voor gezondere kuddes sturen en aanwijzingen geven over onze eigen immuunsystemen.
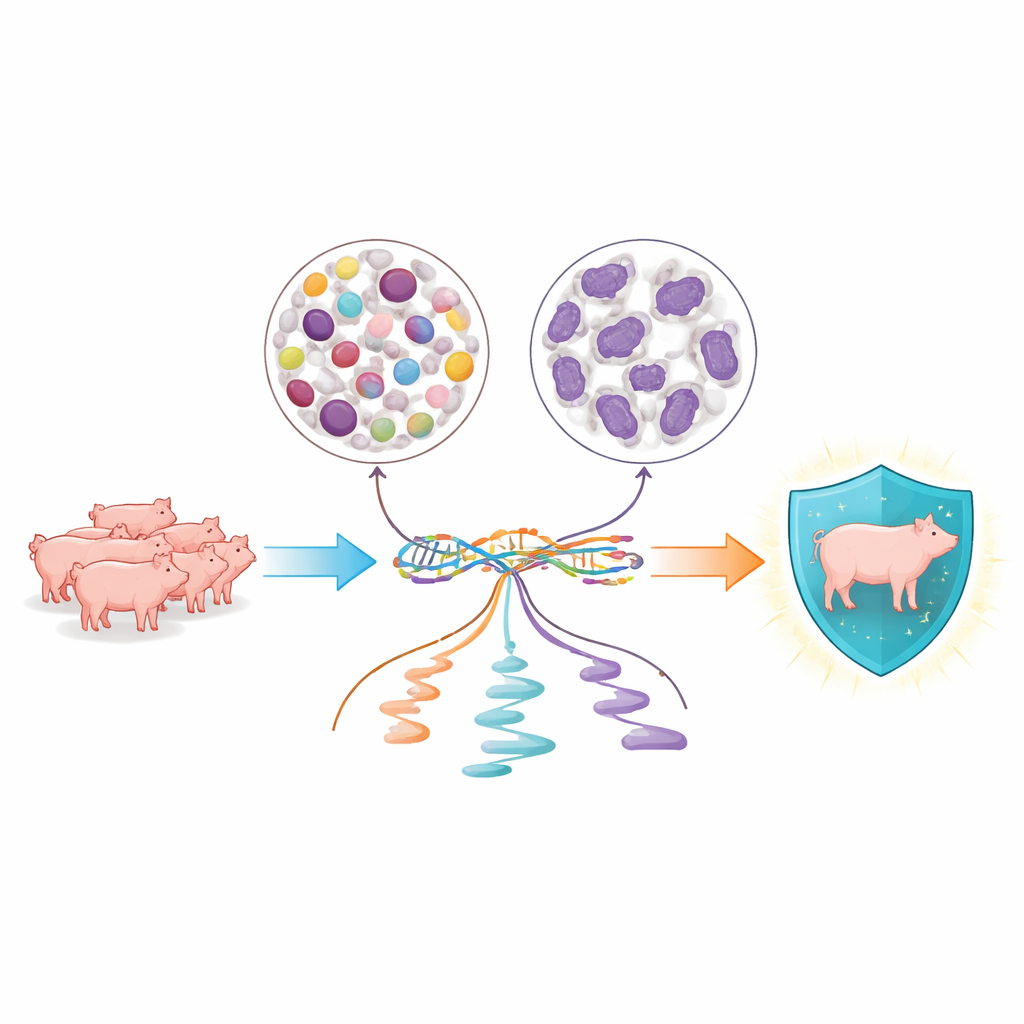
Nauw kijken naar twee belangrijke bloedcelgroepen
De onderzoekers concentreerden zich op twee grote groepen witte bloedcellen die voortdurend het varkensbloed patrouilleren: perifere mononucleaire bloedcellen, waaronder lymfocyten en monocyten die betrokken zijn bij tragere, gerichte verdedigingsreacties, en neutrofielen, die snelle, eerste lijnsaanvallen op microben uitvoeren. Van 134 jonge Yorkshire-varkens zuiverden ze elk celtype afzonderlijk en verzamelden zowel hele-genoom DNA-gegevens als gedetailleerde momentopnames van RNA, de moleculen die genetische instructies binnen cellen dragen. Dit stelde hen in staat niet alleen te zien welke genen aanstonden, maar ook hoe de cel die boodschappen knipte en afwerkte voordat ze werden gebruikt.
DNA-varianten koppelen aan moleculaire schakelaars
In plaats van alleen te kijken welke DNA-varianten met ziektegevoeligheid geassocieerd zijn, brachten de onderzoekers in kaart hoe varianten drie soorten moleculaire kenmerken binnen elk celtype beïnvloeden. Sommige varianten wijzigden hoeveel RNA een gen produceerde. Andere veranderden hoe het RNA werd gespliced, door stukken te trimmen of te herschikken. Een derde klasse verschoof hoe het RNA aan het uiteinde werd afgerond, een proces dat polyadenylering wordt genoemd en de stabiliteit van het bericht kan beïnvloeden. Deze variant–effectparen worden moleculaire kwantitatieve trait-loci genoemd, of molQTLs. De kaarten onthulden duizenden zulke locaties in elk celtype, en opvallend genoeg was meer dan vier vijfde specifiek voor óf de gemengde mononucleaire cellen óf de neutrofielen, wat benadrukt hoe verschillend hetzelfde genoom in diverse immuuncellen kan worden gelezen.
Netwerken vinden die genen koppelen aan immuun-eigenschappen
Om te bekijken hoe deze moleculaire schakelaars zich verhouden tot immuniteit op het niveau van het hele dier, combineerden de wetenschappers de molQTL-kaarten met standaardbloedtests en metingen van immuunsignaalproteïnen. Ze bouwden co-expressienetwerken—groepen genen die samen in expressie toenemen of afnemen—en onderzochten welke netwerken overeenkomen met eigenschappen zoals het aandeel neutrofielen of lymfocyten, het aantal witte bloedcellen, of niveaus van interferonen en tumor necrosefactor. Modules die samenhingen met lymfocytenkenmerken waren verrijkt voor adaptieve immuunroutes, terwijl modules gekoppeld aan neutrofielen snelle aangeboren verdedigingen en inflammatoire signalering benadrukten. Veel sleutelgenen in deze modules werden direct gereguleerd door celspecifieke molQTLs, wat duidelijke trajecten suggereert van DNA-variant naar veranderde celcompositie of -functie.
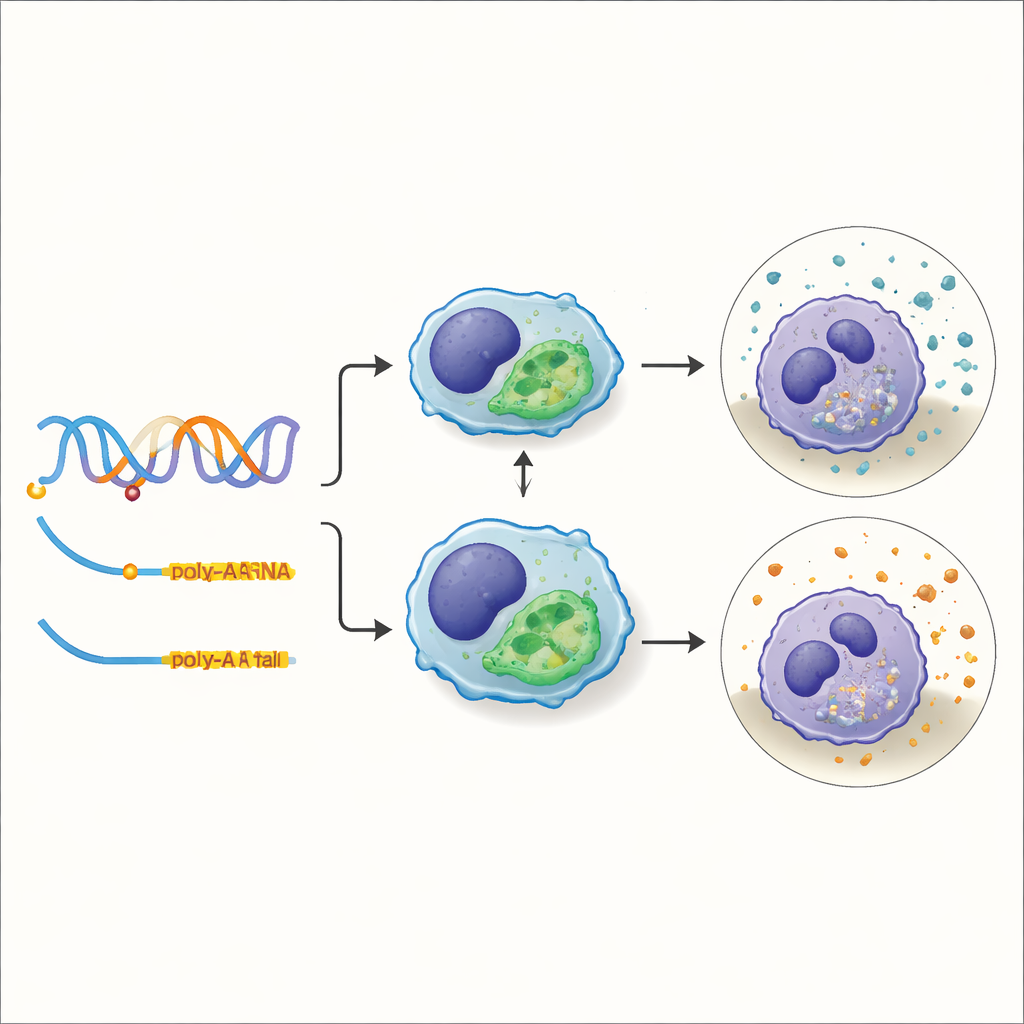
Inzoomen op een variant die de cellulaire "opruim"-capaciteit afstemt
Een van de meest praktische eigenschappen die het team onderzocht, was fagocytische capaciteit—het vermogen van immuuncellen om afval of ziekteverwekkers op te nemen en te verwijderen. Door hun molQTLs te overlappen met resultaten van eerdere genome‑wide association studies voor fagocytose, identificeerden ze 588 regio’s waar dezelfde DNA-verandering vermoedelijk zowel een moleculaire verschuiving als een verandering in cellulaire opruimprestatie veroorzaakt. Een opvallend voorbeeld was een variant binnen een gen genaamd TXNDC15. Deze verandering schakelde het gen niet simpelweg aan of uit; in plaats daarvan beïnvloedde het welke polyadenyleringsplaats de cel voor het RNA van dat gen koos. Varkens met één versie van de variant gaven de voorkeur aan een kortere staart op het RNA, dat daardoor stabieler bleek en in hogere hoeveelheden ophoopte, en deze dieren toonden sterkere fagocytische activiteit in hun immuuncellen.
Wat dit betekent voor gezondere varkens en meer
Simpel gezegd laat dit werk zien hoe kleine DNA-verschillen de "instructies" binnen specifieke immuunceltypen kunnen herschakelen en daarmee kunnen beïnvloeden hoeveel van die cellen aanwezig zijn en hoe goed ze hun taken uitvoeren. Door celtypen zorgvuldig te scheiden en niet alleen de genactiviteit te volgen maar ook hoe boodschappen worden geknipt en afgewerkt, onthult de studie verborgen regelpunten die onderzoeken op bulkweefsel missen. De resulterende genetische kaart biedt een fundament voor het fokken van varkens die van nature beter bestand zijn tegen ziekten, wat mogelijk het antibioticagebruik kan verminderen. Tegelijkertijd, omdat de immuunfunctie van varkens sterk op die van mensen lijkt, kunnen deze inzichten onderzoekers ook helpen begrijpen hoe soortgelijke mechanismen werken in de menselijke gezondheid en ziekte.
Bronvermelding: Yang, J., Chen, S., Tang, Y. et al. Integrated analysis of GWAS and molQTLs reveals cell-specific genetic variants in the porcine immune system. Commun Biol 9, 408 (2026). https://doi.org/10.1038/s42003-026-09605-y
Trefwoorden: varkensimmuniteit, genetische varianten, immuuncellen, fagocytose, moleculaire QTLs