Clear Sky Science · nl
Remming van ATM Verhoogt Knock-in-efficiëntie door AAV-geïnduceerde Activatie van Apoptotische Routes te Onderdrukken
Genbewerking effectiever maken
CRISPR-genbewerking belooft behandelingen voor genetische aandoeningen, sterkere gewassen en krachtige onderzoekstools. Maar een van de meest waardevolle trucs—precies nieuw DNA op een gekozen plaats in het genoom invoegen, bekend als een “knock-in”—werkt nog steeds inefficiënt. Deze studie onderzoekt waarom sommige cellen nieuwe DNA makkelijker accepteren dan andere en onthult een manier om cellen vaker nauwkeurige bewerkingen te laten uitvoeren, vooral bij gebruik van adeno-geassocieerd virus (AAV), een toonaangevende vector voor gentherapie.
DNA-herstel realtime volgen
Om te begrijpen wat precieze DNA-insertie bevordert of belemmert, bouwden de onderzoekers een verfijnd “dashboard” in muis-embryonale stamcellen. Dit drievoudige reportersysteem gebruikt drie fluorescerende merkers om in dezelfde cellen bij te houden of CRISPR het DNA heeft geknipt, of er een precieze knock-in heeft plaatsgevonden, en of de cel in plaats daarvan het donor-DNA op een ruwere manier heeft ingelast. Door verschillende kleurcombinaties met flowcytometrie uit te lezen, konden ze zuivere, sjabloon-gebaseerde bewerkingen scheiden van foutgevoelige inserties en onbewerkte cellen. Deze gelijktijdige tracking stelde hen in staat te kaart te brengen hoe verschillende DNA-herstelroutes aan elk resultaat bijdragen met veel hogere resolutie dan oudere PCR-gebaseerde testen.
Twee DNA-hulpen, twee zeer verschillende reacties
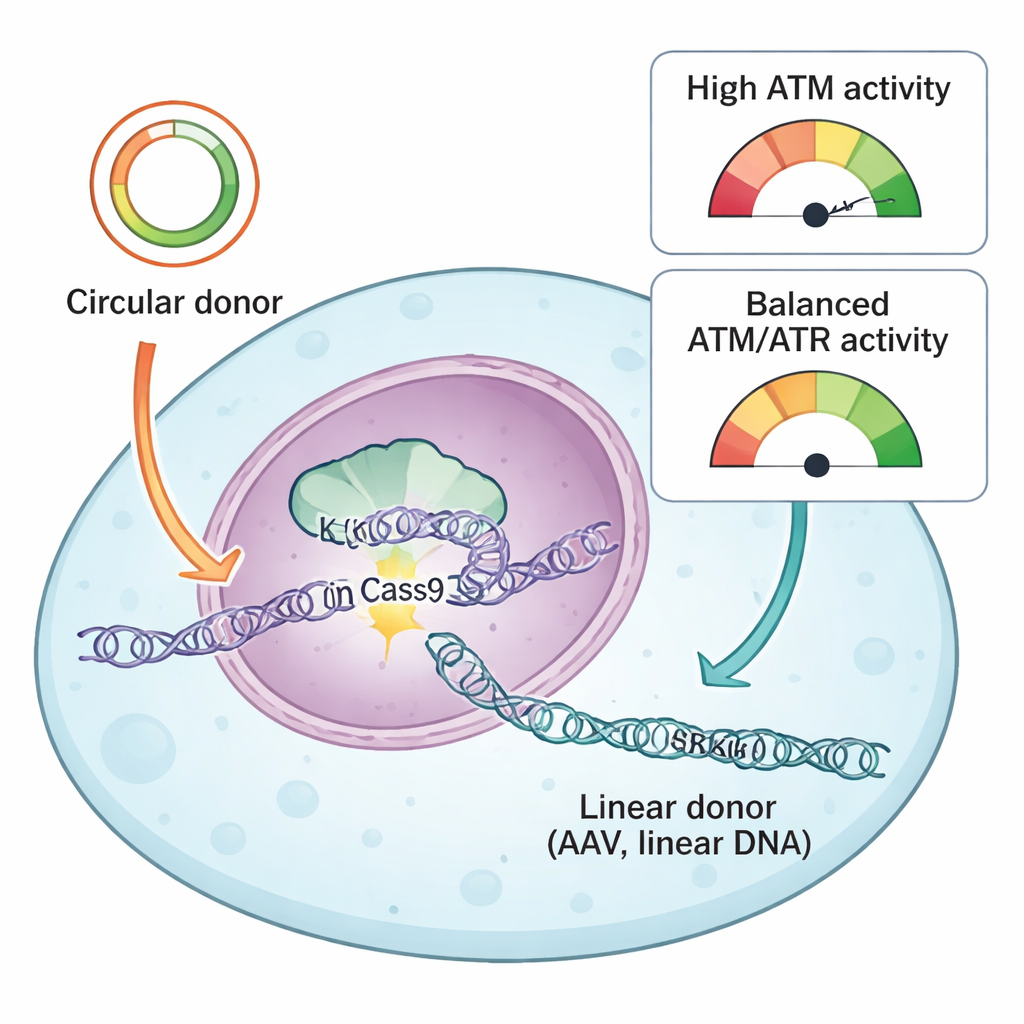
Het team vergeleek twee veelvoorkomende typen donor-DNA die CRISPR-reparaties sturen: circulaire plasmiden en lineair AAV-afgeleid DNA. Beide dragen overeenkomende “homologiearmen” die de cel vertellen waar de nieuwe sequentie moet worden ingevoegd, maar ze komen de cel binnen in verschillende fysieke vormen. Circulaire plasmiden zijn gesloten lussen van dubbelstrengs DNA, terwijl AAV-donoren meestal binnenkomen als enkellijnige lineaire moleculen. Met hun reportersysteem en een bibliotheek van remmers die eiwitten van de DNA-schaderespons targeten, vonden de auteurs dat één sleutelproteïne, ATR, uniform essentieel was voor succesvolle knock-ins met beide donortypen. Remming van ATR verminderde de precieze insertie sterk, terwijl het zachtjes stimuleren van ATR-activiteit via een KEAP1–NRF2-route knock-ins efficiënter maakte, vooral bij AAV-donoren.
Wanneer DNA-bescherming averechts werkt
Een andere sensor van DNA-schade, ATM, bleek opvallend afhankelijk van het donortype te reageren. Bij circulaire plasmide-donoren verminderde blokkade van ATM zowel precieze knock-in als end-joining-gemedieerde inserties, wat past bij zijn klassieke rol in het helpen van cellen bij het repareren van dubbelstrengsbreuken. Maar bij lineair DNA—of dat nu van AAV, zelf-complimentair AAV of plasmiden die in rechte stukken zijn geknipt kwam—had ATM-remming het tegenovergestelde effect: het verhoogde de knock-in-efficiëntie. De onderzoekers traceerden dit effect tot hoe cellen pieken van lineair DNA interpreteren. Hoge doses AAV activeerden ATM sterk, wat op zijn beurt p53 en caspase 3 inschakelde, centrale spelers in geprogrammeerde celdood. Cellen die veel kopieën van het donor-DNA hadden opgenomen, en dus de grootste kans op een succesvolle knock-in, werden ook het meest waarschijnlijk gedood door dit waarschuwingssysteem.
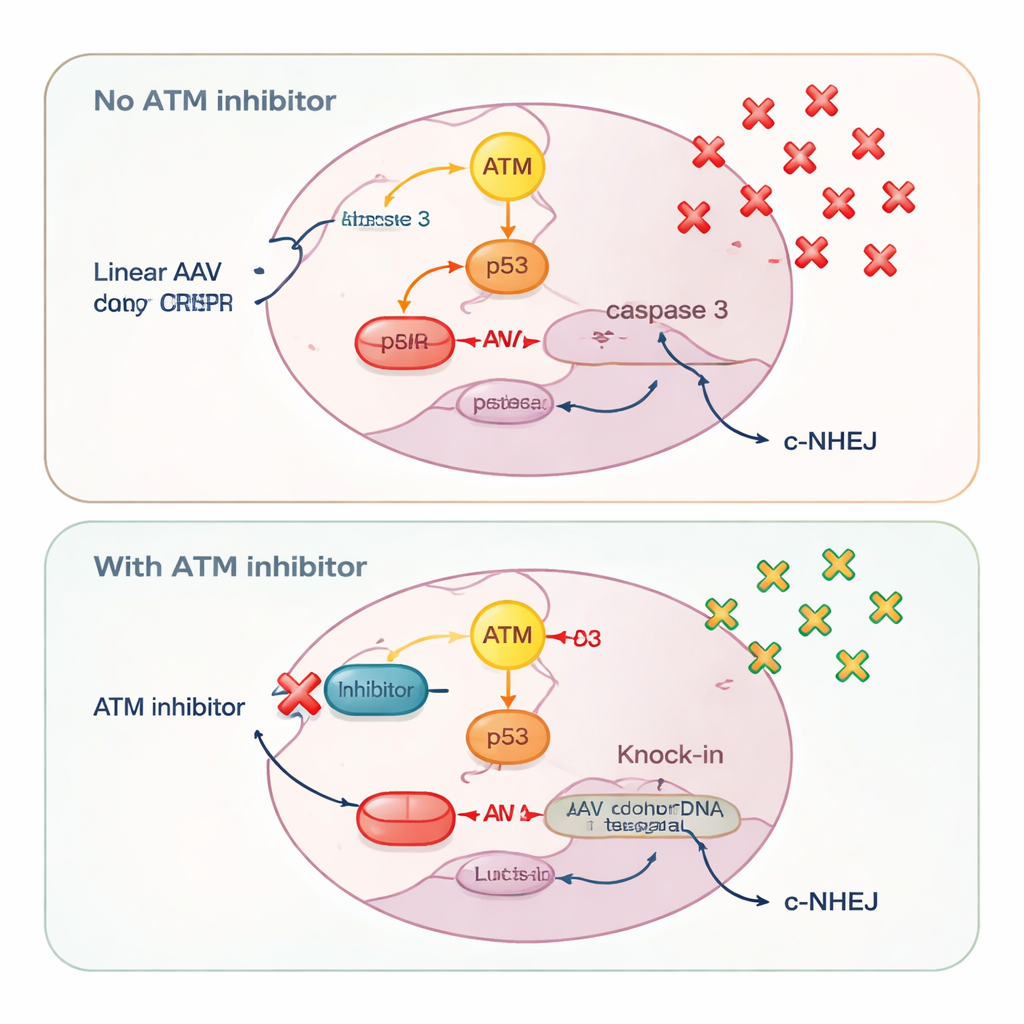
De best uitgeruste cellen redden
Door ATM-remmers toe te voegen, dempten de wetenschappers de ATM–p53–caspase 3‑doodroute. Dit spaarde cellen die grote hoeveelheden donor-DNA droegen, waardoor meer van hen lang genoeg overleefden om een precieze knock-in te voltooien. Metingen van virale genoomkopieën bevestigden dat ATM-remming het aantal AAV-moleculen dat in cellen werd behouden verhoogde. Tegelijk verzwakte ATM-blokkade lichtelijk een snelle, botste reparatieroute die klassieke non-homologe end-joining wordt genoemd, zoals bleek uit verminderde activatie van DNA-PK, een kernenzym in die route. Het verzwakken van deze concurrerende hersteloptie duwde meer CRISPR‑sneden richting homologie-gebaseerde knock-in in plaats van snelle lapmiddelen die het donor-sjabloon negeren.
Wat dit betekent voor toekomstige gentherapieën
Voor niet‑specialisten is de boodschap dat dezelfde cellulaire beschermmechanismen die ons tegen DNA‑schade behoeden, per ongeluk precieze genbewerking kunnen ondermijnen, vooral wanneer grote hoeveelheden viraal donor‑DNA worden gebruikt. Dit werk laat zien dat het zachtjes afstemmen van die beschermingen—ATR actief houden maar tijdelijk ATM terughouden wanneer lineaire donoren zoals AAV aanwezig zijn—CRISPR knock-ins betrouwbaarder en efficiënter kan maken. Zo’n strategie zou gentherapieën, celengineering en ziekte‑modellen kunnen verbeteren door meer cellen de gewenste wijziging te laten accepteren en onnodig celverlies te vermijden.
Bronvermelding: Natsagdorj, ME., Hara, H., Uosaki, H. et al. ATM Inhibition Enhances Knock-in Efficiency by Suppressing AAV-Induced Activation of Apoptotic Pathways. Commun Biol 9, 177 (2026). https://doi.org/10.1038/s42003-026-09604-z
Trefwoorden: CRISPR knock-in, AAV-gene-editing, DNA-schaderespons, ATM-remming, genoomtechniek