Clear Sky Science · nl
DTX1-gemedieerde afbraak van TUBB3 in Kupffercellen verlaagt de progressie van hepatocellulair carcinoom door M1/M2-polarisatie te reguleren
Waarom de immuun-"buren" van leverkanker ertoe doen
De meeste mensen zien kanker als een ziekte van dwalende cellen die ongecontroleerd groeien. Maar tumoren leven in een drukke omgeving van immuuncellen, bloedvaten en ondersteunend weefsel die óf de kanker bestrijden óf haar stilletjes helpen groeien. Deze studie richt zich op leverkanker—specifiek hepatocellulair carcinoom—en onthult hoe een eiwit in gespecialiseerde leverimmuuncellen de balans kan doen doorslaan tussen een anti-kankerreactie en een tumorvriendelijke omgeving. Inzicht in deze verborgen schakelaar kan nieuwe wegen openen om bestaande immunotherapieën te verbeteren.
Een leverkanker gestuurd door zijn omgeving
De lever is rijk aan immuuncellen, waaronder een resident-populatie genaamd Kupffercellen die normaal helpen het orgaan gezond te houden. Bij leverkanker transformeren veel van deze cellen in tumor-geassocieerde macrofagen die ofwel de kanker aanvallen (een M1-achtig stadium) of haar beschermen (een M2-achtig stadium). Patiënten wiens tumoren vol zitten met M2-type macrofagen doen het doorgaans slechter en reageren vaak slecht op middelen die de immuunremmen opheffen, zoals PD-1-remmers. De auteurs begonnen met het doorzoeken van openbare genenbanken en patiëntmonsters op zoek naar moleculen die zowel met leverkanker als met deze macrofagen geassocieerd zijn, en kwamen uit bij een structureel eiwit genaamd TUBB3 dat onverwacht overvloedig aanwezig was in tumorweefsel.
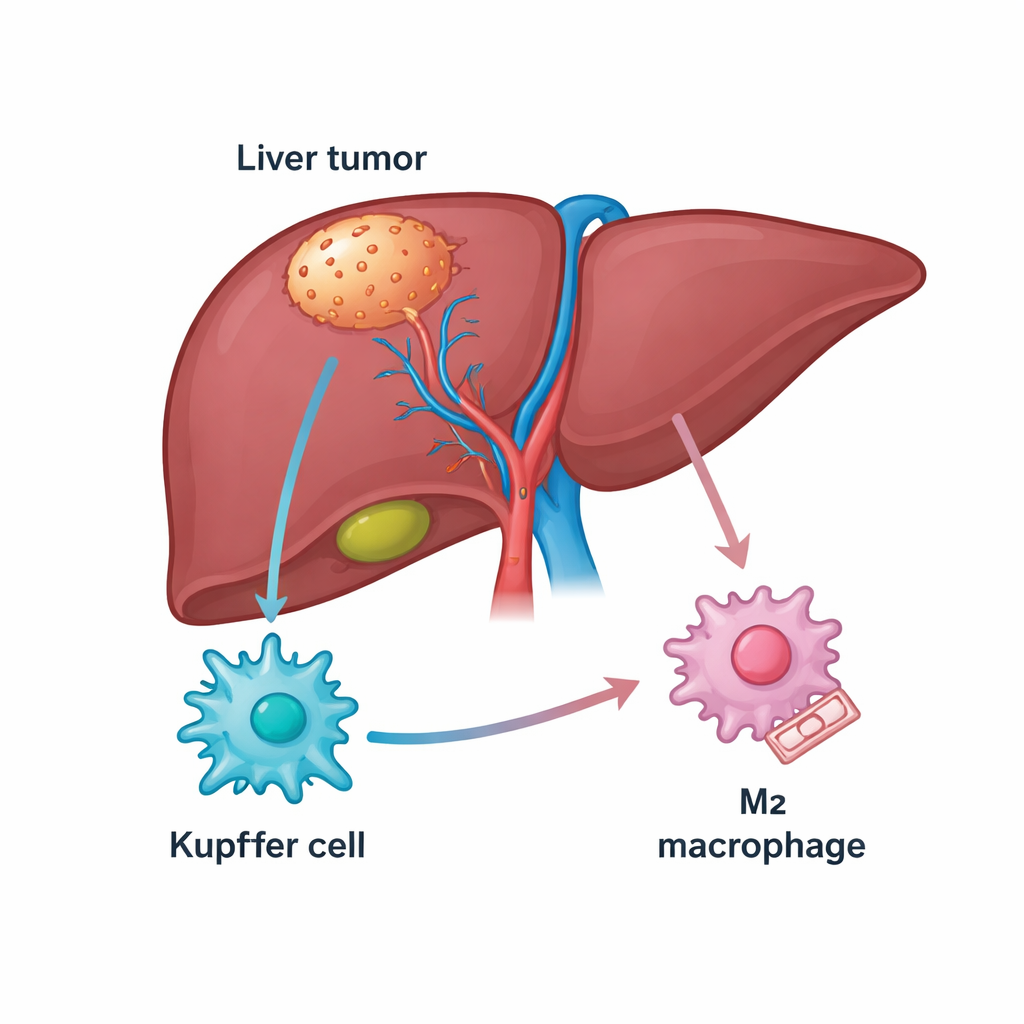
Een verrassend eiwit dat immuuncellen ertoe brengt tumoren te helpen
TUBB3 staat vooral bekend als een bouwsteen van microscopische “rails” in cellen, maar is ook in verband gebracht met agressief gedrag en medicijnresistentie in verschillende kankers. Hier vonden de onderzoekers dat TUBB3-niveaus veel hoger waren in levertumoren dan in aangrenzend gezond weefsel, en dat patiënten met meer TUBB3 doorgaans kortere overleving hadden. Met kleuringstechnieken toonden ze aan dat TUBB3 vooral verrijkt was in Kupffercellen binnen tumoren, en dat de aanwezigheid ervan sterk samenhing met markers van de tumor-ondersteunende M2-toestand. Met andere woorden: Kupffercellen vol TUBB3 gedroegen zich vaker op manieren die de immuunaanval dempen en kankergroei ondersteunen.
Macrofagen herprogrammeren om levertumoren te remmen
Om oorzaak en gevolg te testen verlaagde het team TUBB3-niveaus in Kupffercellen in laboratoriumexperimenten. Toen TUBB3 werd onderdrukt, produceerden deze cellen minder M2-achtige signalen, meer M1-achtige signalen en scheidden ze minder moleculen uit die normaal immuunactiviteit onderdrukken. Leverkankercellen die werden blootgesteld aan deze hergeprogrammeerde macrofagen groeiden langzamer, deelden minder en waren minder in staat te migreren en te invaseren. Bij muizen leidde het mengen van levertumorcellen met TUBB3-deficiënte Kupffercellen tot kleinere tumoren, meer kankerceldood en een grotere toestroom van dodelijke CD8 T-cellen bewapend met destructieve eiwitten. Als macrofagen volledig uit de dieren werden verwijderd, verdween het voordeel van het blokkeren van TUBB3 grotendeels, wat benadrukt dat het effect via deze immuuncellen loopt en niet alleen via de kankercellen.
Het blootleggen van een interne rem op een belangrijke signaalweg
De studie onderzocht ook hoe TUBB3 deze invloed uitoefent. De auteurs concentreerden zich op een goed bekende groeien overlevingsweg die wordt gereguleerd door de eiwitten PTEN en AKT, en die ook bepaalt of macrofagen een M1- of M2-identiteit aannemen. Ze ontdekten dat het verlagen van TUBB3 PTEN verhoogde, wat op zijn beurt de activerende “fosfaatlabels” op AKT verminderde en de macrofagen richting de tumorbestrijdende toestand duwde. Wanneer ze AKT kunstmatig herkoppelden, keerden macrofagen terug naar het M2-patroon en kregen kankercellen hun agressieve gedrag terug, zelfs zonder TUBB3. Dit plaatst TUBB3 stroomopwaarts van PTEN en AKT als een soort interne draaiknop voor macrofaaggedrag.
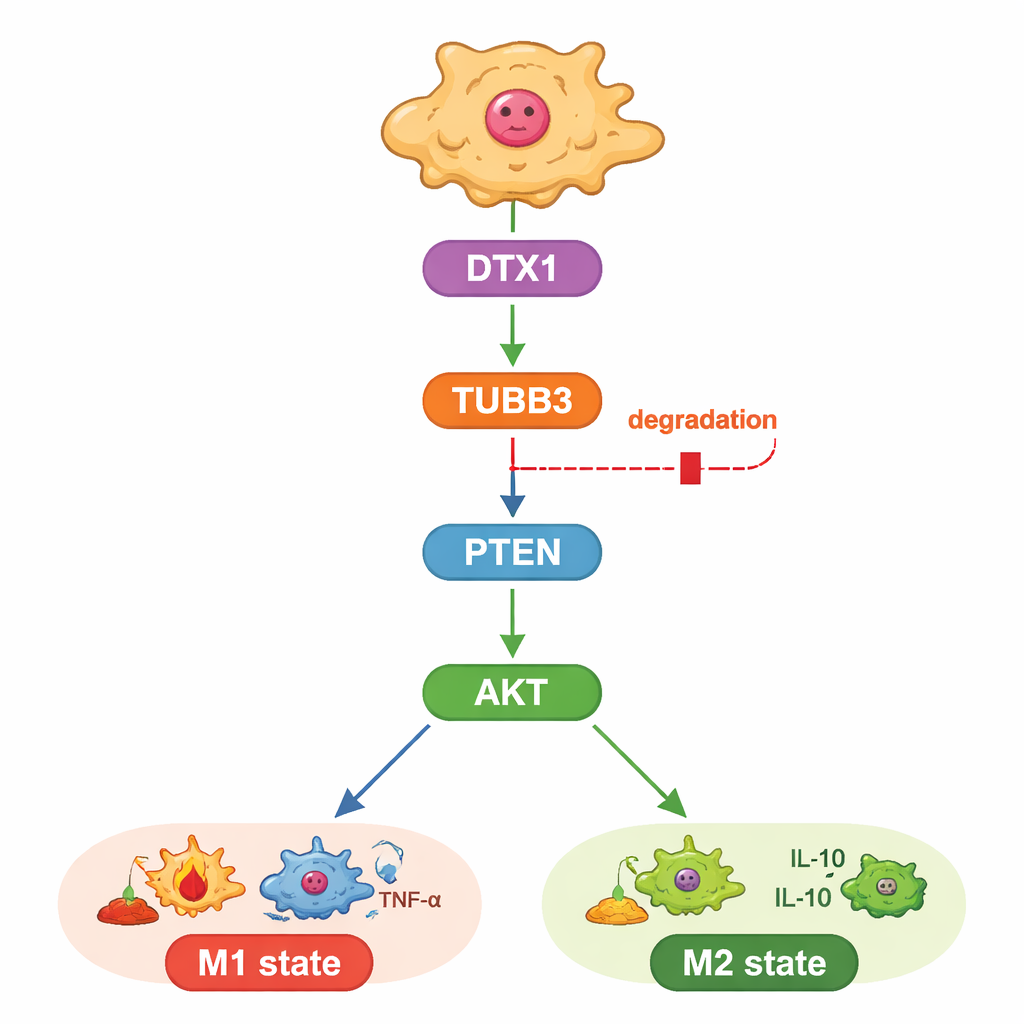
Een ingebouwd vuilnislabel dat weer aangezet kan worden
Tenslotte vroegen de onderzoekers zich af waarom TUBB3 zo overvloedig is in levertumoren. Door bioinformatische voorspellingen te combineren met expressiegegevens identificeerden ze een enzym genaamd DTX1, onderdeel van een familie die eiwitten markeert voor afbraak, als een waarschijnlijke regulator. DTX1-niveaus waren lager in levertumoren dan in gezond weefsel en stonden in verband met betere patiëntuitkomsten en een grotere aanwezigheid van M1-type macrofagen. In cellen versnelde het verhogen van DTX1 de afbraak van TUBB3, dempte AKT-activiteit en duwde macrofagen naar de tumorbestrijdende staat, waardoor de groei van kankercellen werd beperkt. Het opnieuw invoeren van extra TUBB3 tilde deze voordelen van DTX1 opzij, zowel in kweek als in muizentumoren. Samen tekenen deze resultaten een duidelijke lijn van DTX1 via TUBB3 en PTEN/AKT naar de immuuntoon van de tumor.
Wat dit betekent voor toekomstige behandeling van leverkanker
Voor niet-specialisten is de kernboodschap dat dit werk een eerder verborgen controlesysteem in lever-residente immuuncellen identificeert dat bepaalt of ze de kanker helpen of tegenwerken. Wanneer het vuilnis-label-enzym DTX1 laag is, hoopt TUBB3 zich op, wordt een groeipathway geactiveerd en glijden Kupffercellen in een tumorondersteunende modus die het effect van immunotherapie verzwakt. Het herstellen van deze route—door TUBB3 te verlagen, DTX1 te verhogen of het PTEN/AKT-signaal zorgvuldig bij te stellen—zou lokale immuunverdediging kunnen heractiveren en behandelingen zoals PD-1-remmers effectiever kunnen maken. Hoewel dergelijke strategieën nog experimenteel zijn, onderstrepen ze de belofte van het behandelen niet alleen van de tumorcellen, maar ook van de omliggende immuun-"buren" die sterk bepalen hoe leverkanker zich gedraagt.
Bronvermelding: Sun, J., Sun, T., Zhang, Y. et al. DTX1-mediated degradation of TUBB3 in Kupffer cells mitigates hepatocellular carcinoma progression by regulating M1/M2 polarization. Commun Biol 9, 311 (2026). https://doi.org/10.1038/s42003-026-09593-z
Trefwoorden: hepatocellulair carcinoom, tumor-geassocieerde macrofagen, Kupffercellen, immunotherapie, AKT-signaaltransductie