Clear Sky Science · nl
Transiënte proliferatie door omkeerbare YAP- en mitogenencontrole van de cycline D1/p27-verhouding
Hoe weefsels weten wanneer ze moeten groeien
Als je huid snijdt of een orgaan beschadigt, schakelen nabije cellen tijdelijk van een rusttoestand naar een herstelfase en delen ze zich net genoeg om de wond te dichten voordat ze weer stoppen. Dit artikel stelt een bedrieglijk eenvoudige vraag: hoe weten cellen wanneer ze moeten beginnen en, even belangrijk, wanneer ze moeten stoppen met delen zodat genezing plaatsvindt zonder overmatige, kankerachtige groei? De onderzoekers onthullen een ingebouwde balans in cellen die een krachtig groeisignaal slechts tijdelijk inschakelt en daarna op betrouwbare wijze weer uitzet.
Een stoplicht voor celdeling
In veel weefsels werkt een moleculair systeem dat Hippo–YAP heet als een verkeersregelaar voor celgroei. Wanneer weefsels druk bezet en intact zijn, houdt Hippo een eiwit genaamd YAP buiten de kern en blijven cellen in rust. Wanneer weefsel beschadigd raakt of uitgerekt wordt, ontspant Hippo, verhuist YAP naar de kern en krijgen cellen een duwtje om te delen. De auteurs bestudeerden duizenden individuele epitheelcellen die als platte vellen gekweekt werden en stelden ze bloot aan verschillende combinaties van groeifactoren (mitogenen), geneesmiddelen en cel-dichtheden. Ze vonden dat groeifactor-signalen, fysieke druk en YAP-activiteit niet onafhankelijk werken; in plaats daarvan komen ze samen op één intern beslissingspunt dat bepaalt of elke cel de celcyclus opnieuw ingaat.
De sleutelverhouding binnenin de cel
De centrale bevinding is dat cellen besluiten te delen op basis van de verhouding tussen twee eiwitten in de kern tijdens de vroege groeifase G1. Het ene eiwit, cycline D1, duwt de cel richting deling; het andere, p27, werkt als rem. Het is niet de absolute hoeveelheid van een van beide eiwitten die telt, maar de cycline D1/p27-verhouding. Wanneer deze verhouding boven een kritische drempel uitkomt, wordt een poortwachterseiwit genaamd Rb gefosforyleerd en laat het de machinerie voor DNA-replicatie los, waardoor de cel verder kan. Onder die drempel blijft de cel in rust. Het team toonde aan dat kunstmatige activatie van YAP, of het blokkeren van remmen hogerop in de Hippo-route, consequent de cycline D1/p27-verhouding verhoogde en cellen over deze drempel dreef, zelfs onder omstandigheden die normaal gesproken cellen stilhouden.
Hoe signalen van buiten worden versterkt en daarna vervagen
YAP werkt niet alleen: het vergroot de gevoeligheid van de cel voor groeisignalen van buitenaf. De onderzoekers gebruikten RNA-sequencing en eiwitmetingen om aan te tonen dat YAP het aantal en de activiteit van receptor-eiwitten aan het celoppervlak verhoogt, waaronder leden van de EGFR-familie en andere receptor-tyrosinekinasen. Deze receptoren voeden klassieke groeipaden zoals MEK–ERK en, in mindere mate, mTOR, die cycline D1 verhogen en p27 verlagen om de interne verhouding richting deling te kantelen. Belangrijk is dat deze versterking geen snelle aan/uit-schakelaar is. Zelfs nadat YAP-activiteit is geblokkeerd, nemen het verhoogde receptor-signaal en de verhoogde cycline D1/p27-verhouding slechts langzaam af over vele uren, waardoor cellen de tijd krijgen een beperkte ronde deling te voltooien voordat de remmen volledig worden hersteld.
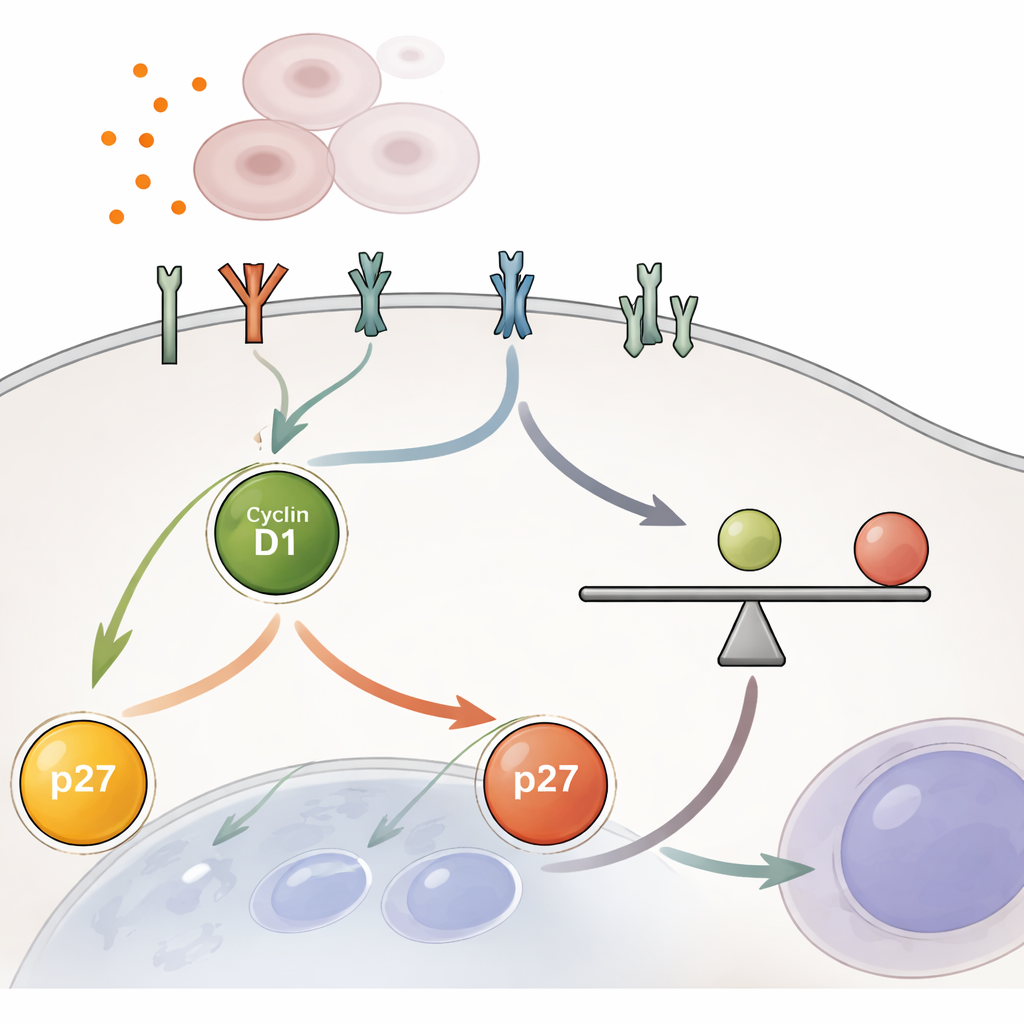
Ingebouwde waarborgen tegen ongeremde groei
De studie onderzoekt ook wat er gebeurt wanneer natuurlijke remmen op YAP verzwakt zijn, zoals in sommige tumoren. Het uitschakelen van een junctie-eiwit genaamd Merlin, dat normaal helpt Hippo te activeren, liet YAP deels los en maakte cellen gevoeliger voor groeifactoren. Toch konden zelfs deze cellen worden stilgelegd door zeer hoge lokale celdichtheid, wat de contactremming herstelde en de cycline D1/p27-verhouding verlaagde. Dit toont aan dat het systeem meerdere controlelagen heeft: oppervlakte-receptoren, Hippo–YAP en de cycline D1/p27-verhouding dragen allemaal bij aan de beslissing of cellen doorgaan met delen.
Waarom dit ertoe doet voor genezing en kanker
Voor een algemeen publiek is de belangrijke boodschap dat weefselherstel wordt aangestuurd door een transiënt, zichzelf limiterend groeiprogramma. YAP-activatie en verhoogde receptor-signalisatie tillen de cycline D1/p27-verhouding boven een drempel zodat cellen kunnen delen en schade kunnen herstellen. Naarmate cellen delen en het weefsel weer voller wordt, schakelt contactremming geleidelijk YAP en receptor-signalen uit, daalt de verhouding en stopt de deling. Wanneer dit timingmechanisme wordt verbroken — bijvoorbeeld door aanhoudende YAP-activatie of verlies van remmen hogerop — kunnen cellen ongevoelig worden voor dichtheid en door blijven delen, een stap richting kanker. Inzicht in dit op verhoudingen gebaseerde beslissingssysteem kan helpen bij het ontwerpen van regeneratieve therapieën die herstel veilig versterken zonder ongecontroleerde groei te ontketenen.
Bronvermelding: Ferrick, K.R., Upadhya, S.W., Fan, Y. et al. Transient proliferation by reversible YAP and mitogen control of the cyclin D1/p27 ratio. Commun Biol 9, 340 (2026). https://doi.org/10.1038/s42003-026-09590-2
Trefwoorden: YAP-signaaltransductie, celcycluscontrole, weefselregeneratie, contactremming, cycline D1 p27-balans