Clear Sky Science · nl
Structurele inzichten in WRN-helicase tonen conformationele toestanden en kansen voor medicijnontwikkeling tegen MSI‑H-kanker
Waarom dit belangrijk is voor kankerbehandeling
Bepaalde kankers hebben een ingebouwde zwakte: ze kunnen fouten in hun DNA slecht repareren. Een eiwit dat WRN‑helicase heet fungeert als een moleculair reparatiegereedschap dat deze kwetsbare tumoren in leven houdt. Deze studie onthult, op atomaire schaal, hoe WRN langs DNA beweegt en hoe experimentele geneesmiddelen die beweging kunnen blokkeren — en biedt daarmee een routekaart voor nieuwe behandelingen die deze gevoelige kankercellen selectief doden terwijl gezond weefsel gespaard blijft.
De DNA‑klusjesman onder de microscoop
WRN‑helicase maakt deel uit van het onderhoudsteam van de cel en helpt DNA te ontwinden zodat schade kan worden gedetecteerd en hersteld. Mensen die zonder werkend WRN worden geboren, ontwikkelen het syndroom van Werner, een zeldzame aandoening gekenmerkt door voortijdige veroudering, wat aangeeft hoe cruciaal dit eiwit is voor het behoud van het genoom. Tumoren met “microsatellietinstabiliteit‑hoog” (MSI‑H) — een veelvoorkomend defect bij darmkanker en sommige andere tumoren — blijken bijzonder afhankelijk van WRN. Wanneer WRN in deze cellen wordt uitgeschakeld, valt hun al fragiele DNA snel uiteen en sterven de kankercellen. Dat maakt WRN een aantrekkelijk doelwit voor geneesmiddelen, maar tot nu toe ontbrak het aan een duidelijk beeld van hoe het eiwit van vorm verandert terwijl het DNA pakt, chemische brandstof verbruikt en langs het genetische materiaal beweegt.
WRN zien rekken en ademen
De auteurs gebruikten röntgenkristallografie om meerdere hoogresolutie “momentopnames” vast te leggen van de kern van het menselijke WRN‑helicase. Ze bepaalden structuren van WRN alleen en van WRN gebonden aan enkelstrengs DNA en een niet‑afbreekbare ATP‑achtige brandstofmolecule. Deze beelden toonden dat het eiwit is opgebouwd uit twee hoofdlobjes die verbonden zijn door een flexibele scharnier die zich gedraagt als een ademend gewricht. In zijn rusttoestand, zonder brandstof, neemt WRN een compacte “gesloten” vorm aan waarbij de lobben dicht tegen elkaar liggen. Wanneer ATP‑achtige brandstof en DNA aanwezig zijn, zwaaien de lobben uiteen naar een meer “open” configuratie die DNA kan omsluiten in een positief geladen groeve. Een kleine aromatische lus binnen WRN herschikt zich tot een korte helix en klemt zich tussen DNA‑basen, als een ratel die het eiwit helpt vooruit te stappen zonder terug te glijden.
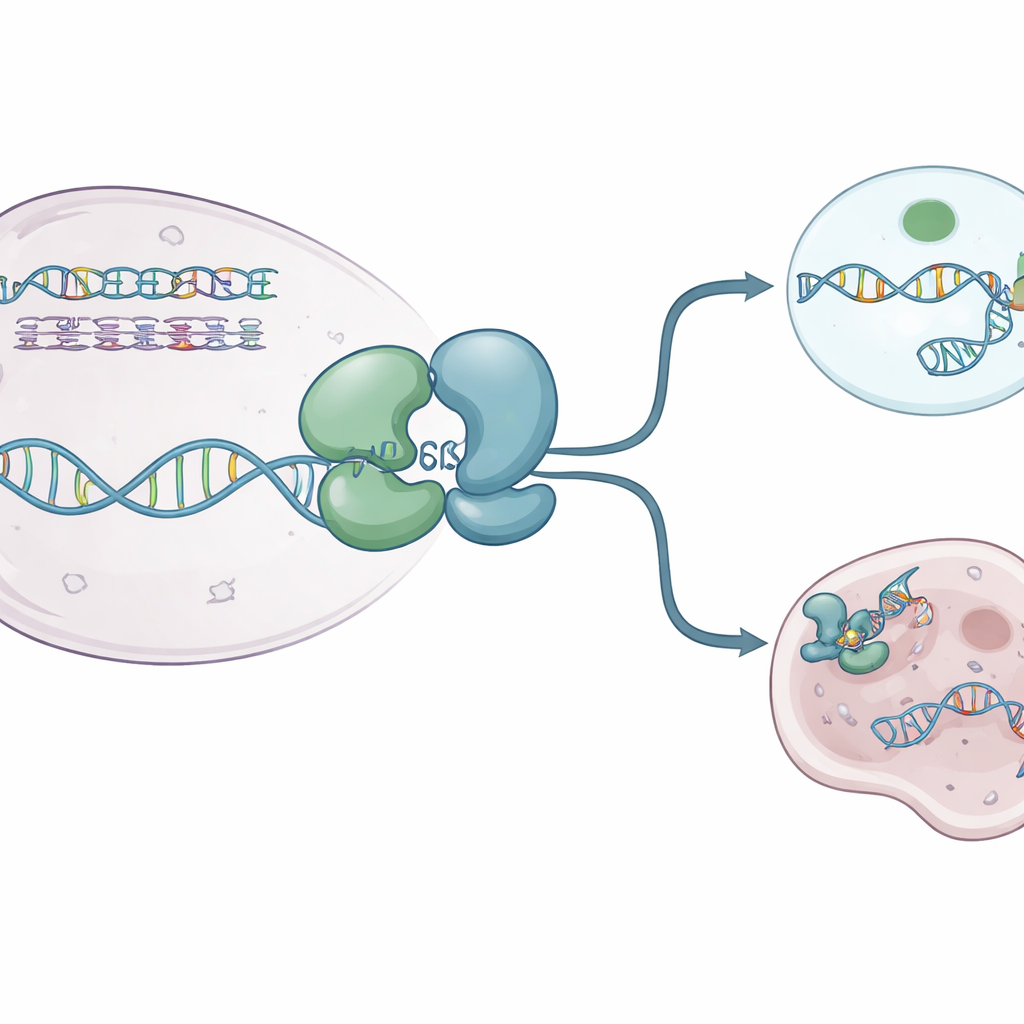
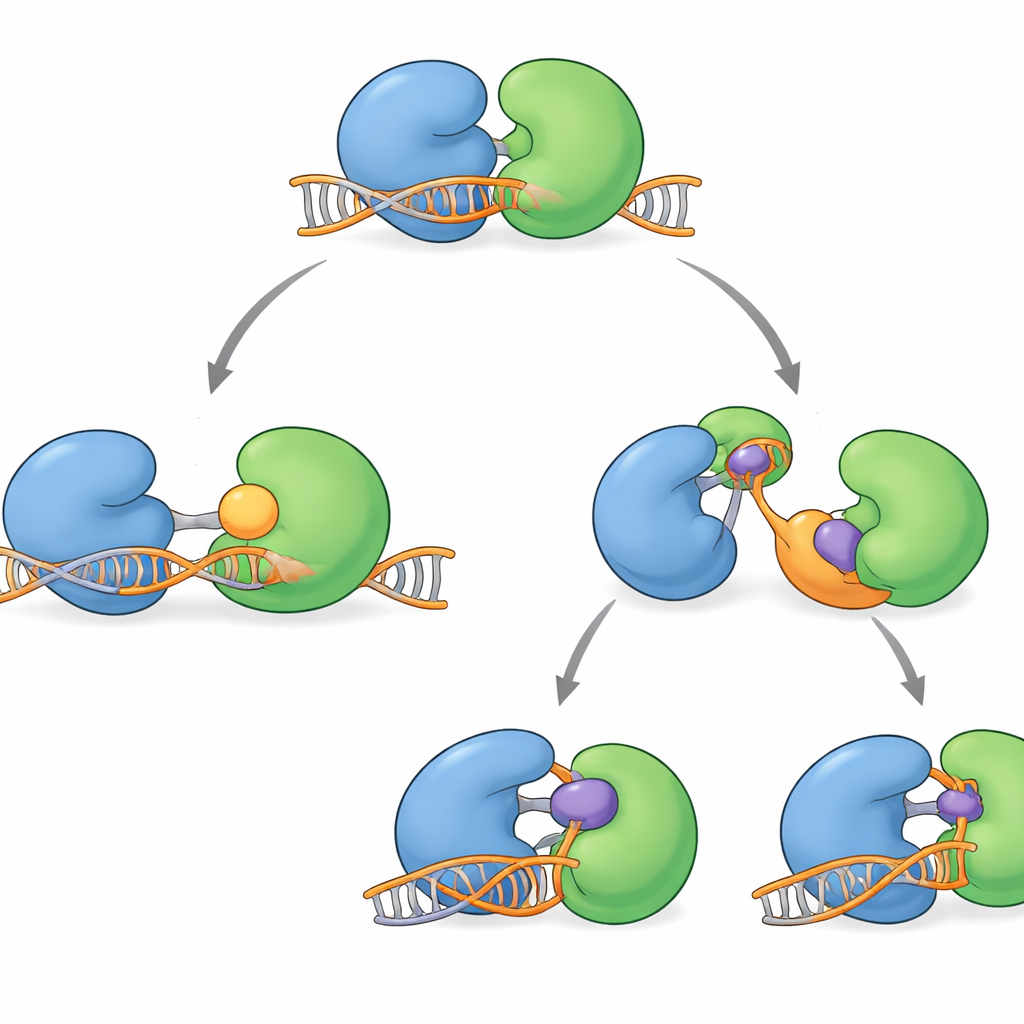
Hoe huidige medicijnen WRN uitschakelen
Verschillende WRN‑blokkerende verbindingen zijn recentelijk in klinische tests gekomen. Ze blokkeren de actieve groeve van het eiwit niet direct. In plaats daarvan werken ze op afstand, door de scharnierregio vast te grijpen en WRN te vergrendelen in vormen die DNA niet goed kunnen binden. Sommige moleculen, zoals HRO761 en een verwant klinisch kandidaatgebied van GSK, draaien één lob ongeveer 180 graden ten opzichte van de andere, wat een dramatische “gedraaide” vorm oplevert die buiten DNA zit. Andere, waaronder VVD‑133214 en een nauw verwant verbinding bestudeerd in deze studie, klemmen WRN vast in een strak “gesloten” arrangement dat er niet in slaagt belangrijke DNA‑vasthoudende oppervlakken bloot te leggen. Biofysische experimenten bevestigden dat wanneer deze geneesmiddelen gebonden zijn, WRN geen stabiel complex meer kan vormen met enkelstrengs DNA, waardoor de koppeling tussen ATP‑gebruik en DNA‑ontwinding effectief wordt verbroken.
Hoe kankercellen leren te ontsnappen
Om te zien hoe tumoren deze medicijnen mogelijk ontwijken, kweekte het team MSI‑H‑darmkankercellen in aanwezigheid van WRN‑remmers gedurende weken tot maanden. Resistente populaties verschenen snel. Genetische analyses toonden aan dat de cellen in elk geval een enkele, precieze wijziging in het WRN‑gen nabij de medicijnbindende scharnier hadden verworven. Één mutatie verzwakte het effect van de “gedraaide‑toestand” remmer HRO761, terwijl een andere mutatie de gevoeligheid voor VVD‑133214 verminderde, dat de gesloten toestand prefereert. Bovendien verhoogden veel resistente cellen de productie van WRN, waardoor ze zichzelf meer kopieën van het doel gaven en het effect van het medicijn deels verwaterden. Deze bevindingen weerspiegelen resistentiepatronen die ook bij andere gerichte kankertherapieën worden gezien, waarbij kleine structurele aanpassingen in het doeleiwit of overexpressie de behandeling kunnen verzwakken.
Vooruitblik: slimmere WRN‑blokkers
Samen brengen de nieuwe structuren een volledige werkcyclus van WRN in kaart terwijl het zich aan DNA hecht, een stap zet en zich vervolgens reset. Ze tonen ook dat de huidige klinische verbindingen voornamelijk “off‑DNA” vormen van het eiwit stabiliseren. Voor een algemene lezer is de kernboodschap dat we nu begrijpen waar WRN kwetsbaar is en hoe tumoren zich kunnen aanpassen. Dit suggereert een volgende golf remmers die WRN binden wanneer het op DNA is vastgezet, en het mogelijk in een toxische toestand gevangen houden — vergelijkbaar met succesvolle middelen die andere DNA‑reparatie‑enzymen in de val lokken. Zulke “on‑DNA” WRN‑blokkers, gebruikt alleen of samen met bestaande middelen, zouden duurzamere manieren kunnen bieden om de verborgen zwakte van MSI‑H‑kankers uit te buiten.
Bronvermelding: Fletcher, C.T., Mornement, A.A., Barrett, C. et al. Structural insights into WRN helicase reveal conformational states and opportunities for MSI-H cancer drug discovery. Commun Biol 9, 334 (2026). https://doi.org/10.1038/s42003-026-09584-0
Trefwoorden: WRN-helicase, microsatellietinstabiliteit, DNA-reparatie, allosterische remmers, medicijnresistentie