Clear Sky Science · nl
Lokale kationklem vervormt en verzacht RNA-duplex
Waarom deze kleine draai in RNA van belang is
Binnen elke cel worden DNA en RNA voortdurend gebogen, uitgerekt en gedraaid terwijl ze genetische informatie opslaan en gebruiken. Deze bewegingen zijn niet slechts mechanische details—ze bepalen hoe genen worden afgelezen, hoe virussen zich kopiëren en hoe nieuwe op RNA gebaseerde medicijnen en nanodevices zullen functioneren. Deze studie laat zien dat eenvoudige zouten, bestaande uit positief en negatief geladen ionen, dramatisch kunnen veranderen hoe stijf of flexibel RNA is, en dat RNA zeer anders reageert dan DNA. Inzicht in deze subtiele ‘verzachtende en verstevigende’ wisselwerking kan onderzoekers helpen RNA-geneesmiddelen, vaccins en moleculaire hulpmiddelen beter te ontwerpen.
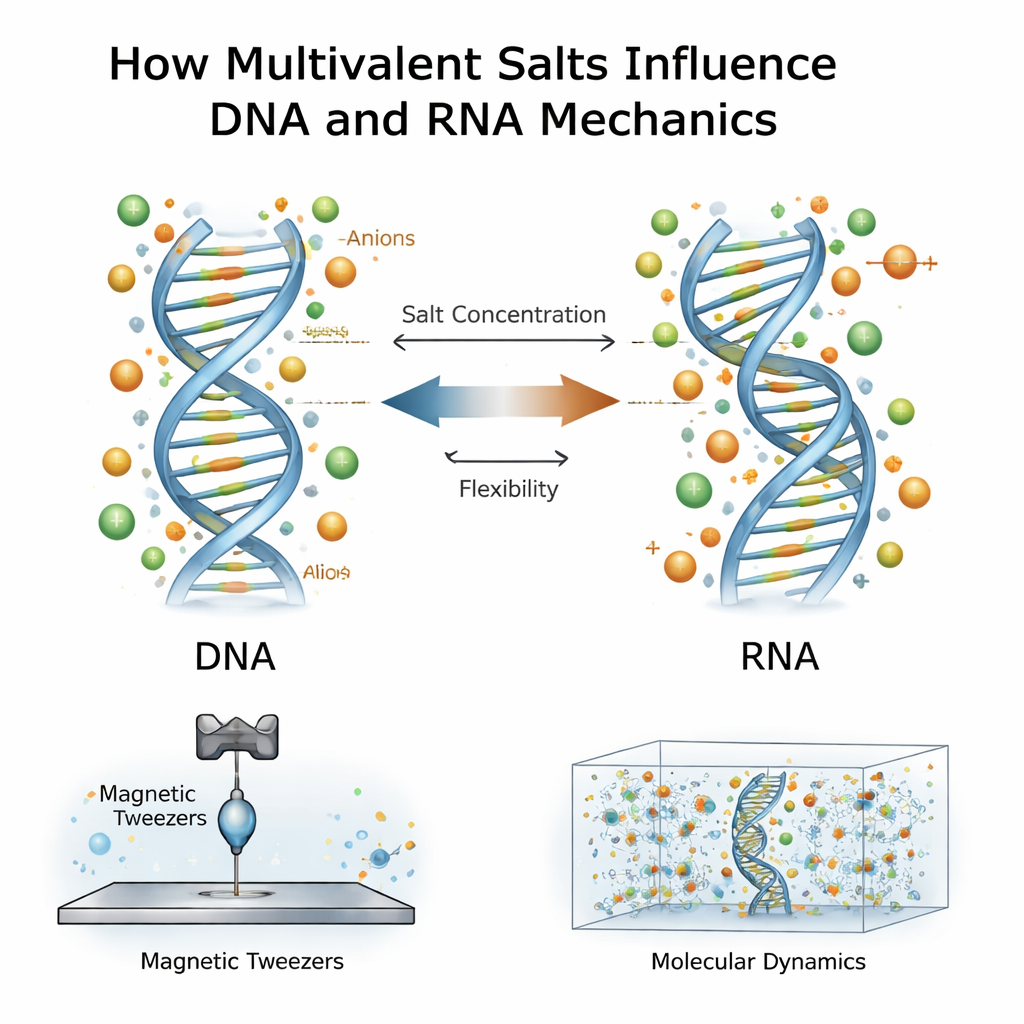
Zoute omgeving en genetische moleculen
DNA en RNA dragen een sterke negatieve elektrische lading, dus ze worden omgeven door wolken van tegengesteld geladen ionen in water. Het meeste eerdere werk richtte zich op positief geladen ionen, vooral multivalente ionen die twee of drie positieve ladingen dragen, zoals magnesium of spermidine. Deze ionen staan bekend om het bijeenhouden van DNA-strengen, het condenseren daarvan of het veranderen van hoe gemakkelijk ze buigen. RNA, hoewel chemisch vergelijkbaar met DNA, gedraagt zich anders: het is meestal moeilijker te buigen maar gemakkelijker uit te rekken. Het nieuwe werk stelt een diepergaande vraag: wat gebeurt er wanneer zowel de positieve ionen als hun begeleidende negatieve partners—an ionen genoemd—interageren met DNA en RNA bij zeer hoge zoutconcentraties, veel hoger dan in typische cellen?
Aantrekken van individuele moleculen om stijfheid te meten
De onderzoekers gebruikten een techniek die magnetische pincetten heet om individuele DNA- of RNA-dubbelhelixen één voor één uit te rekken. Elk molecuul was aan de ene kant verankerd aan een glasoppervlak en aan de andere kant aan een klein magnetisch bolletje. Door magneten boven het preparaat te verplaatsen, konden ze met gecontroleerde krachten trekken en vastleggen hoe ver elk molecuul uitrekte en hoe het draaide onder spanning. Uit deze kracht–uitrekselcurven haalden ze vier cruciale mechanische eigenschappen: hoe moeilijk het molecuul buigt, hoe moeilijk het uitrekt, de effectieve lengte per basenpaar en hoe draaien de lengte verandert. Ze herhaalden deze metingen over een breed bereik van multivalente zoutconcentraties voor verschillende zouten, waaronder spermidine en calciumchloride.
DNA verstevigt weer, maar RNA verzacht plotseling
Voor DNA kwam het gedrag grotendeels overeen met de verwachtingen. Naarmate de concentratie van multivalente positieve ionen toenam, werd DNA eerst gemakkelijker te buigen—de stijfheid daalde—omdat de ionen zijn negatieve lading neutraliseerden. Bij nog hogere niveaus compenseerden de overtollige positieve ionen zelfs teveel, waardoor de netto-lading van DNA effectief omkeerde. Deze “ladingsinversie” maakte DNA opnieuw moeilijker te buigen, waardoor de stijfheid weer steeg. Verrassend genoeg toonde RNA het tegenovergestelde en een veel dramatischer patroon. Bij lage tot matige zoutniveaus nam de buigstijfheid toe: het RNA-duplex werd rechter en stijver. Maar bij zeer hoge concentraties daalde de buigstijfheid van RNA met meer dan de helft, en andere eigenschappen zoals de rekbaarheid en het draai–rek-gedrag keerden op onverwachte manieren om.
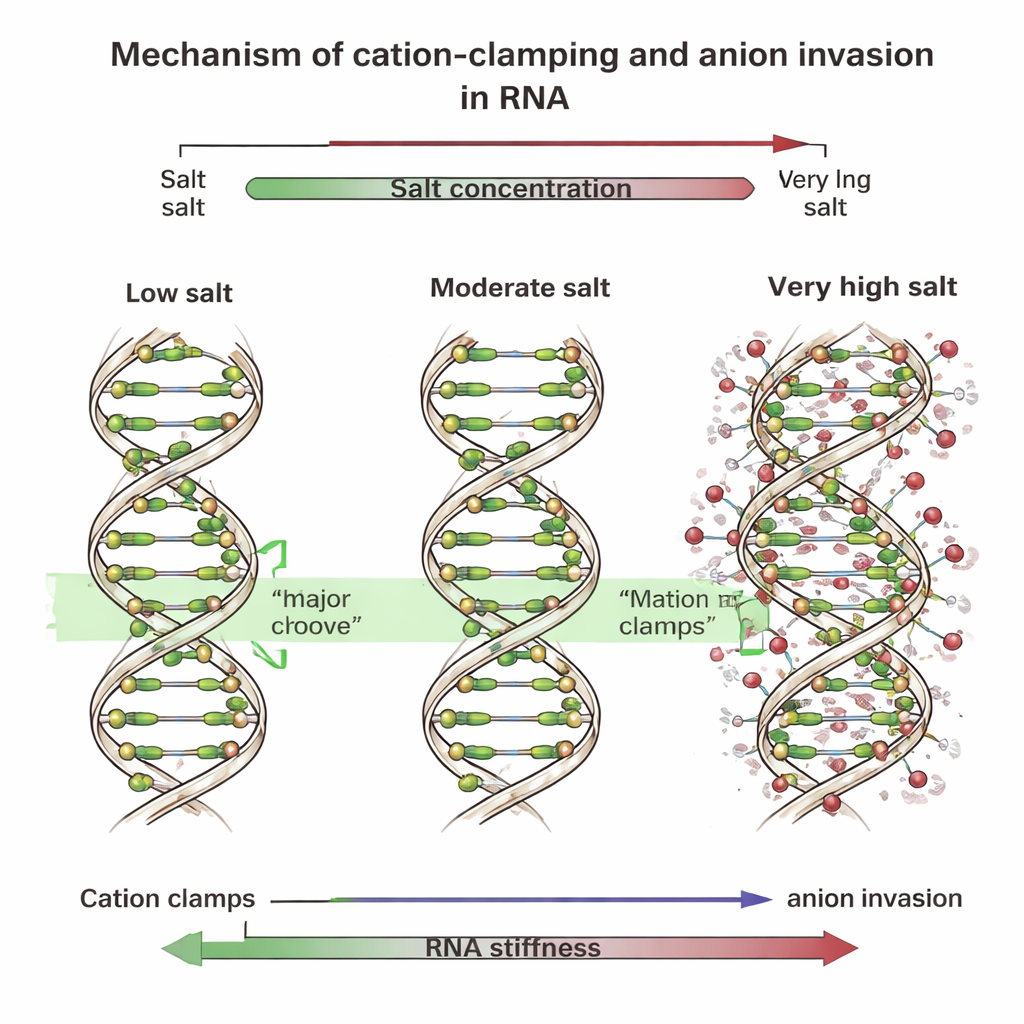
Klemmen, groeven en indringende ionen
Om de oorzaak te achterhalen, voerde het team gedetailleerde computersimulaties uit die elk atoom van korte DNA- en RNA-fragmenten in zout water volgden. Deze simulaties toonden dat multivalente positieve ionen zich bij lage en matige concentraties nestelen in een brede oppervlakte op RNA die de major groove wordt genoemd. Daar vormen ze “kationklemmen” die de groef overspannen, de zijden naar elkaar toe trekken, de helix rechttrekken en deze stijver maken. DNA, wiens groeven anders gevormd zijn, bindt deze ionen voornamelijk langs zijn buitenste ruggegraat. Bij zeer hoge zoutniveaus drukken echter veel negatieve ionen—zoals chloride—dicht op de RNA-ruggegraat en zelfs in de major groove. Hun aanwezigheid verstoort de ordelijke klemmen en breekt ze op in onregelmatige, vlekkerige “lokale klemmen” die de helix vervormen. Toen de onderzoekers dit effect nabootsten door kunstmatige veren toe te voegen of extra negatieve ionen dicht bij het RNA in de simulaties vast te zetten, boog de RNA-ruggegraat meer en daalde de algehele stijfheid drastisch, precies zoals waargenomen in experimenten.
Wat dit betekent voor toekomstige RNA-technologieën
Simpel gezegd laat de studie zien dat RNA ofwel rechter en stijver kan worden gemaakt ofwel meer geknikt en flexibeler, simpelweg door het type en de concentratie van omliggende zouten te veranderen. Bij bescheiden niveaus van multivalente ionen klemmen positieve ladingen het buitenoppervlak van RNA netjes vast en verstevigen het; bij extreme niveaus breken indringende negatieve ionen die uniforme versteviging en creëren ze vervormde, zachtere regio’s. DNA toont deze scherpe verzachting niet omdat het ionen op een andere manier bindt en in plaats daarvan een netto ladingsomkering ondergaat. Deze inzichten benadrukken dat niet alleen positieve ionen maar ook hun negatieve tegenhangers cruciaal zijn voor het beheersen van RNA-vorm. Die kennis zal onderzoekers helpen de mechanica van RNA doelbewust te verfijnen in het laboratorium—bijvoorbeeld om RNA-geneesmiddelen te stabiliseren, te sturen hoe RNA vouwt in biosensoren of betrouwbaarder op RNA gebaseerde nanostructuren te ontwerpen.
Bronvermelding: Zhang, C., Dong, HL., Zhang, JH. et al. Local cation-clamping distorts and softens RNA duplex. Commun Biol 9, 308 (2026). https://doi.org/10.1038/s42003-026-09580-4
Trefwoorden: RNA-mechanica, multivalente ionen, kationklem, DNA versus RNA, zouteffecten