Clear Sky Science · nl
CISH, een sleutelcontrolepunt binnen de cel, vergeleken met en gecombineerd met bestaande en opkomende immuuncontrolepunten bij kanker
De rem van kankervragende cellen loslaten
Kankerimmunotherapieën hebben de vooruitzichten voor veel patiënten veranderd, maar een groot deel van de mensen profiteert nog steeds weinig of niet. Deze studie onderzoekt een nieuwe manier om de eigen T-cellen van het lichaam—de scherpschutters van het immuunsysteem—te versterken door een interne “rem” genaamd CISH uit te schakelen. In tegenstelling tot huidige medicijnen die inwerken op schakelaars aan het celoppervlak, richt deze strategie zich op een regelsysteem dat diep in de cel ligt, met als doel getransformeerde T-cellen veel beter te laten vinden en vernietigen van tumoren, zelfs wanneer kankers proberen zich te verbergen.
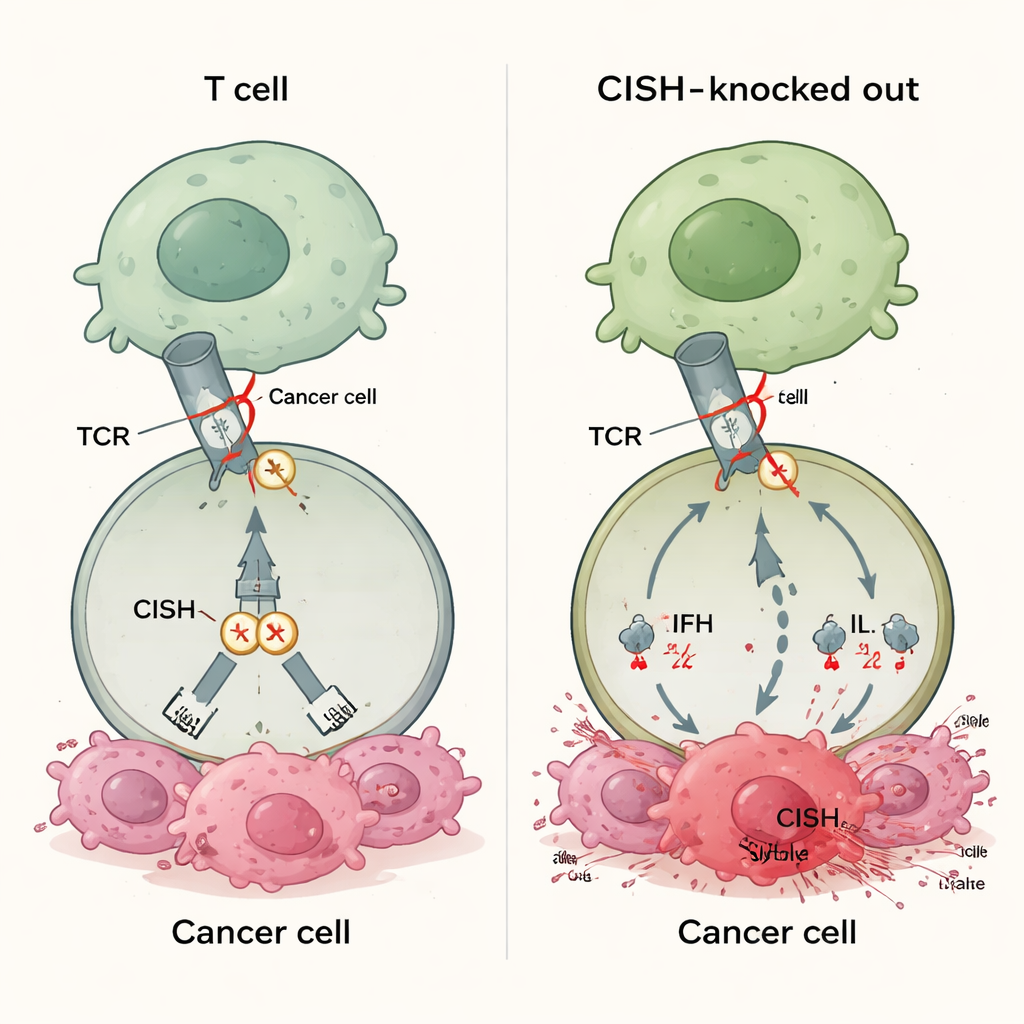
Een nieuw soort immuunrem
De meeste goedgekeurde immunotherapieën blokkeren eiwitten zoals PD-1 op het oppervlak van T-cellen. Deze geneesmiddelen werken alleen wanneer tumoren overeenkomende partnermoleculen zoals PD-L1 vertonen, en veel kankers drukken ofwel nooit genoeg van deze partners uit of verliezen ze in de loop van de tijd. Dat helpt verklaren waarom 30–60% van de patiënten niet reageert op de huidige checkpoint-therapieën. CISH behoort tot een andere klasse remmen die binnenin de T-cel zitten. Het wordt ingeschakeld wanneer de T-celreceptor een doel waarneemt en dempt vervolgens het signaal door de afbraak van een sleutel-signaaleiwit te bevorderen. Omdat deze actie niet afhankelijk is van ligandexpressie door de tumor, zou het uitzetten van CISH in principe de T-celresponsen kunnen versterken bij veel kankertypes, ongeacht de PD-L1-status of andere biomarkers.
Het opnemen tegen bestaande checkpoints
De onderzoekers gebruikten CRISPR-genbewerking om CISH te verwijderen en vergeleken de resulterende T-cellen met cellen zonder PD-1 of zonder verschillende andere interne remmen. Toen ze de T-cellen zwak stimuleerden—een situatie bedoeld om tumoren na te bootsen die slechts lage hoeveelheden antigeen tonen—produceerden CISH-gedelete cellen veel meer belangrijke immuunboodschappers, waaronder interferon-gamma, TNF-alpha en IL-2. Deze cellen waren ook meer "polyfunctioneel", wat betekent dat individuele T-cellen meerdere taken tegelijk konden uitvoeren, een kenmerk van krachtige antitumoractiviteit. Ter vergelijking: het eenvoudig verwijderen van PD-1 hielp niet onder deze lage-signaalcondities. Over meerdere tests heen versterkte het verlies van CISH activering, dodingcapaciteit en de vorming van duurzame geheugenachtige T-cellen sterker dan het uitschakelen van andere kandidaat-intracellulaire checkpoints zoals RASA2, CBLB, SOCS1, REGNASE1, HPK1 of PTPN1/2.
Samenwerken met andere interne schakelaars
Aangezien T-celsignalering door veel overlappende paden wordt geregeld, vroegen de onderzoekers zich af of het combineren van CISH-verwijdering met het wegnemen van andere remmen extra voordelen zou opleveren. Met multiplex CRISPR-bewerking vonden ze dat het verwijderen van CISH samen met SOCS1, HPK1 of RASA2 de productie van behulpzame cytokinen bij zwakke stimulatie verder verhoogde. In een tumormodel gebaseerd op een veelvoorkomende KRAS-mutatie waren T-cellen die waren uitgerust met een KRAS-specifieke receptor beter in het doden van kankercellen wanneer CISH werd verwijderd, en dit effect werd sterker wanneer het verlies van CISH werd gecombineerd met verwijdering van SOCS1 of RASA2. Deze bevindingen suggereren dat CISH een niet-redundante knoopregelaar in de T-celbiologie controleert en kan samenwerken met geselecteerde partners om tumorspecifieke doding te verscherpen.
CAR-T-cellen robuuster maken tegen slinkse tumoren
De auteurs richtten zich vervolgens op een klinisch belangrijke setting: CAR-T-cellen die zich richten op de B-celmarker CD19. Ze creëerden leukemiecellen die verschillende niveaus van CD19 uitdrukten om tumoren na te bootsen die hun doelwit afwerpen of verminderen om therapie te ontlopen. CAR-T-cellen zonder CISH waren opvallend beter in het vernietigen van kankercellen, zelfs wanneer CD19 schaars was, en scheidden meer activerende en rekruterende signalen uit. Tegelijkertijd gaven ze lagere hoeveelheden van moleculen vrij die bekend staan om T-cellen te verzwakken of tumorgroei te bevorderen, zoals Galectine-1, Galectine-3, oplosbaar 4-1BB, IL-1α en het glycoproteïne EMMPRIN/CD147. Samen wijzen deze veranderingen op een agressievere, minder gemakkelijk onderdrukte CAR-T-cel, die bijzonder geschikt is voor vijandige, lage-antigeen tumoromgevingen.
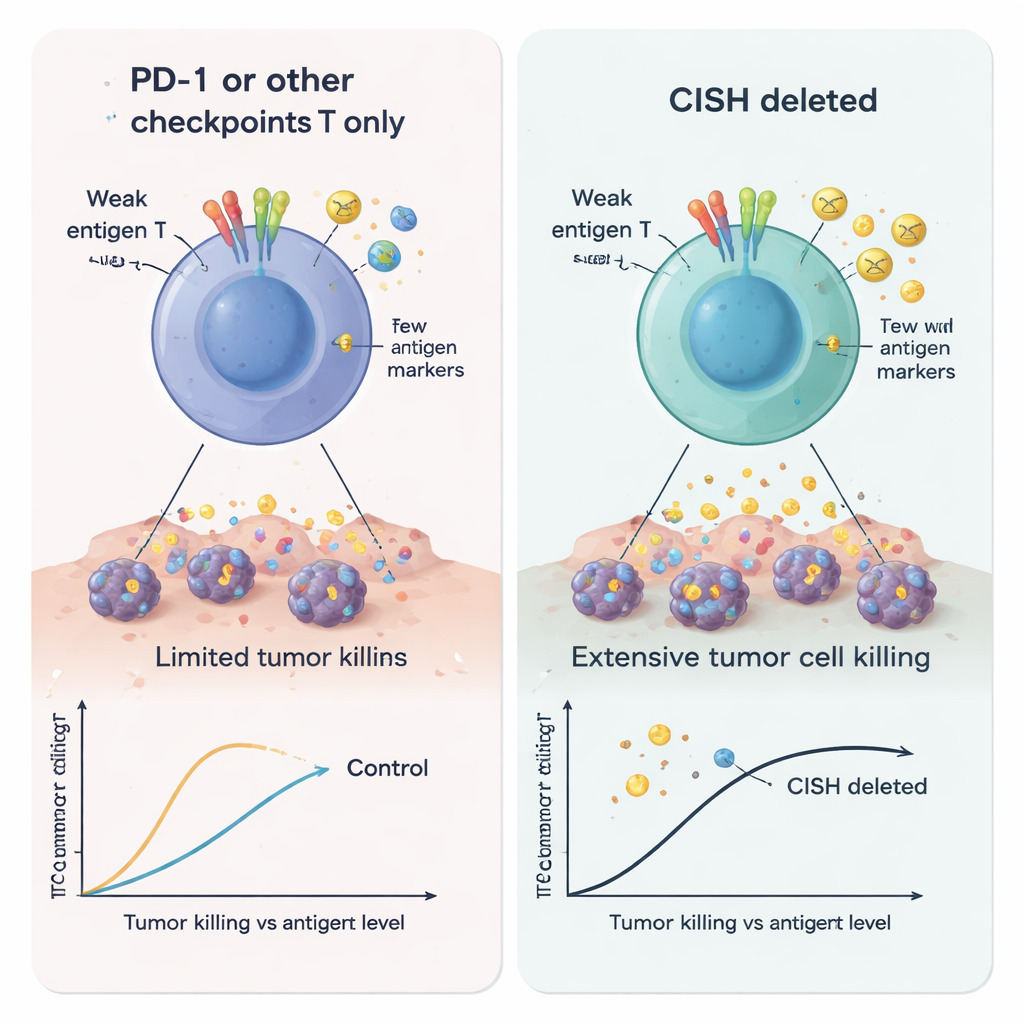
Van laboratoriumbank naar patiënten
Los van reageerbuis- en kweekschotelwerk heeft het idee om CISH te richten al patiënten bereikt. Een eerste-in-mens onderzoek met tumorinfiltrerende lymfocyten die bewerkt waren om CISH te verwijderen bij een persoon met gevorderde dikkedarmkanker leverde een volledige respons op die meer dan twee jaar heeft aangehouden, ondanks de weerstand van de kanker tegen meerdere voorgaande behandelingen. Door aan te tonen dat CISH een krachtig, geneesmiddelbaar intern checkpoint is dat de gevoeligheid van T-cellen voor zelfs zwakke tumorsignalen verhoogt, helpt deze studie dat opmerkelijke klinische resultaat te verklaren en ondersteunt ze inspanningen om toekomstige therapieën te ontwikkelen—of het nu gaat om genbewerkte cellen of pillen—die deze interne rem veilig versoepelen en het bereik van kankerimmunotherapie verbreden.
Bronvermelding: Cano, F., Bravo-Blas, A., Colombe, M. et al. CISH, a key intracellular checkpoint, in comparison and combination to existing and emerging cancer immune checkpoints. Commun Biol 9, 319 (2026). https://doi.org/10.1038/s42003-026-09579-x
Trefwoorden: kankerimmunotherapie, T-cellen, CAR-T-therapie, immuuncontrolepunten, CRISPR-genbewerking