Clear Sky Science · nl
Een pathogene mutatie in α-SNAP belemmert binding aan membraanlipiden door een kritisch hydrofoob lusje te verbergen
Hoe een kleine eiwitverandering de hersenontwikkeling kan verstoren
Onze hersencellen vervoeren voortdurend vracht in kleine blaasjes die vesikels worden genoemd, en een helper-eiwit genaamd alpha-SNAP is cruciaal om die leveringen mogelijk te maken. Een zeldzame mutatie in alpha-SNAP, bekend van een muizenlijn genaamd “hyh”, veroorzaakt ernstige problemen in hersenvorming en vloeistofbalans. Deze studie stelt een schijnbaar eenvoudige vraag met grote gevolgen: voorkomt die ene letterverandering in alpha-SNAP dat het aan celmembranen hecht, en kan dat een belangrijke reden zijn dat de hersenen misgaan?
Een cellulaire losplaatsmedewerker met vele taken
Alpha-SNAP functioneert normaal als een soort losplaatsmedewerker voor vesikels: het helpt ze te versmelten met cellulair membraan zodat vracht kan worden vrijgegeven of gerecycled. Het werkt samen met een groep eiwitten die SNAREs worden genoemd en een energieverbruikende machine genaamd NSF om membranen samen te trekken en het systeem vervolgens te resetten voor de volgende ronde. Naast deze klassieke rol helpt alpha-SNAP ook bij het regelen van processen zoals cellulaire schoonmaak (autofagie), geprogrammeerde celdood, calciuminstroom en energieweging. Al deze functies zijn op de een of andere manier afhankelijk van het vermogen van alpha-SNAP om het vettige oppervlak van membranen aan te raken en gedeeltelijk in te dringen.
Een verborgen lusje en een lastiggevallen mutatie
Eerder werk toonde aan dat alpha-SNAP een kort vettig “lusje” gebruikt dicht bij één uiteinde van het eiwit om zich aan membranen te haken. In het gezonde eiwit steekt dit lusje naar buiten en kan het in de buitenlaag van het membraan duiken. In de hyh-muis wordt één bouwsteen op positie 105 vervangen, wat de M105I-mutatie creëert. De auteurs gebruikten computersimulaties om te bekijken hoe deze verandering de vorm van het eiwit verandert. Ze vonden dat het mutant-eiwit iets compacter wordt en zo draait dat het hydrofobe lusje naar binnen wordt geklapt, weg van water en weg van membranen. Daardoor nadert het mutant-eiwit membranen onder een vlakkere hoek en drukt het er vaak tegenaan met een minder kleverig gebied, wat zowel de contactduur als de diepte van insertie vermindert. Berekeningen van bindingsenergie ondersteunden dit: het wildtype-eiwit nestelde zich in een laag-energie, sterk gebonden toestand, terwijl de mutant zwakkere, ondiepere contacten prefereerde.
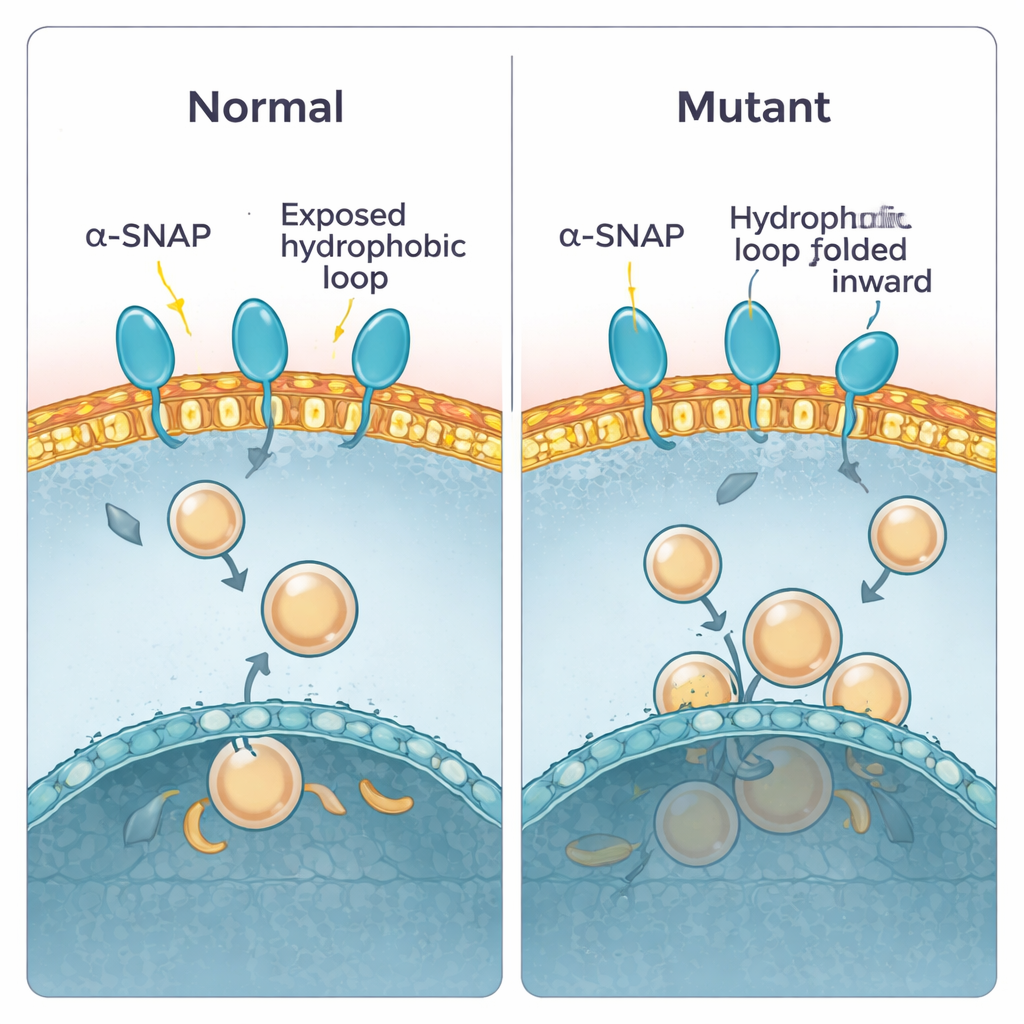
De voorspelling testen in het laboratorium
Om deze voorspellingen te controleren, zuiverde het team zowel normaal als mutant alpha-SNAP en testte hoe ze zich gedroegen in verschillende experimentele opstellingen. Eerst gebruikten ze een detergent dat zich scheidt in waterige en vette fasen, wat de keuze tussen water en membraan nabootst. Normaal alpha-SNAP verdeelde zich evenredig, in overeenstemming met een gebalanceerd, gedeeltelijk vettig oppervlak. De mutantversie was minder geneigd de vette fase binnen te gaan, wat suggereert dat zijn vette delen inderdaad meer begraven zijn. Vervolgens lieten ze de eiwitten interageren met platte plasmamembraan-“vellen” bereid uit cellen en maakten ze beelden van hoeveel bindingspunten verschenen. Opnieuw stipte normaal alpha-SNAP het membraan aan, terwijl de mutant veel minder bond. Ten slotte lieten ze kunstmatige membraanblaasjes (liposomen) gemaakt van hersenlipiden door suikergradiënten drijven. Wildtype alpha-SNAP voer omhoog met vesikels rijk aan plasmamembraanlipiden, terwijl de mutant achterbleef en slecht bond, tenzij de vesikels van een ander, meer intern membraanmengsel waren gemaakt.
Gevolgen in de zich ontwikkelende hersenen
De onderzoekers richtten zich vervolgens op de hersenen van zich ontwikkelende muizembryo's, met focus op een stadium waarin nieuwe zenuwcellen ontstaan. Door celinhoud te scheiden in oplosbare en membraangebonden fracties lieten ze zien dat de totale alpha-SNAP-niveaus al waren verlaagd in hyh-hersenen, maar belangrijker nog: het aandeel dat aan membranen was gebonden, was onevenredig laag vergeleken met normale muizen. Toen ze verder verschillende membraantypen scheidden, vonden ze dat het grootste verlies plaatsvond aan het plasmamembraan, het buitenoppervlak van de cel, terwijl interne membranen veel minder werden aangetast. Microscopie vertelde hetzelfde verhaal: in normaal weefsel omlijnde alpha-SNAP cellen in een honingraatpatroon dat overeenkwam met een bekend oppervlaktemarker. In hyh-hersenen vervaagde deze duidelijke randkleuring tot een meer diffuse, interne gloed, wat aangeeft dat het mutant-eiwit er niet in slaagt verankerd te blijven aan de celrand waar vesikelfusie en signalering het meest actief zijn.
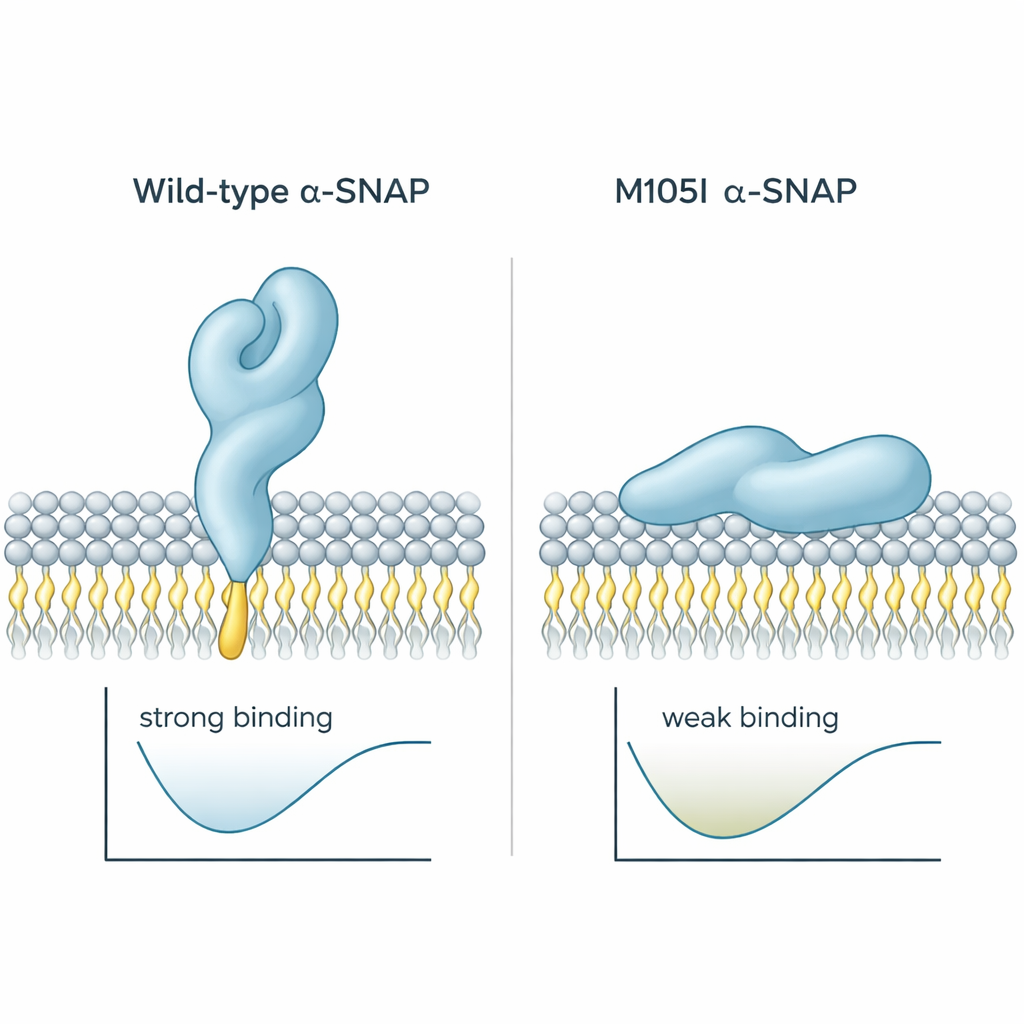
Waarom dit relevant is voor ziekte
Alles bij elkaar genomen toont het werk aan dat de M105I-mutatie meer doet dan alleen de hoeveelheid alpha-SNAP verlagen; ze verandert hoe het eiwit vouwt zodat het belangrijke membraangrijpende lusje verborgen raakt. Dat maakt het voor alpha-SNAP moeilijker de plasmamembraan vast te grijpen en de juiste oriëntatie aan te nemen om fusie-machinerie te organiseren. In een zich ontwikkelende hersenen, waar precieze levering van signalen en bouwmaterialen aan het celoppervlak essentieel is, draagt deze subtiele structurele fout waarschijnlijk bij aan hydrocefalie, verkeerd aangesloten cortex en andere afwijkingen die bij hyh-muizen worden gezien. Voor niet-specialisten is de boodschap duidelijk: zelfs een kleine verandering in de vorm van een enkel eiwit kan vormen hoe cellen communiceren en daarmee hoe een brein wordt opgebouwd.
Bronvermelding: Méndez-Ruette, M., Bedoya, M., Hinrichsen, B. et al. A pathogenic mutation in α-SNAP impairs membrane lipid binding by concealing a critical hydrophobic loop. Commun Biol 9, 294 (2026). https://doi.org/10.1038/s42003-026-09578-y
Trefwoorden: alpha-SNAP, membraanbinding, proteïnemutatie, hersenontwikkeling, blaasfusie