Clear Sky Science · nl
Ontwikkeling van capsaïcine-afgeleide prohibitine-liganden om de interactie Aurora kinase A/PHB2 en mitofagie in kankercellen te moduleren
Waarom een chilipeperstof van belang is voor kanker
Chilipepers danken hun branderigheid aan capsaïcine, een klein molecuul dat zich bindt aan eiwitten in onze cellen. Deze studie onderzoekt een onverwachte wending van dat bekende kruid: onderzoekers hebben capsaïcine herontworpen om nieuwe, geneesmiddelachtige moleculen te maken die zich richten op de “energiecentrales” van kankercellen — de mitochondriën — en een proces temperen dat die cellen gebruiken om hun energiefabriekjes in goede staat te houden. Omdat kankercellen in sterke mate afhankelijk zijn van efficiënte mitochondriën om hun ongecontroleerde groei van brandstof te voorzien, kan het selectief verstoren van dit ondersteuningssysteem een nieuwe benadering voor anticancermiddelen openen.
Cellulaire energiecentrales en hun interne opruimploeg
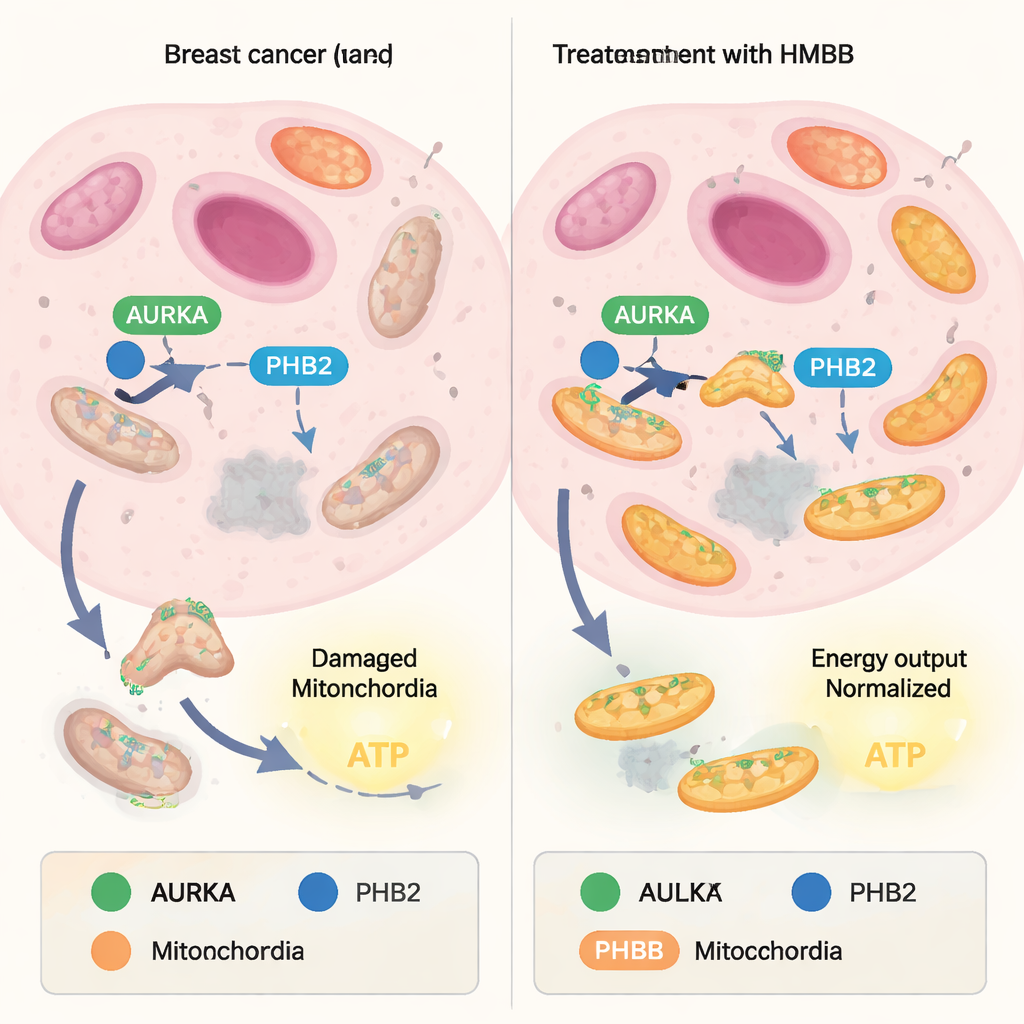
Mitochondriën houden voortdurend een balans tussen het opbouwen van nieuwe eenheden en het recyclen van beschadigde. De recyclingszijde, mitofagie genoemd, werkt als een kwaliteitscontrolesysteem: versleten mitochondriën worden gemarkeerd en afgebroken, terwijl gezondere achterblijven. Veel kankercellen kapen deze balans en gebruiken mitofagie om zwakke mitochondriën te verwijderen en te verrijken voor “toppresteerders” die grote hoeveelheden ATP produceren, de energie-eenheid van de cel. Een eiwit genaamd Aurora kinase A (AURKA), dat vaak te veel wordt geproduceerd in tumoren, werd recentelijk binnen mitochondriën aangetroffen waar het samenwerkt met een ander eiwit, Prohibitin‑2 (PHB2), en de autofagie-adapter LC3. Samen vormen ze een complex dat mitofagie bevordert en een hoge energieproductie in kankercellen ondersteunt.
Van pittige capsaïcine naar op maat gemaakte moleculaire hulpmiddelen
Eerder werk had aangetoond dat een natuurlijk verbinding, xanthohumol, zich kan binden aan PHB2 en het AURKA–PHB2–LC3-complex kan verstoren, waardoor mitofagie wordt geblokkeerd en de mitochondriale ATP-productie afneemt. De chemische structuur van xanthohumol is echter niet ideaal voor geneesmiddelenontwikkeling. In deze studie richtten de auteurs zich op capsaïcine, een andere natuurlijke PHB-ligand, en stelden ze de vraag of deze te herscheppen viel tot praktischere hulpmiddelen. Ze bevestigden eerst dat capsaïcine de interactie tussen AURKA en PHB2 in levende borstkankercellen licht verzwakt, met behulp van een beeldvormingstechniek (FRET/FLIM) die meet hoe dicht twee gelabelde eiwitten bij elkaar zitten. Vervolgens synthetiseerden ze 16 capsaïcine-geïnspireerde moleculen door de “staart” en het aromatische “hoofd” van de oorspronkelijke structuur te modificeren en testten systematisch hoe elke versie de AURKA–PHB2-partnerschap binnen mitochondriën beïnvloedde.
Een moleculair ‘lijm’ ontdekken die eiwitten aan elkaar vastzet
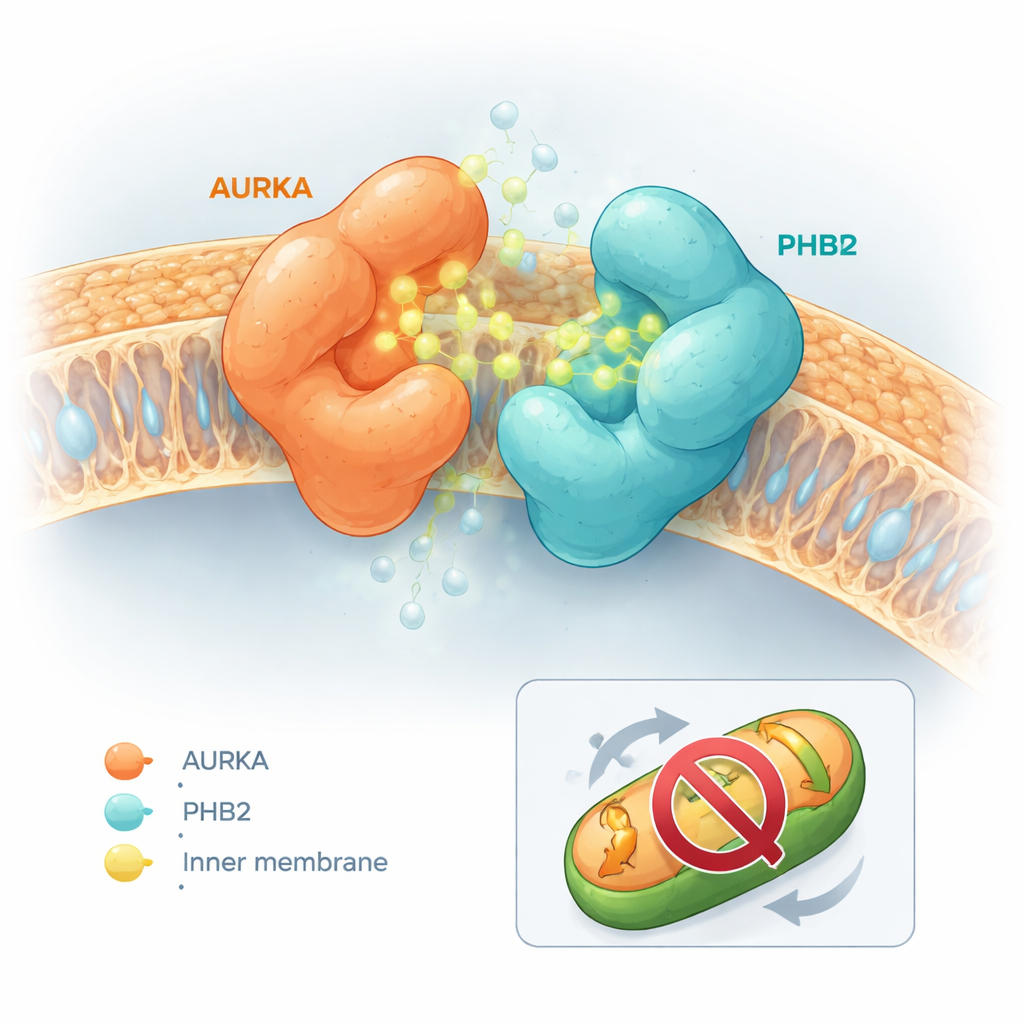
De gewijzigde moleculen hadden opvallend verschillende effecten. Sommige, zoals capsaïcine zelf of een derivaat dat verbinding 5 wordt genoemd, zorgden ervoor dat AURKA en PHB2 gemakkelijker uit elkaar gingen. Andere deden bijna niets. Een subset echter — met name een molecuul aangeduid als verbinding 13, later HMBB genoemd — had het tegenovergestelde effect en versterkte de binding tussen AURKA en PHB2 aanzienlijk. Computergestuurde docking-simulaties hielpen dit gedrag te verklaren. Capsaïcine en verbinding 5 neigden ertoe zich in de actieve plaats van AURKA te plaatsen op manieren die fysieke botsingen met PHB2 veroorzaakten, waardoor de twee eiwitten uit elkaar werden geduwd. In contrast nestelden verbindingen 12 en 13 zich in de actieve plaats van AURKA en maakten ze gelijktijdig contact met een bekend remmend pocket op PHB2 zonder een botsing te veroorzaken. Hun vormen stelden hen in staat te fungeren als een “moleculaire lijm”, die AURKA en PHB2 overbrugde en het complex stabiliseerde.
Het blokkeren van mitochondriale opruiming zonder het controlesysteem van de cel uit te schakelen
Een cruciale vraag was of dit moleculaire-lijmgedrag AURKA overal in de cel simpelweg uitschakelde — wat brede bijwerkingen zou riskeren — of dat het selectiever werkte. Met behulp van een aparte fluorescente biosensor die rapporteert over AURKA-activatie bij centrosomen — de structuren die het delingsapparaat van de cel organiseren — observeerde het team dat HMBB de AURKA-activiteit op deze locaties niet dempte. In mitochondriale assays keerde HMBB echter het verlies aan mitochondriale massa om dat normaal wordt veroorzaakt door AURKA-overexpressie in borstkankercellen. In cellen die van nature hoge niveaus van AURKA produceren, verhoogde HMBB het mitochondriale gehalte, wat aangeeft dat AURKA-gedreven mitofagie werd geblokkeerd. In cellen met lage AURKA-niveaus had HMBB weinig effect, wat de afhankelijkheid van de AURKA–PHB2-route onderstreepte.
Wat dit kan betekenen voor toekomstige kankerbehandelingen
Gezamenlijk tonen de bevindingen aan dat zorgvuldig ontworpen capsaïcine-afgeleiden de manier waarop AURKA en PHB2 in mitochondriën met elkaar interageren fijn kunnen afstemmen. Door als moleculaire lijm te werken, vergrendelen HMBB en verwante verbindingen AURKA en PHB2 in een configuratie die het gebruikelijke mitofagieprogramma verhindert, zonder de essentiële rollen van AURKA elders in de cel stil te leggen. Voor een niet-specialistische lezer is het belangrijkste idee dat de auteurs prototype-moleculen hebben gemaakt die selectief interfereren met hoe kankercellen hun energiecentrales in topconditie houden, mogelijk hun energievoorziening verzwakkend terwijl normale cel-functies worden gespaard. Hoewel deze verbindingen zich nog in een vroeg laboratoriumstadium bevinden, illustreren ze een veelbelovende strategie: het gebruik van kleine, geneesmiddelachtige moleculen om specifieke eiwitpartnerschappen binnen mitochondriën te targeten en daarmee de metabole voordelen aan te tasten waarop veel tumoren vertrouwen.
Bronvermelding: Djehal, A., Caron, C., Giordano, D. et al. Development of capsaicin-derived prohibitin ligands to modulate the Aurora kinase A/PHB2 interaction and mitophagy in cancer cells. Commun Biol 9, 320 (2026). https://doi.org/10.1038/s42003-026-09573-3
Trefwoorden: mitochondriën, mitofagie, Aurora kinase A, capsaïcine-afgeleiden, kankermetabolisme