Clear Sky Science · nl
Functionele herschikking van iNKT-cellen door sulfatide-reactieve type II NKT-cellen programmeert alveolaire macrofagen opnieuw om long ischemie-reperfusieletsel te verlichten
Waarom het beschermen van donorlongen ertoe doet
Wanneer chirurgen een long transplanteren of de bloedstroom herstellen na een blokkade, kan de plotselinge terugkeer van zuurstof het weefsel paradoxaal genoeg beschadigen. Dit probleem, long ischemie–reperfusieletsel genoemd, is een belangrijke oorzaak van vroeg falen na longtransplantatie en andere kritieke ingrepen. De hier samengevatte studie onderzoekt hoe een zeldzame groep immuuncellen kan worden “herschreven” om ontsteking te kalmeren, wat een nieuwe manier kan bieden om kwetsbare longen te beschermen wanneer dat het meest nodig is.
Immuuncellen die kunnen genezen of schaden
Onze longen worden bewaakt door alveolaire macrofagen, immuuncellen die in de luchtzakjes zitten en snel op gevaar reageren. Deze cellen kunnen schakelen tussen twee hoofdmodi. In een “vecht”-modus (vaak M1 genoemd) produceren ze ontstekingsbevorderende stoffen die helpen ziekteverwekkers te doden maar ook weefsel kunnen beschadigen. In een “herstel”-modus (vaak M2 genoemd) geven ze verzachtende moleculen af die ontsteking beperken en genezing bevorderen. Bij long ischemie–reperfusie verschuift het evenwicht richting de schadelijke vechtmodus. De onderzoekers redeneerden dat als ze de macrofagen op het juiste moment zachtjes naar de herstelmodus konden duwen, ze de impact van dit letsel mogelijk konden verzachten.
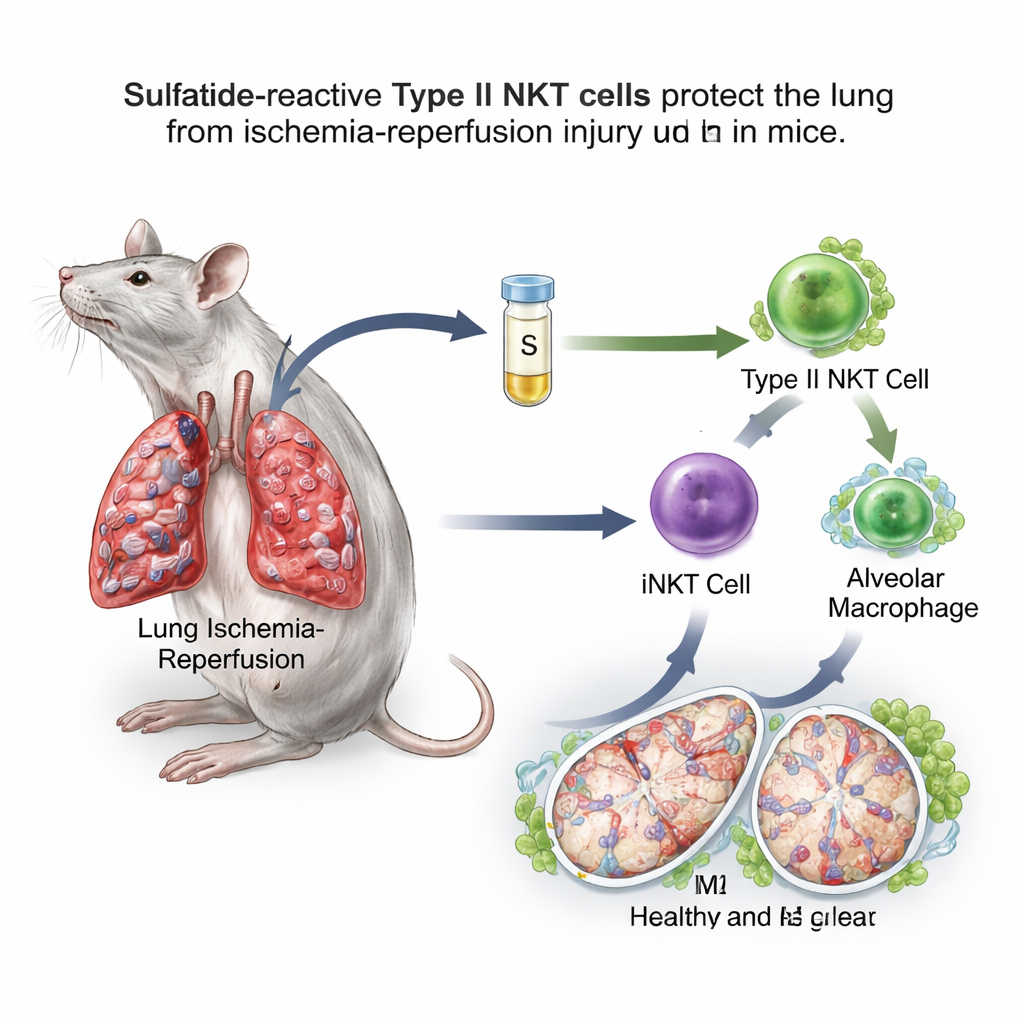
Een suiker–vetmolecuul schakelt een immuunschakelaar om
Het team richtte zich op natural killer T (NKT)-cellen, ongewone immuuncellen die tussen snel reagerende aangeboren afweer en langzamere, gerichte reacties in zitten. NKT-cellen komen in twee hoofdtypen. Type I, ook invariant NKT (iNKT)-cellen genoemd, staan erom bekend de long ischemie–reperfusie bij muizen te verergeren. Type II NKT-cellen kunnen daarentegen immuunreacties in andere organen remmen. Een vetachtig molecuul genaamd sulfatide wordt specifiek herkend door type II NKT-cellen. In een muismodel waarbij de bloedstroom naar één long een uur werd afgesloten en vervolgens werd hersteld, kregen de onderzoekers enkele uren voor het insult sulfatide toegediend. Ze vonden dat sulfatide-behandelde muizen minder longzwelling, minder lekkende bloedvaten, lagere oxidatieve stress, betere zuurstofwaarden en verminderde ontstekingsstoffen in longspoelvloeistof hadden vergeleken met onbehandelde dieren.
Macrofaag-herschrijving via een relais van signalen
Nadere bestudering toonde aan dat sulfatide alveolaire macrofagen verschoof naar de herstelgerichte M2-toestand. Deze macrofagen vertoonden meer oppervlaktemarkers en genexpressie die met genezing geassocieerd zijn en waren beter in het dempen van ontsteking wanneer ze in andere muizen werden overgedragen. Toen de wetenschappers selectief alveolaire macrofagen verwijderden, verslechterde het longletsel en verloor sulfatide grotendeels zijn beschermende effect, wat aantoont dat deze cellen een cruciale schakel in de route vormen. Belangrijk is dat het voordeel van sulfatide verdween in muizen die ofwel type II NKT-cellen ofwel type I iNKT-cellen misten, en dat het kon worden hersteld door iNKT-cellen terug te geven die vooraf aan sulfatide waren blootgesteld. Samen onthulden deze experimenten een relais: sulfatide activeert type II NKT-cellen, die op hun beurt het gedrag van iNKT-cellen herschikken, en deze herschrijven vervolgens alveolaire macrofagen.
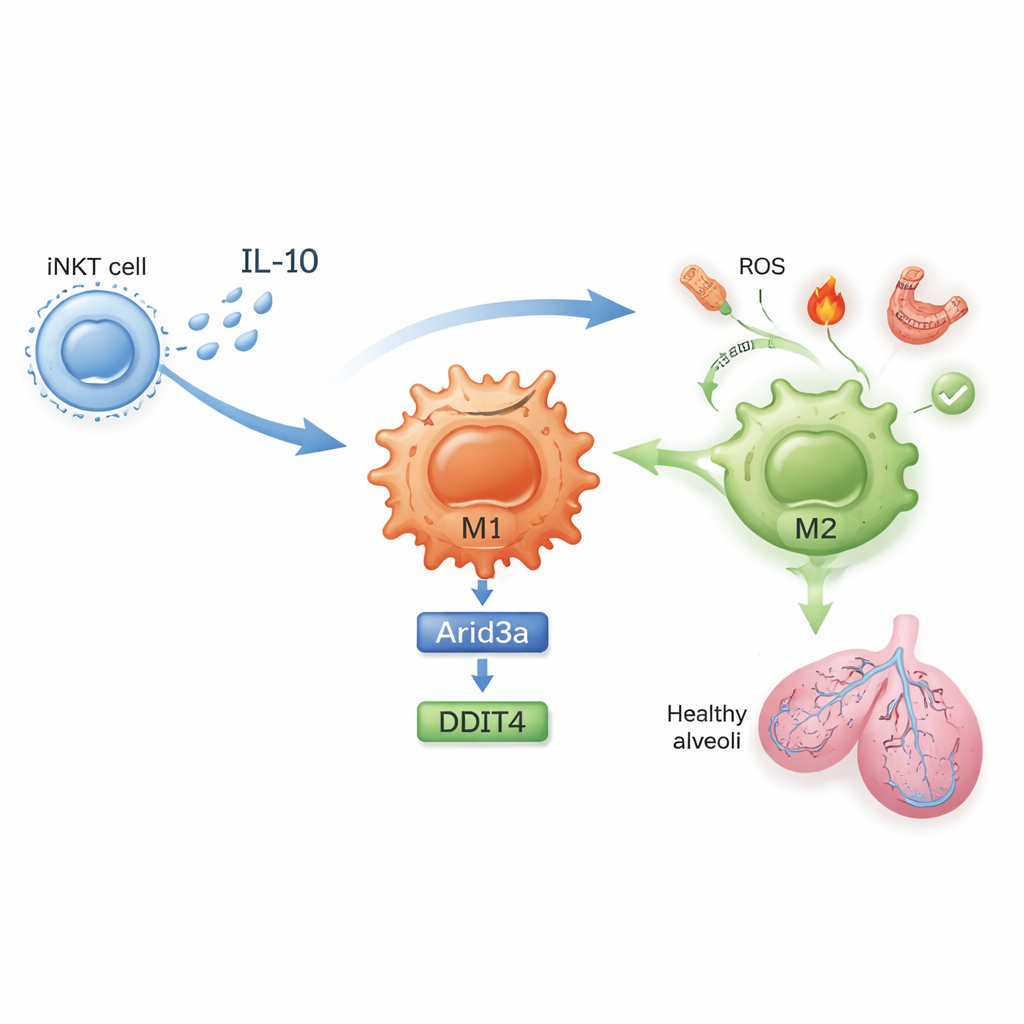
Een moleculaire keten die ontsteking kalmeert
Wat verandert er precies in deze cellen? In onbehandelde muizen prolifereerden long iNKT-cellen tijdens ischemie–reperfusie en produceerden hoge niveaus interferon-gamma, een krachtig ontstekingssignaal. Na blootstelling aan sulfatide maakten iNKT-cellen in plaats daarvan meer interleukine‑10 (IL‑10), een krachtig ontstekingsremmend molecuul, en minder interferon-gamma. De studie laat zien dat IL‑10 van iNKT-cellen direct op macrofagen werkt om hun M2-polarisatie te bevorderen. Met genexpressieprofilering en zorgvuldig ontworpen kweekexperimenten ontdekten de auteurs een moleculaire keten binnen macrofagen: IL‑10 verhoogt een transcriptiefactor genaamd Arid3a, die op zijn beurt een stress-responsgen genaamd DDIT4 omhoog reguleert. Deze Arid3a–DDIT4-as helpt een groeireguleringspad stil te leggen dat anders macrofagen in een ontstekingsstaat houdt, en duwt ze richting het beschermende M2-programma.
Van muizenlongen naar toekomstige therapieën
Om te testen hoe centraal deze moleculaire keten is, gebruikten de onderzoekers kleine interfererende RNA’s om Arid3a of DDIT4 in macrofagen te dempen voordat ze in muizen werden overgedragen. Wanneer één van beide genen werd uitgeschakeld, duwde sulfatide macrofagen niet volledig naar de herstelmodus en werd de longbescherming verzwakt. Aanvullende analyse suggereert dat een signaalproteïne genaamd YES1 helpt bij het herschakelen van iNKT-cellen naar IL‑10-productie door sulfatide-geactiveerde type II NKT-cellen. Hoewel deze bevindingen afkomstig zijn van muismodellen en van gemodificeerde cellen in het laboratorium, schetsen ze een helder verhaal: door kort een specifieke subset NKT-cellen met sulfatide te activeren, zou het mogelijk zijn anders schadelijke immuunreacties om te zetten in reacties die getransplanteerde of beschadigde longen beschermen. In de toekomst zouden geneesmiddelen die dit pad nabootsen meer patiënten kunnen helpen overleven en herstellen na levensreddende longingrepen.
Bronvermelding: Li, Q., Yin, J., Lin, Q. et al. Functional remodeling of iNKT cells by sulfatide-reactive type II NKT cells reprograms alveolar macrophages to alleviate lung ischemia-reperfusion injury. Commun Biol 9, 289 (2026). https://doi.org/10.1038/s42003-026-09572-4
Trefwoorden: long ischemie reperfusie letsel, alveolaire macrofagen, natural killer T-cellen, interleukine-10, immuunmodulatie