Clear Sky Science · nl
MHC1-TIP maakt multimodale immunopeptidoomprofilering in één buis mogelijk en onthult intratumorale heterogeniteit in antigeenpresentatie
Een kijkje in de ID-kaarten van kanker
Elke cel draagt kleine moleculaire “ID-kaartjes” aan haar oppervlak die het immuunsysteem helpen beslissen of die cel gezond of gevaarlijk is. Bij kanker kunnen deze ID-kaartjes—korte eiwitfragmenten die antigenen heten—onthullen wat een tumorcel abnormaal maakt en ze markeren voor vernietiging door immuuncellen. Deze studie introduceert een nieuwe laboratoriummethode, MHC1-TIP, die het veel makkelijker en goedkoper maakt om deze ID-kaartjes te lezen uit zeer kleine hoeveelheden patiëntweefsel, en daarmee kansen opent voor preciezere kankerimmunotherapieën.
Waarom signalen aan de celoppervlakte ertoe doen
Ons immuunsysteem controleert continu cellen door te kijken naar antigenen die worden getoond op speciale moleculen genaamd MHC klasse I. Tumorcellen tonen vaak afwijkende antigenen die, in principe, door T-cellen herkend kunnen worden en kunnen worden aangegrepen met therapieën zoals gepersonaliseerde vaccins. Het daadwerkelijk meten welke antigenen aanwezig zijn in echte patiëntmonsters is echter technisch veeleisend. Traditionele methoden vereisen enorme aantallen cellen, veel verwerkingsstappen en dure antilichamen, waardoor ze slecht geschikt zijn voor kleine biopsieën of schaarse klinische monsters. Tegelijkertijd zijn tumoren niet uniform: verschillende regio’s kunnen verschillende eiwitten tot expressie brengen, wat de mogelijkheid opent dat ook antigeenpresentatie van plaats tot plaats binnen eenzelfde tumor varieert.
Een eenbuizige snelweg naar kankermoleculen
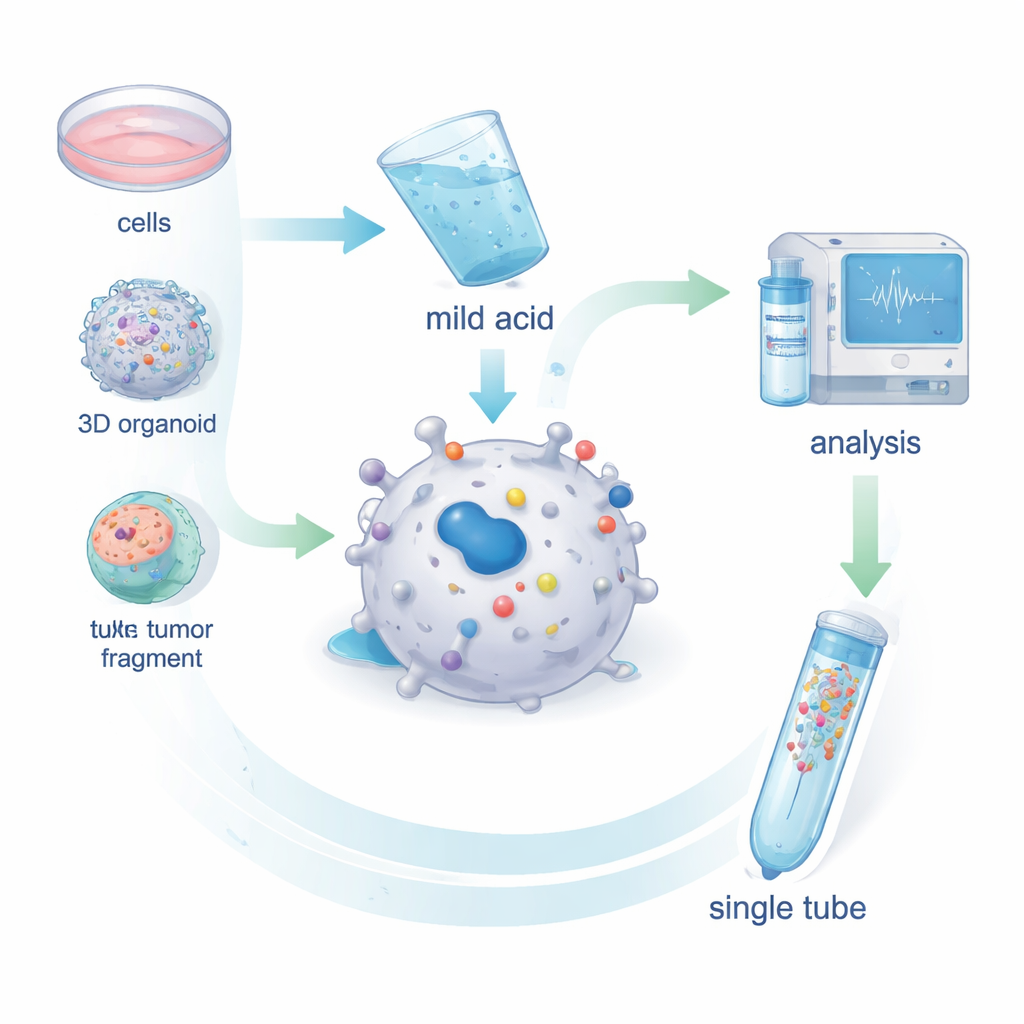
De onderzoekers ontwikkelden MHC1-TIP (MHC-I 1-Tube Immunopeptidomics) als een gestroomlijnde manier om antigenen van levende cellen te verzamelen. In plaats van cellen te lyseren en MHC-moleculen met antilichamen uit te vissen, wassen ze intacte cellen—of kleine tumorfragmenten—kort met een milde zure oplossing. Deze zachte behandeling zorgt ervoor dat de antigenen die in de MHC-groef zitten loslaten zonder de cellen te doden. De vrijgekomen peptiden passeren vervolgens een klein filter dat grotere resten verwijdert en worden gevangen op een kleinschalige kolom binnen één buis. Vandaar gaan ze rechtstreeks naar een massaspectrometer, die de peptidesequenties identificeert. Tests in melanomacellen toonden aan dat deze milde zuurbehandeling bijna alle MHC–antigeencomplexen aan het oppervlak verwijdert en dat de teruggewonnen peptiden overeenkomen met echte MHC-gebonden antigenen qua lengte en sequentiepatronen.
Meer data uit minder materiaal
MHC1-TIP is ontworpen om met zeer weinig cellen te werken en toch veel identificeerbare antigenen te leveren. Door de nieuwe workflow te combineren met een moderne massaspectrometriemodus genaamd data-independent acquisition, detecteerde het team honderden antigenen uit slechts 100.000 cellen en duizenden uit een paar miljoen cellen—een diepte vergelijkbaar met de gouden standaard van de veldaanpak met antilichamen, maar met minder materiaal en lagere kosten. De methode werkte ook op patiëntafgeleide organoïden, driedimensionale mini‑tumoren gekweekt in het laboratorium, en op kleine ex vivo tumorfragmenten kleiner dan een kubieke millimeter. Belangrijk is dat omdat de zuurwas de cellen grotendeels intact laat, het overgebleven materiaal kan worden gebruikt voor volledige eiwitprofilering van hetzelfde monster, waardoor een directe vergelijking mogelijk is tussen hoeveel van een bepaald eiwit aanwezig is en hoeveel daarvan daadwerkelijk als antigeen wordt gepresenteerd.
Verborgen verschillen binnen één enkele tumor
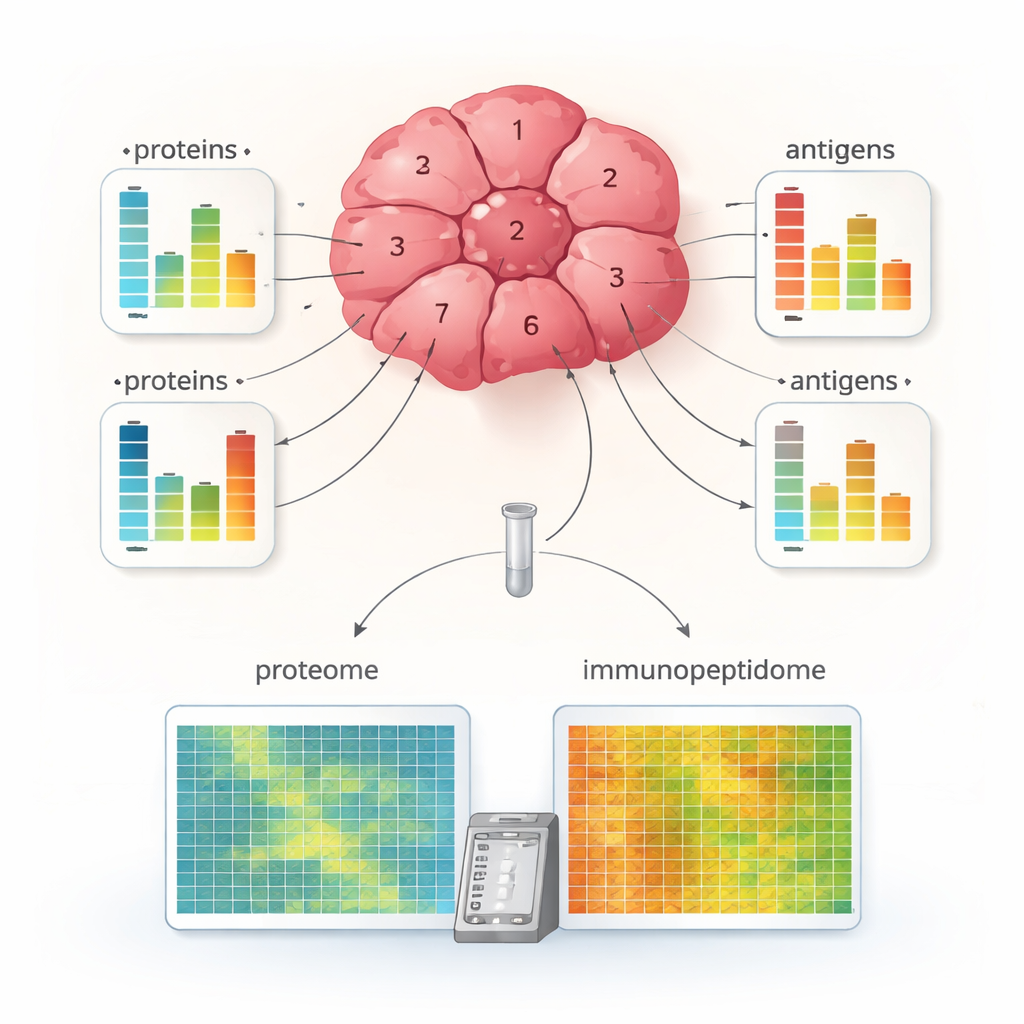
Toepassing van MHC1-TIP op meerdere kleine fragmenten uit verschillende regio’s van een niercelcarcinoom toonde opvallende interne diversiteit aan. Sommige fragmenten lieten rijke antigeenpresentatie zien, terwijl andere zeer weinig antigenen toonden, zelfs wanneer hun totale eiwitinhoud vergelijkbaar kon zijn. Voor veel eiwitten stemden veranderingen in antigeenniveaus niet overeen met veranderingen in hun eiwithoeveelheid, wat suggereert dat antigeenverwerking en het laden op MHC-moleculen onafhankelijk worden gereguleerd van de hoeveelheid van het ouderlijk eiwit. Het team combineerde ook antigeengegevens met markers van immuuncellen en MHC‑machinerie, en identificeerde tumorregio’s die “immune-hot” waren, met hoge antigeenweergave en aanwijzingen voor actieve T‑cellen, en “immune-cold” regio’s met minder antigenen en minder opvallende immuunaanval. Dit niveau van detail was zelden mogelijk uit zulke kleine stukjes weefsel.
Wat dit betekent voor toekomstige kankerzorg
Voor niet‑specialisten is de kernboodschap dat het simpelweg meten welke eiwitten een tumor produceert niet genoeg is om te weten wat het immuunsysteem daadwerkelijk kan zien. De nieuwe MHC1-TIP methode biedt een praktische manier om de werkelijke antigeenweergave te lezen uit zeer kleine, klinisch realistische monsters, terwijl tegelijk het bredere eiwitlandschap wordt gemeten. De ontdekking dat antigeenpresentatie sterk kan variëren tussen verschillende delen van dezelfde tumor, en niet altijd de eiwitniveaus volgt, waarschuwt tegen het kiezen van vaccin- of T‑celdoelen uitsluitend op basis van gen- of eiwitexpressie. In de toekomst kunnen benaderingen zoals MHC1-TIP helpen effectievere, gepersonaliseerde immunotherapieën te ontwerpen door te focussen op antigenen die daadwerkelijk aan het oppervlak worden getoond en consistenter door de tumor heen worden gepresenteerd.
Bronvermelding: Bathini, M., Bocaniciu, D., Johnson, F.D. et al. MHC1-TIP enables single-tube multimodal immunopeptidome profiling and uncovers intratumoral heterogeneity in antigen presentation. Commun Biol 9, 296 (2026). https://doi.org/10.1038/s42003-026-09570-6
Trefwoorden: antigeenpresentatie, immunopeptidomica, kankerimmunotherapie, tumorheterogeniteit, massaspectrometrie