Clear Sky Science · nl
Herwaardering van de specificiteit tussen Gα‑eiwit en respons‑element in GPCR‑signalering
Waarom kleine schakelaars in cellen van belang zijn voor de geneeskunde
Veel van de geneesmiddelen van vandaag werken door moleculaire "schakelaars" aan het oppervlak van onze cellen om te zetten, de zogeheten G‑proteïne‑gekoppelde receptoren, of GPCR’s. Deze schakelaars geven berichten door naar het binnenste van de cel via hulp‑eiwitten die G‑eiwitten heten en zetten uiteindelijk genen aan of uit. Decennialang hebben onderzoekers eenvoudige lichtproducerende tests gebruikt om te zien welke G‑eiwitten een bepaald middel of receptor benut. Deze studie stelt een fundamentele maar cruciale vraag: vertellen die tests ons echt wat we denken — en kunnen we er nog steeds op vertrouwen bij het ontwerpen van de volgende generatie precisiegeneesmiddelen?
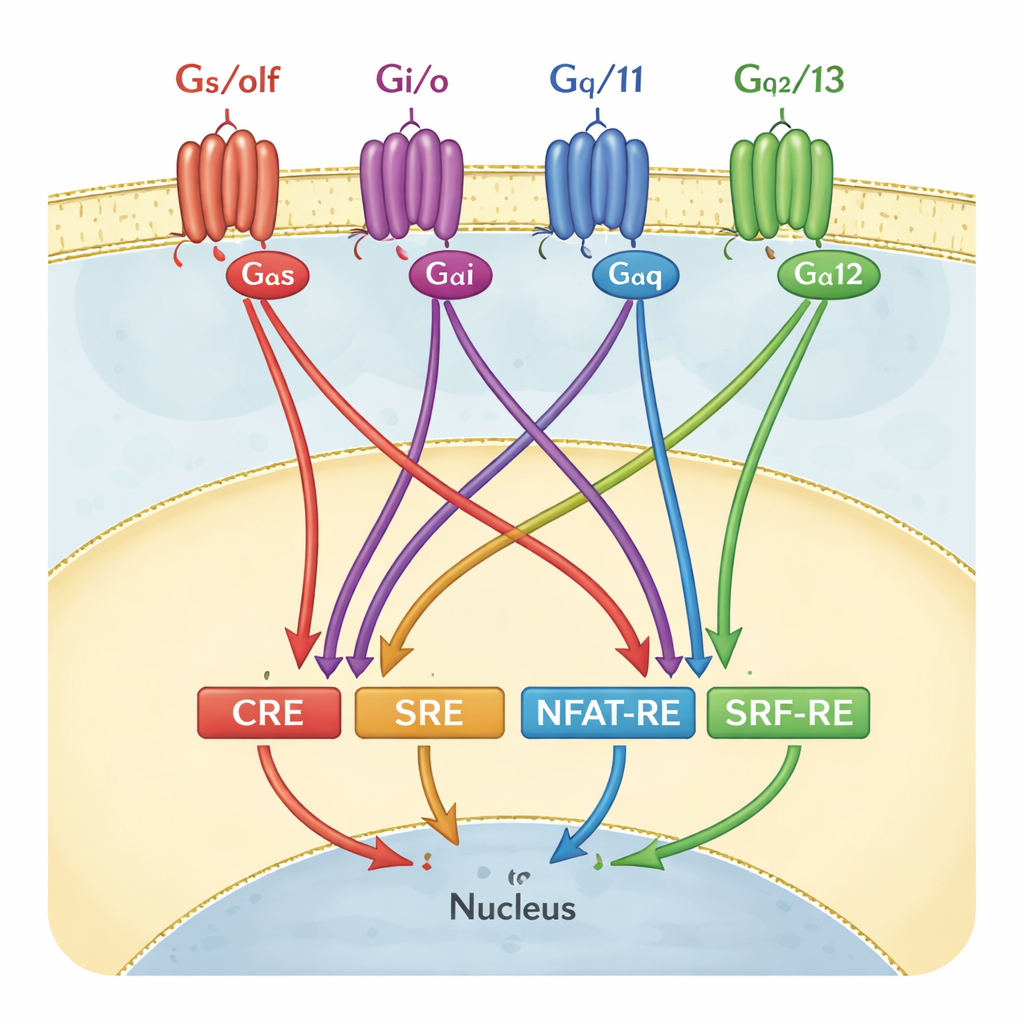
Hoe wetenschappers gewoonlijk GPCR‑signalen lezen
Om de activiteit van GPCR’s te volgen gebruiken veel laboratoria reporter‑genassays. In deze tests worden cellen zodanig gemodificeerd dat wanneer een bepaald gen‑schakelaartje, of "respons‑element", geactiveerd wordt, de cellen gaan gloeien. Vier van deze schakelaartjes zijn bijzonder populair: CRE, SRE, NFAT‑RE en SRF‑RE. Elk werd lange tijd gezien als representatief voor één tak van G‑proteïne‑signalering — bijvoorbeeld CRE voor de Gαs/olf‑familie, of SRF‑RE voor Gα12/13. In leerboeken en screeningspijplijnen worden deze koppelingen vaak bijna als eenduidige bedradingstekeningen getekend: zet een specifiek G‑eiwit aan, en slechts één reporter licht op.
De oude bedradingstest op de proef stellen
De auteurs daagden dit beeld systematisch uit met menselijk HEK293‑cellen waarin specifieke G‑eiwitfamilies — of zelfs alle G‑eiwitten — met genoomediting werden verwijderd. Daarna herintroduceerden ze individuele G‑eiwittypen één voor één. In deze cellen brachten ze negen verschillende GPCR’s tot expressie, geselecteerd om receptoren te vertegenwoordigen die heel selectief signaleren of juist via veel G‑eiwitpartners. Door te meten hoe sterk elk van de vier reporters oplichtte bij vele geneesmiddelconcentraties, konden ze zien welke G‑eiwitten echt vereist waren voor elk respons‑element en welke indirect konden bijdragen.
Overlappende paden in plaats van schone kanalen
De resultaten keren het nette één‑receptor‑één‑reporter‑model om. Hoewel CRE nog steeds hoofdzakelijk afhankelijk bleek van Gαs/olf‑eiwitten — het klassieke cAMP‑verhogende pad — konden ook andere G‑eiwitfamilies merkbaar invloed hebben op CRE‑activiteit, maar alleen wanneer Gαs/olf aanwezig was. Voor de andere drie reporters, SRE, NFAT‑RE en SRF‑RE, kwam de Gαq/11‑familie naar voren als de belangrijkste motor, ook al werden SRE en SRF‑RE traditioneel aan andere G‑eiwittakken gekoppeld. SRE en SRF‑RE gedroegen zich bijzonder vergelijkbaar, wat suggereert dat ze gebruikmaken van gedeelde downstream‑machinerie in plaats van van afzonderlijke, geïsoleerde routes. In veel gevallen leverden aanvullende G‑eiwitten zoals Gα12/13 en Gαi/o extra duwtjes of achtergrondactiviteit, wat een web van crosstalk benadrukt in plaats van aparte kanalen.
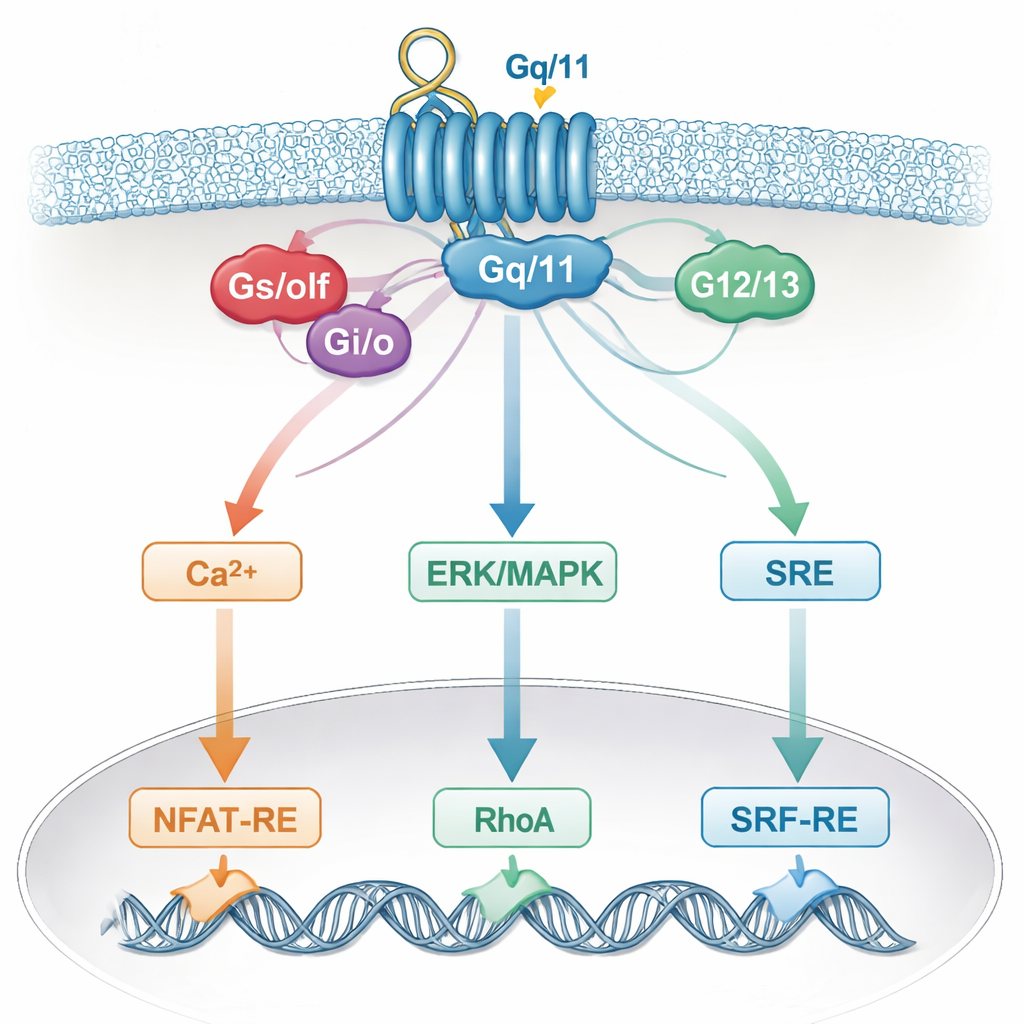
Waarom het celnetwerk onze aflezingen vervaagt
Deze vervaagde specificiteit weerspiegelt waarschijnlijk hoe echte cellen signalen integreren. Een enkele receptor kan meerdere G‑eiwitten activeren, die vervolgens samenkomen op gemeenschappelijke boodschappers zoals calcium, ERK/MAPK, RhoA of cAMP, en op gedeelde helpers zoals Gβγ‑subunits. Deze gedeelde paden voeren op hun beurt informatie naar dezelfde gen‑schakelaars in de kern. Daardoor "luistert" een reporter die men dacht dat hij op één G‑eiwitfamilie reageerde in feite naar meerdere. Celtypespecifieke factoren en de precieze set aanwezige receptoren voegen nog meer complexiteit toe, wat betekent dat conclusies uit één celsysteem mogelijk niet in een ander systeem gelden.
Wat dit betekent voor medicijnontwikkeling
Voor niet‑specialisten is de belangrijkste conclusie dat veel veelgebruikte gloeigebaseerde GPCR‑tests minder specifiek zijn dan hun labels suggereren. Ze kunnen ons nog steeds vertellen dat een receptor actief is en globaal welke brede paden betrokken zijn, maar ze zijn geen betrouwbaar bewijs dat een bepaalde G‑eiwitfamilie — en alleen die familie — betrokken is. De auteurs pleiten ervoor dat onderzoekers en geneesmiddelontwikkelaars deze reporters als grove indicatoren behandelen en ze combineren met directere methoden die eiwitten in real time laten interageren. Dat zal een eerlijker beeld geven van hoe potentiële geneesmiddelen de cellulaire signalering sturen en helpen misleidende snelkoppelingen te vermijden in de zoektocht naar veiligere, meer gerichte therapieën.
Bronvermelding: Saito, A., Kise, R., Yamaguchi, S. et al. Re-evaluating Gα protein–response element specificity in GPCR signaling. Commun Biol 9, 288 (2026). https://doi.org/10.1038/s42003-026-09569-z
Trefwoorden: GPCR‑signalering, G‑eiwitten, reporter‑assays, celsignaalnetwerken, medicijnontwikkeling