Clear Sky Science · nl
Cellulaire en isoform-selectieve G-eiwitgekoppelde receptorkinase-assays voor uitgebreide inhibitorbeoordeling
Waarom het verlagen van de cellulaire “volumeknoppen” ertoe doet
Veel van onze geneesmiddelen werken door de activiteit van celmembraanreceptoren die hormonen, neurotransmitters en medicijnen waarnemen, omhoog of omlaag te draaien. Deze receptoren moeten zorgvuldig weer worden uitgeschakeld zodat cellen niet overstimuleerd blijven; dat proces wordt gedeeltelijk geregeld door enzymen genaamd GRK’s. Wanneer GRK’s te actief zijn, zoals bij hartfalen en sommige vormen van kanker, raakt de signaaloverdracht verstoord. Deze studie ontwikkelt praktische, cellulaire tests om te meten hoe goed experimentele moleculen specifieke GRK’s kunnen blokkeren, wat onderzoekers helpt slimmere middelen te ontwerpen die deze cruciale cellulaire volumeknoppen verfijnd regelen.
Poortwachters aan het celoppervlak
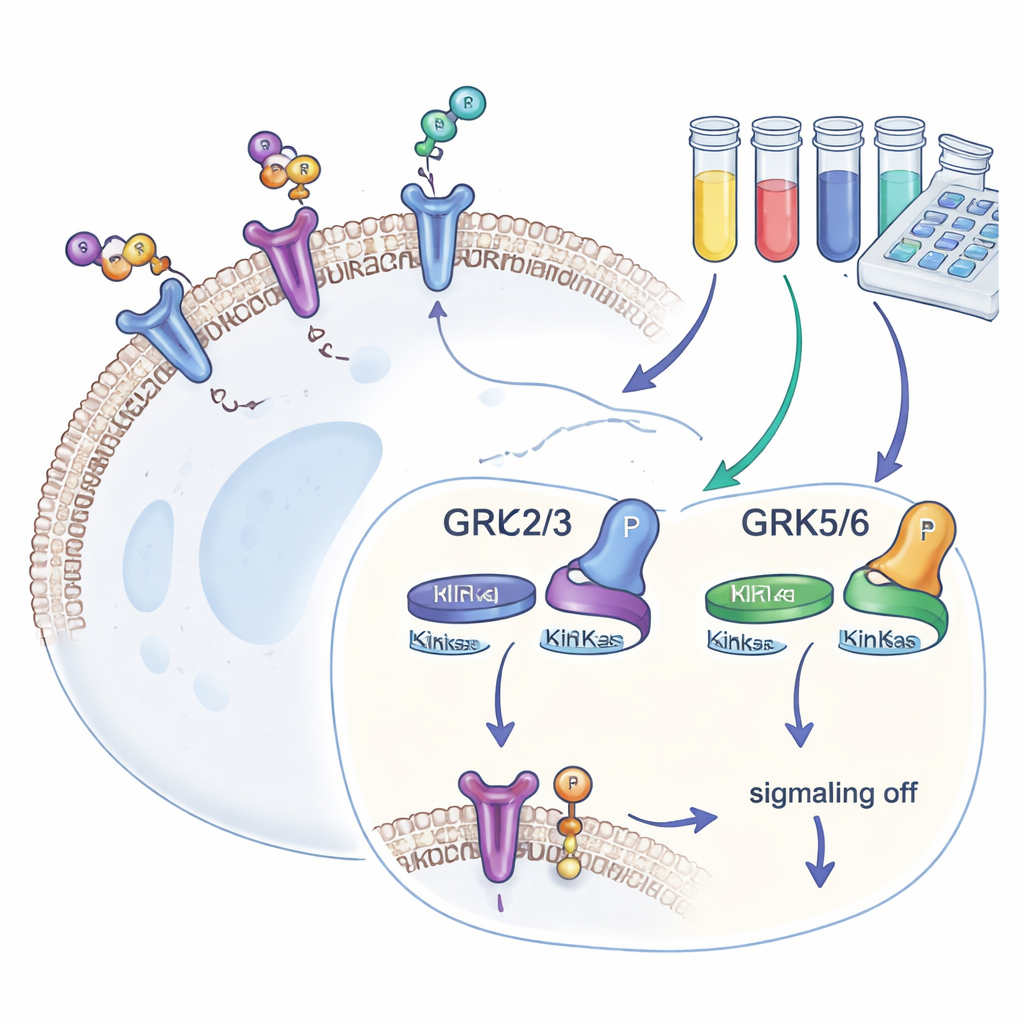
Onze cellen dragen honderden typen G-eiwitgekoppelde receptoren (GPCR’s), die signalen van buiten detecteren en omzetten in interne reacties. Nadat een GPCR is geactiveerd, hechten GRK’s kleine fosfaat-“vlaggetjes” aan zijn staart. Deze vlaggetjes trekken een ander eiwit, beta-arrestine, aan, dat verdere signaaloverdracht stopt en vaak de receptor naar binnen trekt. Vier GRK-varianten — GRK2, GRK3, GRK5 en GRK6 — worden in veel weefsels aangetroffen. Omdat ze bepalen hoe sterk GPCR’s reageren, en omdat hun niveaus veranderen bij ziekten zoals hartfalen, kanker en verslaving, zijn geneesmiddelenontwikkelaars erop gebrand GRK-blokkers te vinden die zowel krachtig als selectief zijn.
Een schoon testveld binnen cellen opbouwen
De meeste eerdere GRK-studies vertrouwden op computermodellen of buis-in-vitrochemie, die laten zien hoe stevig een remmer kan binden maar niet hoe deze presteert in het drukke binnenmilieu van een levende cel. Om deze kloof te overbruggen, hebben de auteurs menselijke HEK293-cellen geconstrueerd die alle vier de veelvoorkomende GRK’s missen en vervolgens telkens slechts één GRK-isoform opnieuw ingebracht. Elke cellijn droeg ook een goed bestudeerde receptor, de beta-2 adrenerge receptor, gemarkeerd zodat de fosforylering op een specifiek staartplaatsje (genoemd T360/S364) kon worden afgelezen met een gevoelige antilichaamgebaseerde assay. Omdat deze site alleen door GRK’s wordt gewijzigd, dient de hoeveelheid aanwezig fosfaat als een directe, kwantitatieve maat voor hoe actief elk GRK-isoform is in levende cellen.
Het onderscheid tussen goede, zwakke en onspecifieke remmers
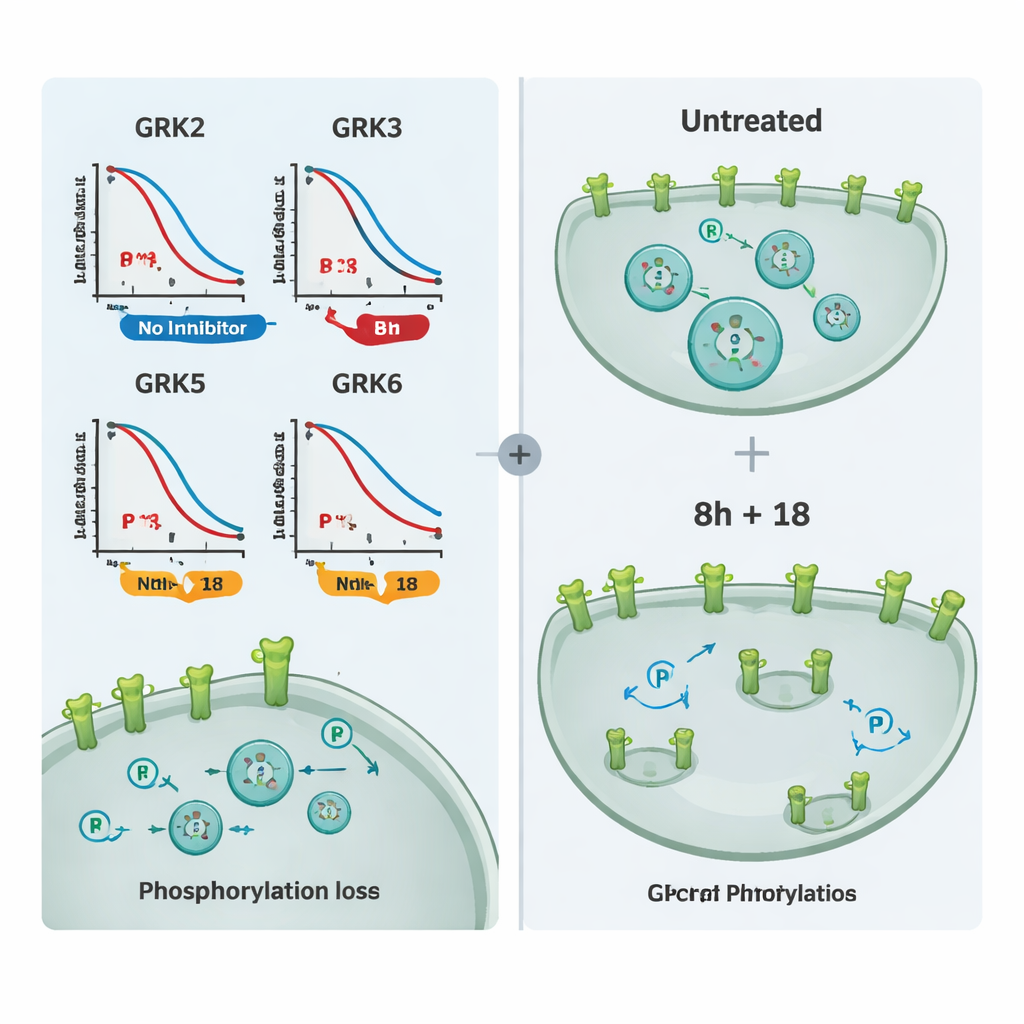
Met deze toolkit testte het team een reeks commercieel verkrijgbare GRK-remmers. Ze groepeerden eerst verbindingen die voornamelijk GRK2 en GRK3 richten, en een andere set gericht op GRK5 en GRK6. Door te vergelijken hoeveel ieder molecuul de receptorfosforylering verminderde in cellen die slechts één GRK-subtype uitdrukten, konden ze de selectiviteit in de echte wereld in kaart brengen. Eén verbinding, genoemd 8h, bleek de meest potente remmer van GRK2/3, terwijl verbinding 18 opviel door selectief GRK5/6 te remmen. Sommige veelgebruikte moleculen toonden weinig effect bij de geteste doseringen, waarschijnlijk omdat ze cellen niet efficiënt binnendrongen, en een zeer krachtige covalente remmer verstoorde de gezondheid van de cellen, waardoor deze ongeschikt was voor beeldvormende experimenten.
Van chemische vingerafdrukken naar receptorgedrag
Om aan te tonen dat deze remmers niet slechts één testreceptor beïnvloeden maar de GPCR-biologie breder, onderzochten de auteurs meerdere medisch belangrijke receptoren, waaronder de mu-opioïde receptor en de vasopressine V2-receptor. Ze maten zowel fosforylering als receptorinternalisatie met microscopie. Verbinding 8h of 18 verminderde elk op zichzelf gedeeltelijk de fosforylering en de naar binnen gerichte beweging van receptoren voor veel targets, maar de combinatie van 8h en 18 verhinderde deze veranderingen vrijwel volledig en hield receptoren aan het celoppervlak. Aanvullende experimenten die de recrutering van beta-arrestine volgden, bevestigden dat dezelfde verbindingen signalering konden bijregelen bij andere receptoren die door overlappende sets GRK’s worden gereguleerd.
Wat dit betekent voor toekomstige geneesmiddelen
Voor niet-specialisten is de kernboodschap dat de studie een betrouwbare set cellulaire tests oplevert — en twee bijzonder nuttige toolverbindingen, 8h en 18 — waarmee onderzoekers in levende cellen precies kunnen zien hoe verschillende GRK-isoformen worden teruggedraaid. In plaats van te gokken op basis van vereenvoudigde testbuisgegevens, kunnen wetenschappers nu kandidaat-remmers naast elkaar vergelijken en beslissen of ze vooral GRK2/3, GRK5/6 of alle vier tegelijk beïnvloeden. Deze helderheid zou de ontwikkeling van middelen die GPCR-signalerings preciezer moduleren versnellen, met potentiële voordelen voor de behandeling van hartziekten, kanker, pijnstoornissen en andere aandoeningen waarbij de signaalbalans verstoord is geraakt.
Bronvermelding: Blum, N.K., Kiefer, M.C., Decker, A. et al. Cell-based and isoform-selective G protein-coupled receptor kinase assays for comprehensive inhibitor evaluation. Commun Biol 9, 287 (2026). https://doi.org/10.1038/s42003-026-09568-0
Trefwoorden: GPCR-signalerings, GRK-remmers, beta-adrenerge receptor, cellulaire assay, geneesmiddelenonderzoek