Clear Sky Science · nl
HBP1 versterkt progesteronreceptoractiviteit en IGFBP1-expressie en stimuleert endometriumdecidualisatie
Waarom dit belangrijk is voor vruchtbaarheid
Wanneer een zwangerschap begint, kan het embryo zich alleen in de baarmoeder nestelen als het slijmvlies van de baarmoeder een cruciale omvorming heeft ondergaan die decidualisatie wordt genoemd. Veel gevallen van onverklaarde onvruchtbaarheid en herhaalde mislukte embryo-overdrachten blijven onbegrepen, en toenemend bewijs suggereert dat de fout vaak in deze omvorming ligt in plaats van in het embryo zelf. Deze studie onthult een tot nog toe ondergewaardeerde moleculaire "schakelaar", een transcriptiefactor genaamd HBP1, die helpt het baarmoederslijmvlies voor te bereiden op implantatie en nieuwe mogelijkheden kan bieden om implantatieproblemen te diagnosticeren en te behandelen.
Een verborgen schakelaar in het baarmoederslijmvlies
Het binnenste slijmvlies van de baarmoeder, het endometrium, verandert ritmisch met elke menstruatiecyclus. Onder invloed van oestrogeen groeit het, en onder progesteron rijpt het tot een ontvankelijk bed voor een embryo. In dit werk richtten de onderzoekers zich op humane endometriumstromale cellen, de structurele cellen die tijdens de implantatie transformeren in grotere, meer secretorische deciduale cellen. Door bestaande genexpressiegegevens te analyseren en nieuwe experimenten uit te voeren, vonden ze dat HBP1-niveaus sterk stijgen zodra deze stromale cellen aan decidualisatie beginnen, wat suggereert dat HBP1 deel uitmaakt van het ingebouwde timingmechanisme dat de baarmoeder klaarmaakt.
Helpen cellen van vorm te veranderen en langzamer te worden
Om te testen of HBP1 slechts aanwezig is of daadwerkelijk nodig, varieerden de onderzoekers de HBP1-niveaus omhoog en omlaag in gekweekte humane endometriumstromale cellen. Wanneer HBP1 werd verlaagd, daalden klassieke decidualisatiemarkers zoals IGFBP1, FOXO1 en prolactine zowel op RNA- als op proteïneniveau. De cellen ondergingen ook niet de gebruikelijke morfologische verandering van slanke, spilvormige cellen naar bredere, polygonale cellen en bleven in plaats daarvan doorgaan met delen. Bij verhoging van HBP1 stegen de IGFBP1-niveaus en vertraagde de celdeling. Samen tonen deze bevindingen aan dat HBP1 cellen helpt de groeimodus te verlaten en de gespecialiseerde deciduale toestand in te gaan die vroege zwangerschap ondersteunt.
Fijnregelen van hormoonsignalen binnen de cel
Progesteron en zijn receptor zijn cruciaal voor de voorbereiding van de baarmoeder, maar niet alle weefsels reageren even goed op het hormoon. De onderzoekers ontdekten dat progesteronsignalering zelf HBP1-niveaus verhoogt, waardoor een positieve feedbacklus ontstaat. Opvallend was dat het verlagen van HBP1 niet veranderde hoeveel progesteronreceptor de cellen produceerden, maar wel de activiteit dempte van belangrijke progesteronresponsieve genen, waaronder FKBP4, FKBP5, FOSL2 en co-activator SRC1. Met genoomwijde benaderingen lieten ze zien dat HBP1 nabij veel van deze genen bindt en geassocieerd is met een toename van een specifiek histonmerk, H3K4me3, dat DNA als actief markeert. In essentie schakelt HBP1 de receptor niet aan of uit; het maakt de doelgenen van de receptor gemakkelijker afleesbaar.
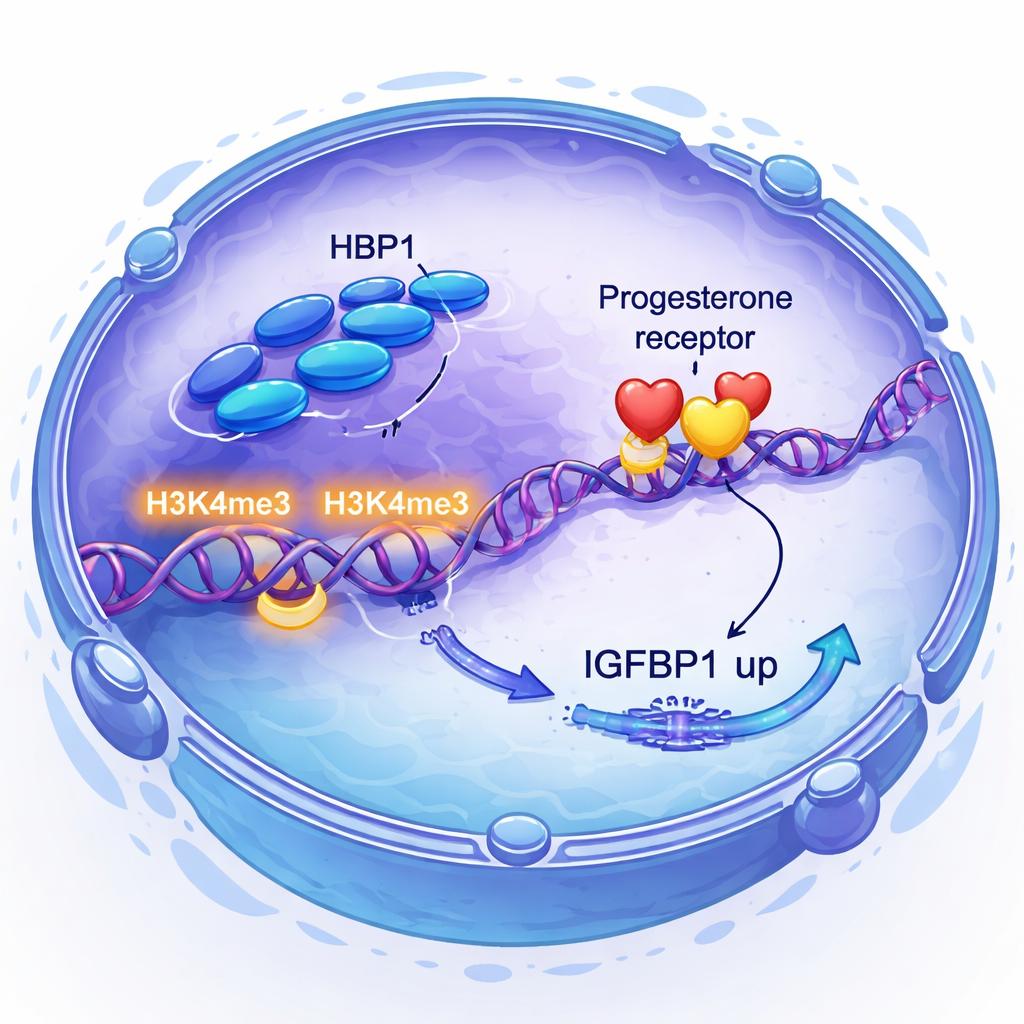
Directe controle van een sleutel-implantatiesignaal
Vervolgens vroegen de onderzoekers hoe HBP1 verbonden is met IGFBP1, een eiwit dat al lang wordt gebruikt als marker van gezonde decidualisatie en waarvan bekend is dat het de communicatie tussen embryo en baarmoeder beïnvloedt. Door RNA-sequencing te combineren met chromatin immunoprecipitation sequencing toonden ze aan dat HBP1 rechtstreeks op het promotorgebied van IGFBP1 zit en daar H3K4me3 verhoogt, wat leidt tot hogere IGFBP1-productie. Ze ontdekten ook dat het verminderen van HBP1 het PI3K–AKT-pad activeerde, een groeigerelateerd signaal dat, wanneer overactief, IGFBP1 onderdrukt. Het blokkeren van dit pad herstelde IGFBP1-niveaus. Zo ondersteunt HBP1 decidualisatie op twee manieren: door IGFBP1 rechtstreeks aan te zetten en door een groeisignaal te dempen dat anders deciduale genen zou tegenhouden.
Een moleculaire fout koppelen aan mislukte implantatie
Ten slotte bekeken de onderzoekers endometriummonsters van vrouwen met terugkerende implantatiefalen en vergeleken deze met weefsels van vruchtbare controles tijdens de midden-secretiefase, wanneer implantatie mogelijk is. Vrouwen met herhaalde falingen hadden opvallend lagere niveaus van HBP1 en diens downstream-partners IGFBP1, FKBP5 en FOSL2, hoewel de niveaus van progesteronreceptor vergelijkbaar waren tussen de groepen. Dit patroon sluit aan bij het idee van "progesteronresistentie"—het hormoon is aanwezig, maar het weefsel kan geen volledige respons geven omdat sleutelondersteunende factoren zoals HBP1 ontbreken.
Wat dit betekent voor patiënten
In begrijpelijke termen suggereert deze studie dat HBP1 functioneert als een hoofdinstelling op het bedieningspaneel van het baarmoederslijmvlies. Wanneer het correct is opgezet, helpt het progesteronsignalen hoorbaar te maken, stimuleert het cellen te stoppen met delen en zich te specialiseren, en verhoogt het de productie van implantatievriendelijke moleculen zoals IGFBP1. Wanneer HBP1 te laag is, kan het slijmvlies onder de microscoop normaal lijken maar functioneel slecht zijn, waardoor embryo's zich eenvoudigweg niet kunnen vestigen. Het begrijpen en meten van HBP1 en zijn netwerk zou artsen in de toekomst kunnen helpen vrouwen met risico op implantatieproblemen te identificeren en nieuwe behandelingen te inspireren die de ontvankelijkheid van de baarmoeder herstellen.
Bronvermelding: Guo, Y., Tian, W., Nie, C. et al. HBP1 enhances progesterone receptor activity and IGFBP1 expression driving endometrial decidualization. Commun Biol 9, 286 (2026). https://doi.org/10.1038/s42003-026-09567-1
Trefwoorden: endometriumdecidualisatie, embryo-implantatie, progesteronsignalering, onvruchtbaarheid, HBP1