Clear Sky Science · nl
Differentiële GABA-dynamiek tussen functionele hersennetwerken bij autisme
Waarom deze hersenstudie ertoe doet
Veel mensen in het autismespectrum beschrijven de wereld als overweldigend, waarbij geluiden, licht en emoties te intens of juist merkwaardig gedempt aanvoelen. Wetenschappers vermoeden dat een deel van de verklaring ligt in hoe hersencellen de balans bewaren tussen "doen" en "stop"-signalen. Deze studie onderzoekt een belangrijk "stop"-chemische stof, GABA, en stelt een praktische vraag: hoe reageert het autistische brein wanneer we dit systeem met een geneesmiddel prikkelen? Het antwoord kan helpen verklaren waarom sommige medicijnen onvoorspelbaar werken bij autisme en waarom het lastig is om de juiste dosering te vinden.
Signalen die hersenactiviteit in balans houden
Onze hersenen functioneren door een voortdurende trekvaart tussen excitatie (neuronen die vuren) en inhibitie (neuronen die remmen). GABA is het belangrijkste chemische middel dat deze remfunctie levert. Bij autisme suggereert jaren van onderzoek dat deze balans verstoord is, vooral in hersensystemen die zintuiglijke informatie verwerken zoals visie, gehoor en aanraking. Maar de meeste eerdere studies waren statisch: ze maten hersenchemie of -structuur in rust en vergeleken autistische en niet-autistische personen. Wat ontbrak, was een dynamische test van hoe het GABA-systeem daadwerkelijk reageert wanneer het door een geneesmiddel wordt uitgedaagd, vooral over de grootschalige netwerken die sensatie, beweging, aandacht en emotie ondersteunen.
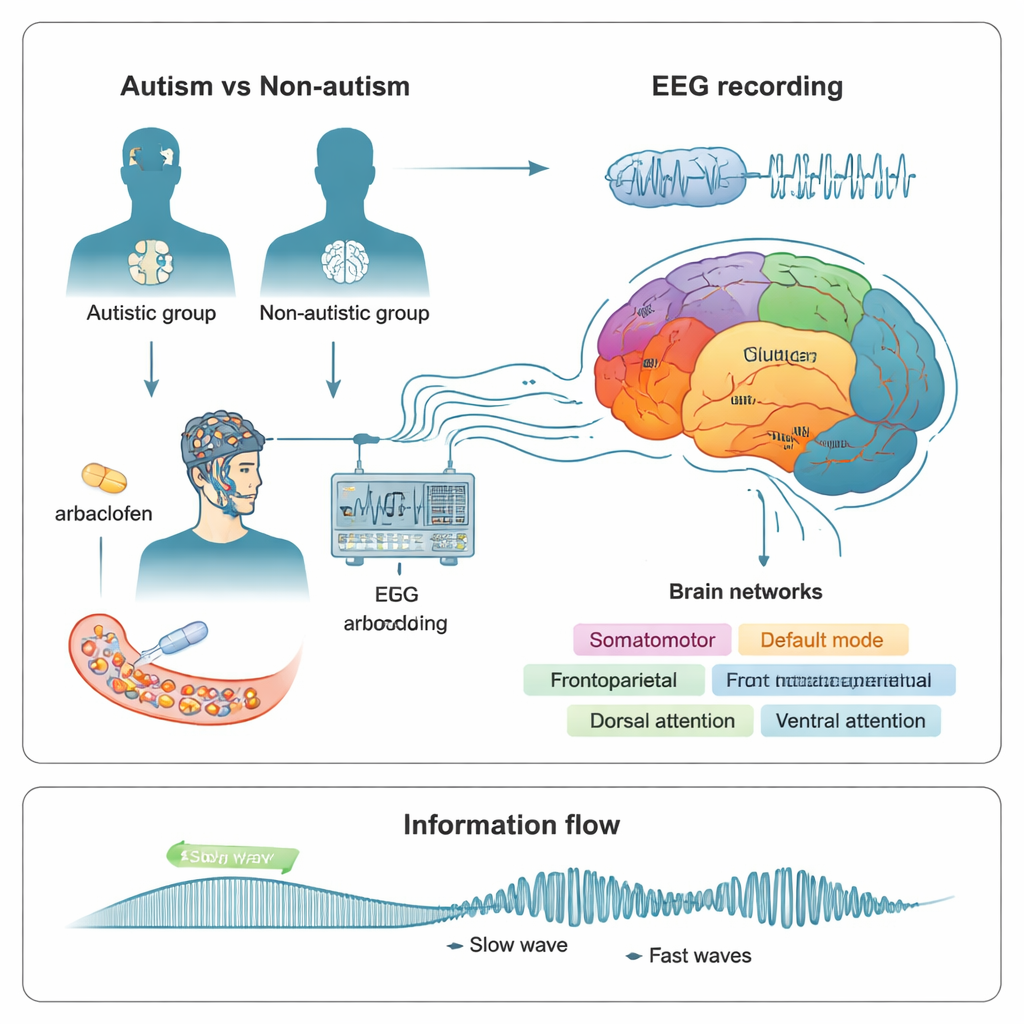
Luisteren naar hersenritmes
Om dit te onderzoeken namen de onderzoekers rustende hersenactiviteit op met EEG, dat piepkleine elektrische signalen van de hoofdhuid meet. Ze bestudeerden 24 niet-autistische volwassenen en 15 autistische volwassenen over meerdere bezoeken. Elke keer slikten deelnemers een placebo of een van twee doses (15 mg of 30 mg) arbaclofen, een geneesmiddel dat een specifiek type GABA-receptor activeert, genaamd GABAB. Ongeveer drie uur later, toen het middel actief was, registreerde het team EEG met ogen open en dicht en gebruikte computermodellen om de signalen terug te voeren naar 400 locaties over de cortex. Deze locaties werden vervolgens gegroepeerd in zeven hoofdfunctionele netwerken, waaronder visueel, somatomotorisch (beweging en aanraking), limbisch (emotie en geheugen) en verschillende hogere-orde denk- en aandachtsnetwerken.
Hoe langzame en snelle hersengolven met elkaar praten
In plaats van alleen te kijken naar hoe sterk bepaalde hersengolven waren, richtte het team zich op hoe verschillende frequenties met elkaar interageren. In gezonde hersenen helpen langzame golven die grote gebieden beslaan vaak bij het coördineren van snellere, meer lokale activiteitspulsen. Deze interactie, fase–amplitude-koppeling genoemd, kun je zien als een langzaam ritme dat "ramen" opent en sluit waarin snelle activiteit waarschijnlijker is. De auteurs maten hoe sterk langzame ritmes in banden zoals theta en alfa gekoppeld waren aan snellere beta- en gamma-activiteit, zowel binnen als tussen de zeven netwerken. Sterkere koppeling kan soms nuttig zijn, maar als die te strak of inflexibel wordt kan dat wijzen op een onbalans in hoe informatie door de hersenen stroomt.
Autistische hersenen tonen strakkere koppeling in rust
Onder placebo toonden autistische deelnemers consequent hogere koppeling tussen theta- en beta-ritmes over de meeste hersennetwerken wanneer hun ogen gesloten waren, vergeleken met niet-autistische vrijwilligers. Het limbische systeem viel op: daar waren alle vier de koppelingsmaten die het team onderzocht verhoogd, wat wijst op ongewoon sterke verbindingen tussen langzame, wijdverspreide ritmes en snelle lokale activiteit in regio’s die betrokken zijn bij emotie en geheugen. Het somatomotorische netwerk liet ook verhoogde koppeling zien tussen theta en gamma. Deze patronen ondersteunen het idee dat de excitatie–inhibitie-balans veranderd is op het niveau van dynamische hersenritmes bij autisme, vooral in zintuiglijke en emotionele netwerken.
Dosering doet ertoe—en verschillende netwerken gedragen zich anders
Toen de onderzoekers arbaclofen inbrachten, werd het beeld complexer en doseerafhankelijk. Bij autistische deelnemers verschuift de hogere 30 mg-dosis de verhoogde theta–beta-koppeling in visuele en somatomotorische netwerken richting het bereik van niet-autistische deelnemers, wat wijst op een meer typisch patroon van sensorische informatieverwerking. Netwerken van hogere orde die planning, zelfgerichte gedachten en aandacht ondersteunen veranderden echter weinig. Het limbische systeem gedroeg zich opnieuw anders: een lage dosis van 15 mg bracht de overdreven koppeling—zowel binnen het netwerk als in zijn verbindingen met andere netwerken—dichter bij de controlegroepen. Maar bij 30 mg verschenen veel van deze afwijkingen weer, en atypische limbische verbindingen met andere netwerken, zoals het somatomotorische systeem, kwamen terug. Met andere woorden: sommige emotionele circuits leken het beste te reageren op een lagere dosis en konden bij hogere doses worden overgestimuleerd.
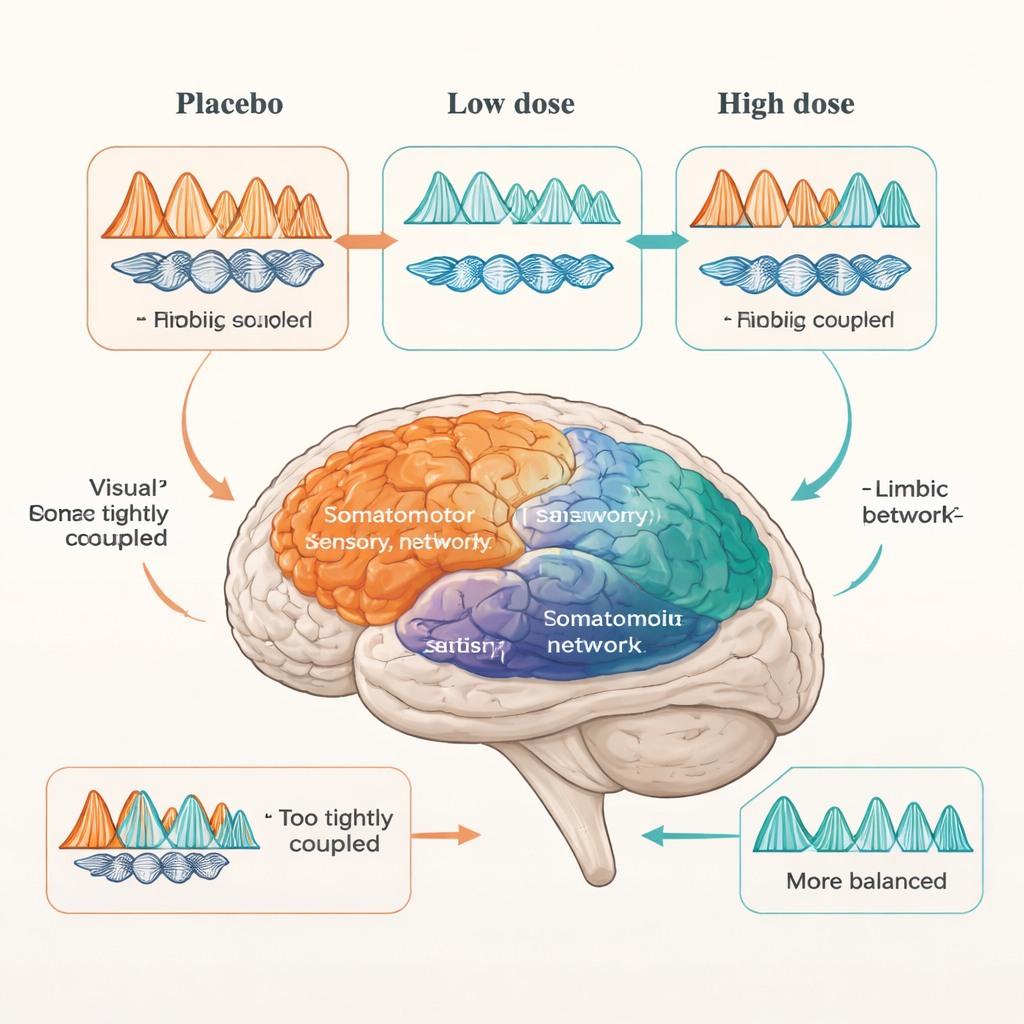
Wat dit betekent voor behandelingen in de praktijk
Voor een leek is de hoofdboodschap dat het autistische brein niet op een eenvoudige, uniforme manier reageert op GABA-werkende geneesmiddelen. Verschillende hersennetwerken—sensitieve, emotionele en hogere-denksystemen—laten onderscheidende gevoeligheidspatronen zien, en sommige circuits zijn bijzonder dosisgevoelig. Dit helpt verklaren waarom middelen die remming bewerkstelligen soms paradoxale of gemengde effecten hebben bij autisme: ze helpen op het ene domein terwijl ze een ander verstoren. Hoewel deze studie niet test of arbaclofen dagelijkse symptomen verbetert, laat ze zien dat zorgvuldig gekozen doses bepaalde autistische hersennetwerken in de richting van een meer typische activiteitsbalans kunnen sturen. Toekomstig werk kan dit soort op hersenen gebaseerde "stress-test" gebruiken om behandelingen te personaliseren, met als doel flexibelere en beter afgestemde communicatie tussen hersennetwerken te herstellen.
Bronvermelding: Huang, Q., Chen, D., Pereira, A.C. et al. Differential GABA dynamics across brain functional networks in autism. Commun Biol 9, 283 (2026). https://doi.org/10.1038/s42003-026-09563-5
Trefwoorden: autisme, GABA, hersennetwerken, EEG, arbaclofen