Clear Sky Science · nl
Radionuclide-gestimuleerde dynamische therapie veroorzaakt complementaire immunogene necroptose- en apoptose-wegenn van kankerceldood
De trucs van kanker tegen zichzelf gebruiken
Kanker staat erom bekend dat het onze beste behandelingen ontwijkt, vooral bij agressieve borstumoren die zich door het lichaam verspreiden. Deze studie onderzoekt een vindingrijke aanpak die radionuclide-gestimuleerde dynamische therapie (RaST) wordt genoemd, waarbij medische beeldvormingstracers en licht-geactiveerde nanodeeltjes worden gebruikt om kankercellen te doden op manieren die ook het immuunsysteem activeren. Voor lezers is dit belangrijk omdat het laat zien hoe bestaande beeldvormingsmiddelen en slimme materialen mogelijk hergebruikt kunnen worden om een duurzamere, door het immuunsysteem ondersteunde kankercontrole te creëren in plaats van slechts tijdelijke tumorkrimp.
Een nieuwe manier om tumoren van binnenuit op te lichten
Traditionele lichtgebaseerde kankerbehandelingen werken alleen waar een extern lichtbundel kan komen, zoals bij huid- of oppervlaktetumoren. RaST omzeilt deze beperking door een radioactieve suiker te gebruiken, vergelijkbaar met de tracer die al in PET-scans wordt gebruikt, die zich van nature ophoopt in snelgroeiende kankercellen. Terwijl deze tracer door de tumor gaat, zendt hij een zwakke blauwe gloed uit die bekendstaat als Cherenkovstraling. De onderzoekers ontwierpen kleine titaandioxide-nanodeeltjes die zijn gecoat met een eiwit dat op kanker gericht is, zodat ook zij zich naar de tumor begeven. Wanneer de tracer en nanodeeltjes elkaar ontmoeten, schakelt het interne licht de deeltjes aan, die op hun beurt pieken van reactieve zuurstofsoorten genereren—zeer reactieve moleculen die kankercellen van binnenuit beschadigen.
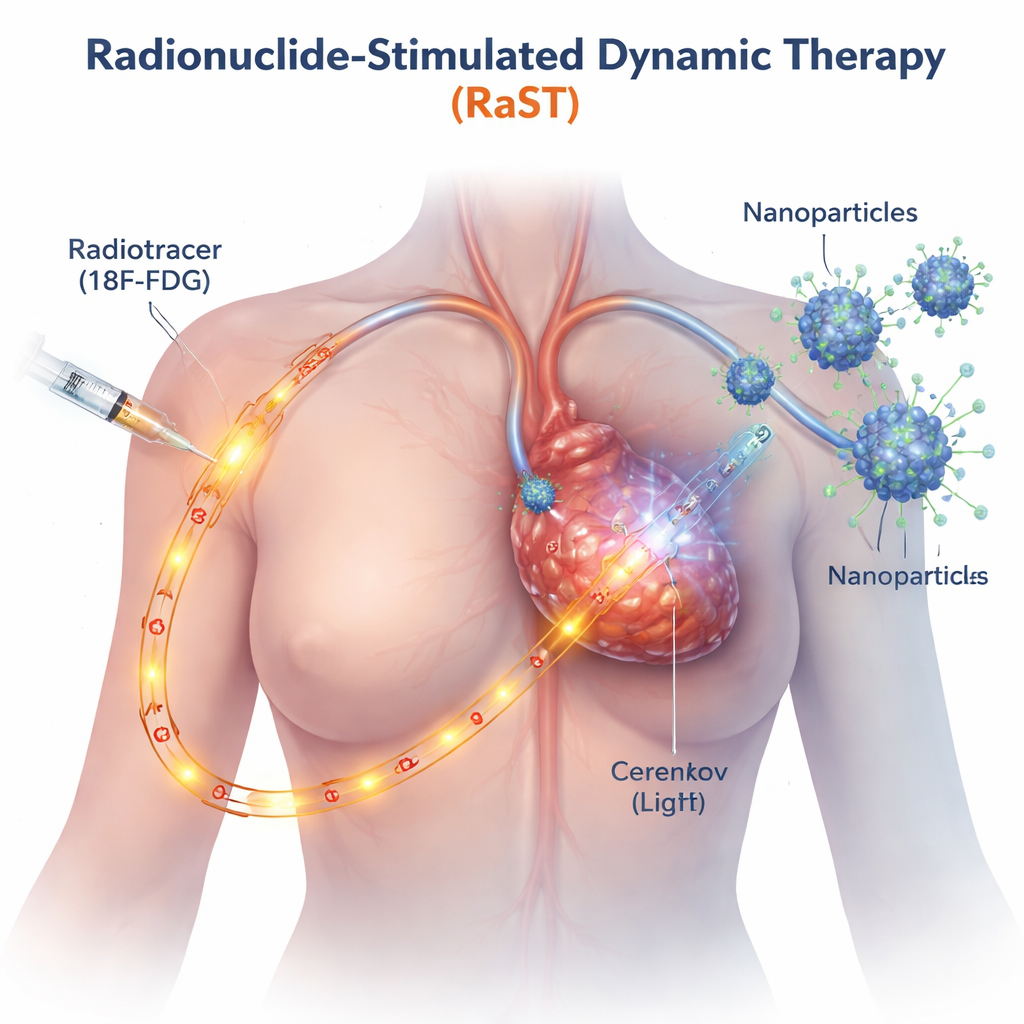
Het activeren van twee verschillende routes naar celdood
Het team wilde weten niet alleen of RaST kankercellen doodde, maar ook hoe dat gebeurde. Met behulp van verschillende agressieve borstkankercellijnen in het laboratorium vonden ze dat zorgvuldig afgestemde doses radioactieve tracer en nanodeeltjes samenwerkten om tumorcellen effectiever te beschadigen dan elk van beide componenten afzonderlijk, zelfs bij types die bekendstaan om resistentie tegen standaardchemotherapie. Gedetailleerde beeldvorming en eiwitmetingen toonden aan dat RaST tegelijkertijd twee gereguleerde programma’s van celdood activeerde. De ene was apoptose, vaak beschreven als cellulaire „zelfmoord”, waarbij cellen zichzelf op ordelijke wijze afbreken. De andere was necroptose, een explosievere vorm van celdood waarbij cellen opzwellen, barsten en moleculaire alarmtekens in hun omgeving achterlaten. Deze signalen, bekend als schade-geassocieerde moleculen en inflammatoire cytokines, kunnen fungeren als fakkels die immuuncellen aantrekken en activeren.
Het immuunsysteem inschakelen voor blijvende controle
Om te onderzoeken of deze inflammatoire manier van tumorvernietiging van belang was in levende organismen, testten de onderzoekers RaST in muismodellen van borstkanker. Bij muizen zonder belangrijke immuunverdediging deed RaST weinig om tumorgroei of uitzaaiing naar de longen te stoppen, ondanks dat er veel lokale celdood werd gegenereerd. Maar bij muizen met een intact immuunsysteem gaf dezelfde behandeling gedeeltelijke en volledige tumorresponzen en voorkwam het metastasen naar de longen. Tumoren die door RaST werden blootgesteld, raakten vol met immuuncellen—vooral myeloïde cellen zoals macrofagen en dendritische cellen—die bedreven zijn in het opnemen van dood materiaal en het presenteren van tumorfragmenten aan T-cellen. Bloedtests toonden golven van immuunstimulerende en immuunregulerende signalen in de tijd, wat suggereert dat RaST eerst een aanval op de kanker ontketent en later overgaat naar een meer gebalanceerde toestand naarmate tumoren krimpen of stabiliseren.
Verborgen resten opsporen en bescherming tegen terugval
Zelfs bij muizen waarbij tumoren aanvankelijk volledig genezen leken door RaST, onthulde een zeer gevoelige beeldstof later kleine pocketjes van resterende kankercellen verborgen in lymfeklieren. Opmerkelijk genoeg ontwikkelden deze dieren over vele maanden geen nieuwe tumoren of verre uitzaaiingen. Chemische analyses toonden aan dat de titaandioxide-nanodeeltjes, aanvankelijk overvloedig aanwezig in botten en lever, geleidelijk opnieuw werden verdeeld naar de milt en lymfeklieren—precies de knooppunten waar immuuncellen patrouilleren. Deze langzame migratie houdt waarschijnlijk een lokale bron van reactieve zuurstof beschikbaar voor immuuncellen, waardoor ze deze verborgen kankeresten kunnen herkennen en onder controle houden voordat ze opnieuw kunnen groeien of uitzaaien.
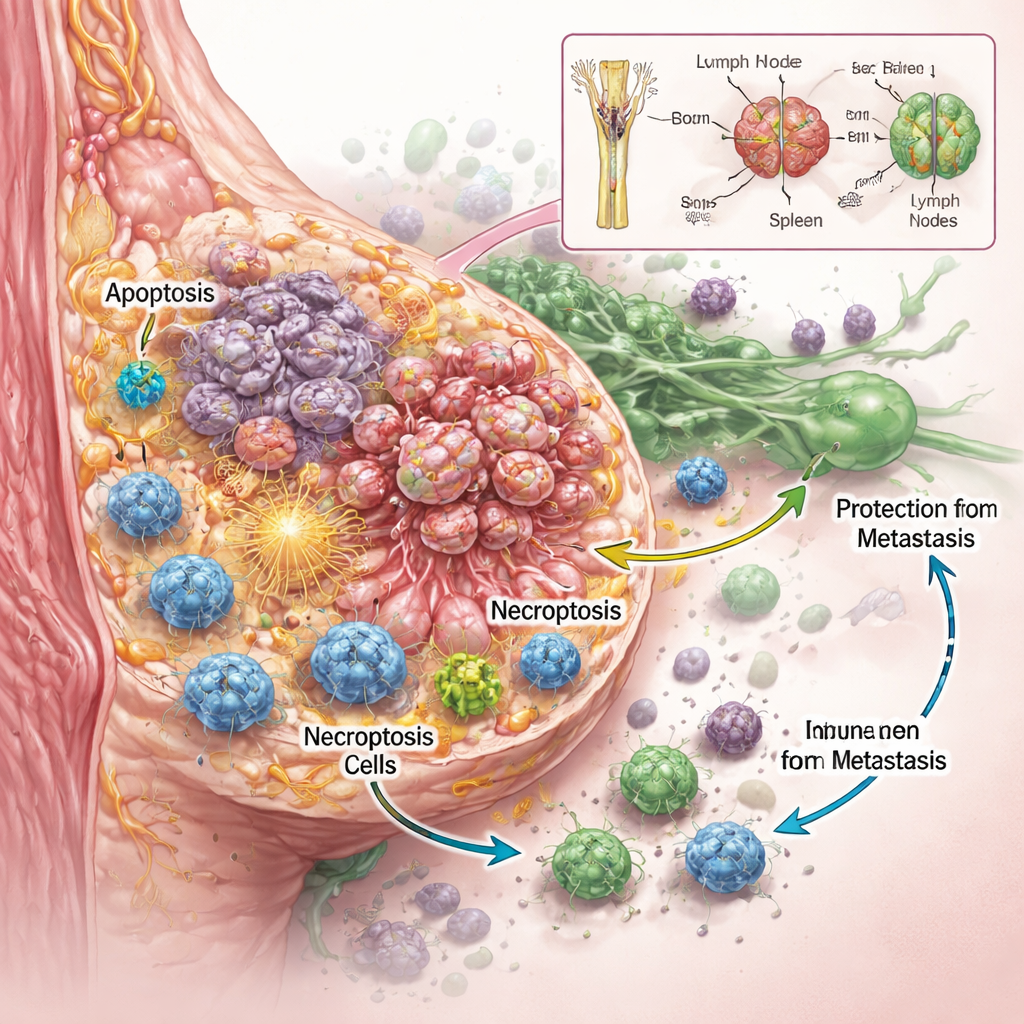
Wat dit kan betekenen voor toekomstige kankerzorg
In eenvoudige bewoordingen laat dit werk zien dat RaST meer is dan slechts een andere manier om tumorcellen te vergiftigen. Door radioactieve tracers, lichtreactieve nanodeeltjes en het eigen afweersysteem van het lichaam te combineren, dwingt het kankercellen tot twee vormen van geprogrammeerde celdood die het immuunsysteem krachtig waarschuwen. Bij immuuncompetente dieren leidt dit tot langdurige controle van agressieve borstumoren en blokkeert het metastasering, zelfs wanneer een paar kankercellen achterblijven in lymfeklieren. Hoewel er nog veel gedaan moet worden voordat deze benadering breed bij mensen kan worden getest, wijst de studie op toekomstige behandelingen die niet alleen tot doel hebben tumoren te verkleinen, maar de relatie tussen kanker, celdood en immuniteit hervormen zodat het lichaam kan helpen de ziekte op de lange termijn onder controle te houden.
Bronvermelding: Egbulefu, C., Black, K., Su, X. et al. Radionuclide-stimulated dynamic therapy induces complementary immunogenic necroptosis and apoptosis cancer cell death pathways. Commun Biol 9, 275 (2026). https://doi.org/10.1038/s42003-026-09555-5
Trefwoorden: borstkanker, nanodeeltjes, immunotherapie, radionuclide-therapie, necroptose