Clear Sky Science · nl
Glycofagie is een oud bilateraal pad dat metabole aanpassing ondersteunt via structurele evolutie van STBD1
Hoe oesters verborgen energietrucs onthullen
Dieren overleven moeilijke tijden door opgeslagen brandstof aan te spreken, maar ze vertrouwen niet allemaal op hetzelfde soort “accu”. Deze studie bekijkt pacifische oesters en toont aan dat oesters, in tegenstelling tot veel andere dieren die het van vet hebben, sterk afhankelijk zijn van opgeslagen suiker in de vorm van glycogeen. Het werk onthult een weinig bekend cellair recyclingpad — glycofagie genoemd — dat oesters helpt hun suikerreserves snel leeg te halen en weer bij te vullen, en tracëert hoe dit systeem zich door het dierenrijk heen heeft ontwikkeld.
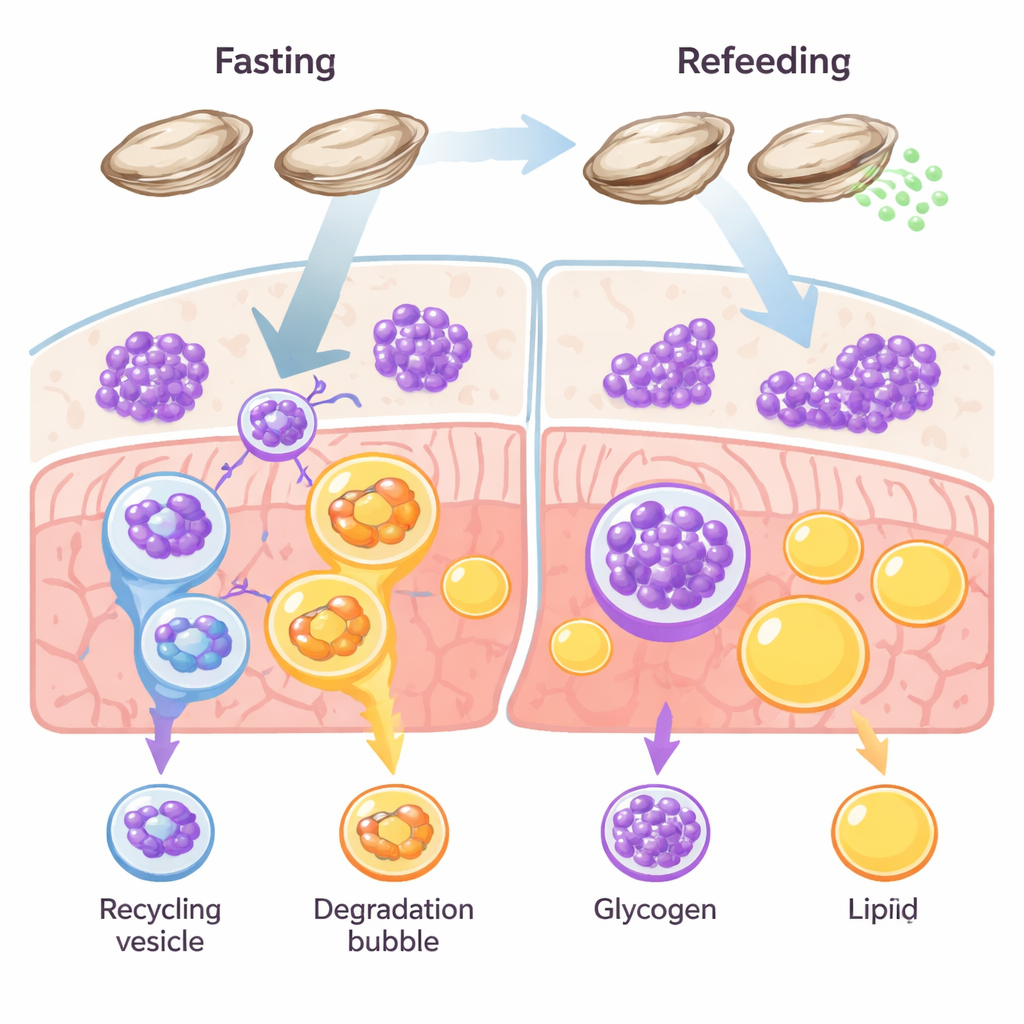
Een suiker-eerst overlevingsstrategie
De meeste dieren hanteren meerdere energieopslagmethoden, voornamelijk vet en glycogeen. Bij gewervelden zoals vissen en zoogdieren domineert gewoonlijk vet als de lange-termijnreserve. Oesters doorbreken die regel. Hun weefsels zitten vol glycogeen, en eerder onderzoek suggereerde dat deze schelpdieren suiker verbranden in plaats van vet wanneer voedsel schaars is of bij de productie van eieren en sperma. De auteurs wilden testen of glycofagie — gerichte afbraak van glycogeen binnen cellen — optreedt als een primair overlevingspad bij oesters tijdens vasten en herstel.
Cellen zien overschakelen van opslag naar verbruik
Het team liet pacifische oesters twee weken vasten en voedde ze daarna opnieuw, en volgde hoe hun weefsels in de loop van de tijd reageerden. Tijdens het vasten lieten microscopische kleuringen een toename zien van autofagie-markers — cellulaire ‘opruimsignalen’ — precies op die plaatsen waar glycogeen was opgeslagen, terwijl het glycogeen zelf afnam. Vetreserves veranderden daarentegen nauwelijks. Toen de oesters weer werden gevoerd, kwam glycogeen snel terug en daalden de autofagiesignalen. Tegelijkertijd stegen en daalden de niveaus van een sleutelreceptor-eiwit genaamd STBD1, dat glycogeen specifiek koppelt aan het autofagiesysteem, in overeenstemming met het gebruik van glycogeen. Een andere receptor die aan vetrecycling is gekoppeld, p62, bleef grotendeels constant. Samen wijzen deze patronen op een toegewijd, suikergericht recyclingpad: glycofagie, niet vetafbrekende lipofagie, doet het zware werk in het energie-evenwicht van oesters.
De moleculaire haak die glycogeen vastgrijpt
Glycofagie berust op STBD1 als een moleculaire haak: het bindt glycogeen en geeft het door aan kleine adaptereiwitten die recyclingblaasjes samenstellen. Bij oesters bleek STBD1 anders bedraad te zijn dan zijn gewervelde tegenhanger. Het oestereiwit draagt zijn glycogeen-grijpende regio, bekend als het CBM20-domein, aan de voorzijde (N-terminale kant), terwijl gewervelde STBD1 ditzelfde module aan de achterzijde (C-terminale kant) plaatsen en een extra vettige staart hebben die het aan cellulaire membranen verankert. Computermodellen en simulaties suggereerden dat de N-terminale opstelling van de oester CBM20 een sterkere, veelzijdigere greep op vertakte suikerketens geeft. Laboratoriumexperimenten bevestigden dit: gezuiverde oester-STBD1 bond glycogeen sterker dan vis- of muis-STBD1, en toen alle versies in menselijke cellen werden tot expressie gebracht, veroorzaakte het oestereiwit een scherpere daling van glycogeen tijdens geïnduceerde autofagie.
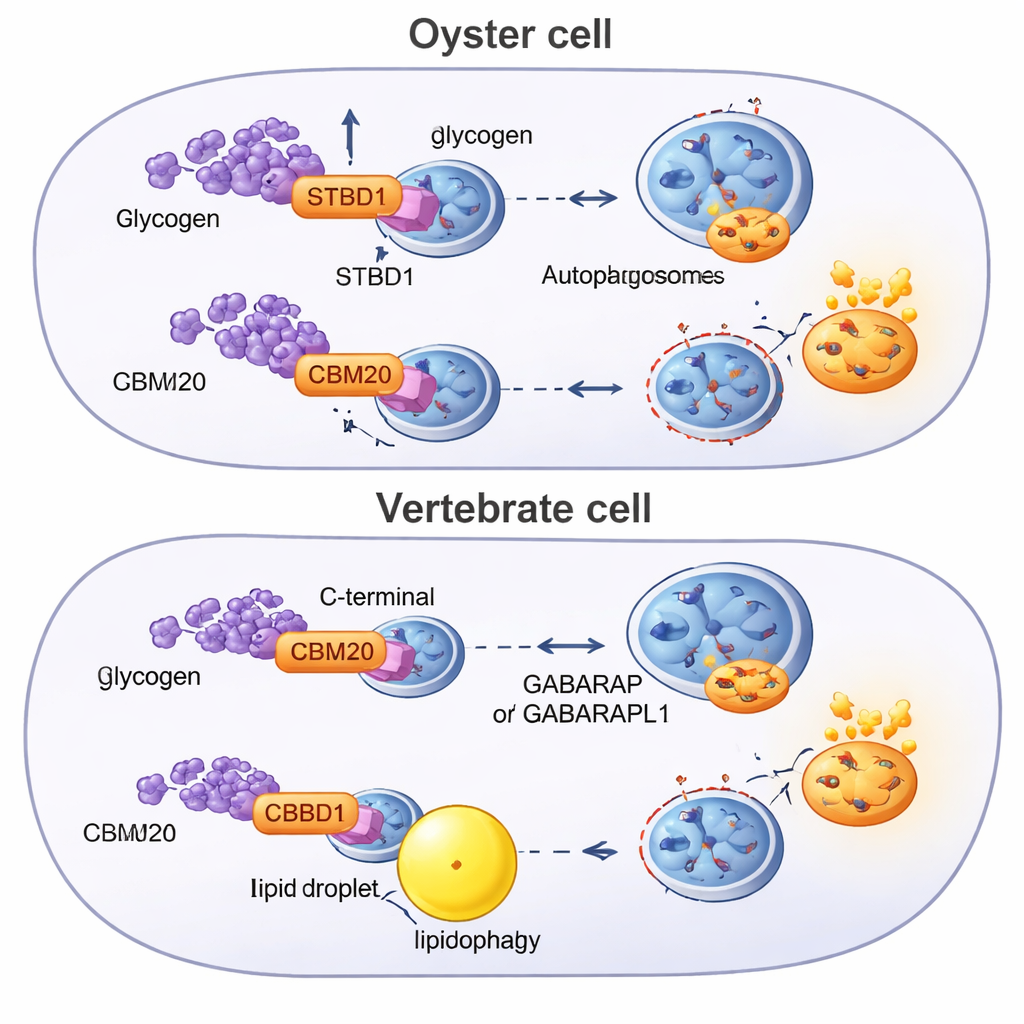
Een oud pad herschakelen in verschillende dierlijke lijnen
Om te begrijpen waar dit systeem vandaan komt, doorzochten de onderzoekers genomen van tientallen dieren op CBM20-bevattende eiwitten en bouwden evolutionaire bomen. Ze vonden dat STBD1 een bilateriale uitvinding is — verschenen in de gemeenschappelijke voorouder van dieren met een tweezijdig lichaamsplan — maar dat de structuur ervan in verschillende lijnen is herschikt. Oesters en andere lophotrochozoa behouden doorgaans het ancestrale N-terminale CBM20-ontwerp, soms met duplicaties van het suikergelsende module. Chordaten, de groep die gewervelden omvat, tonen een afwijkende versie waarin CBM20 naar de eiwitstaart is verplaatst. Deze herschikking correleert met zwakkere glycogeenzuurbinding en met een metabole strategie die meer neigt naar vetafbraak via lipofagie, ondersteund door andere autofagiereceptoren en adaptereiwitten die oesters missen.
Wat dit betekent voor de energiekeuzes van het leven
Voor niet-specialisten is de kernboodschap dat dieren meer dan één manier hebben ontwikkeld om energiegebrek te doorstaan. Oesters tonen een oude, suikergerichte strategie: een hoog-affiniteitversie van STBD1 grijpt glycogeen snel en voert het naar cellulaire recyclingunits, waardoor glycofagie een belangrijke energiebron is tijdens stress. Gewervelden lijken daarentegen een deel van die sterke suikergreep te hebben ingeruild voor een meer gebalanceerde of vetgerichte aanpak, ondersteund door andere eiwitpartners en domeinindelingen. Door gedetailleerde eiwitstructuur te verbinden met brandstofkeuzes op organismaniveau, illustreert deze studie hoe kleine moleculaire ‘herbedradingen’ verschillende takken van de dierlijke stamboom kunnen helpen zich aan te passen aan hun eigen omgevingen en levenswijzen.
Bronvermelding: Ren, L., Bai, Y., Shi, C. et al. Glycophagy is an ancient bilaterian pathway supporting metabolic adaptation through STBD1 structural evolution. Commun Biol 9, 268 (2026). https://doi.org/10.1038/s42003-026-09546-6
Trefwoorden: glycofagie, glycogeenmetabolisme, oesterbiologie, autofagie, evolutie van metabolisme