Clear Sky Science · nl
Epigenetische en metabole herschikking in metastatische feochromocytoom- en paraganglioomtumoren veroorzaakt door SDHB-mutaties
Waarom deze zeldzame tumoren ertoe doen
Feochromocytoom en paraganglioom zijn zeldzame tumoren die ontstaan uit hormoon‑producerende zenuwcellen, vaak nabij de bijnieren. De meeste groeien langzaam en zijn met chirurgie te genezen, maar ongeveer één op de vijf verspreidt zich uiteindelijk naar andere organen en wordt levensbedreigend. Deze studie onderzoekt een eenvoudige maar cruciale vraag: wat maakt dat sommige van deze tumoren gevaarlijk worden? Door diep te kijken naar hoe deze kankers hun genen aan- of uitzetten en hoe ze zichzelf van brandstof voorzien, ontdekken de onderzoekers een verborgen kwetsbaarheid die mogelijk in de toekomst met nieuwe behandelingen kan worden aangegrepen.
Van rustig groeien naar dodelijke verspreiding
Het team richtte zich op tumoren met veranderingen in een gen dat SDHB heet. SDHB helpt de mitochondriën — de energiecentrales van de cel — bij een deel van de Krebs‑cyclus, een kernroute voor energieproductie. Als SDHB beschadigd is, hoopt een stof genaamd succinaat zich op en gaan cellen zich gedragen alsof ze in lage zuurstof leven, zelfs als dat niet het geval is. De onderzoekers bestudeerden weefsel van 34 patiënten en vergeleken tumoren die gelokaliseerd bleven met tumoren die zich al hadden uitgezaaid. Met behulp van een hoogresolutie‑DNA ‘‘methylatie’’‑kaart, die laat zien hoe chemische etiketten genen harder of minder hard laten werken, vonden ze dat metastatische tumoren een sterker patroon van genonderdrukking vertoonden dan goedaardige tumoren, vooral wanneer SDHB gemuteerd was.
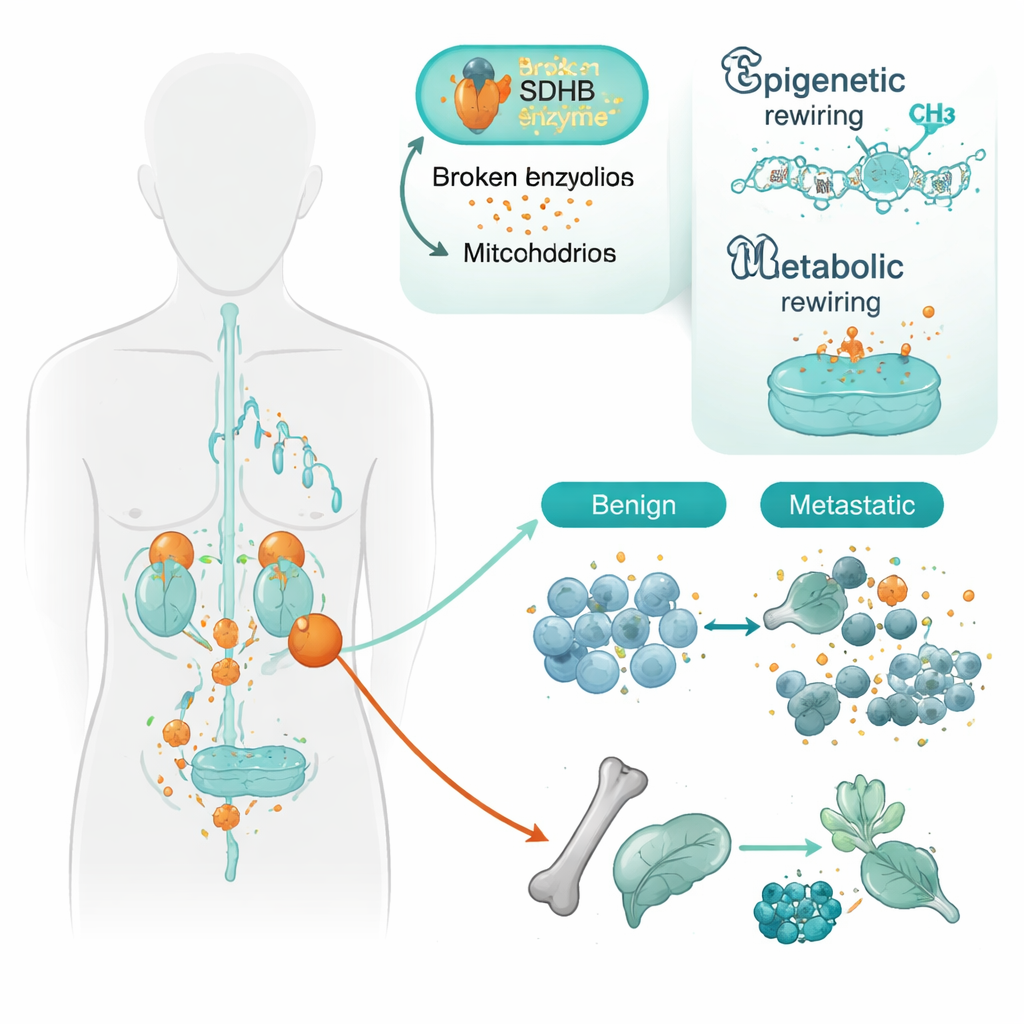
Herschrijven van celidentiteit
Veel van de genen die in agressieve tumoren werden uitgeschakeld, waren betrokken bij het laten rijpen van zenuwachtige cellen en het behoud van hun gespecialiseerde identiteit. Daartoe behoren genfamilies die sturen hoe cellen aan elkaar hechten, hun DNA organiseren en bepalen welk celtype ze worden. Een opvallend voorbeeld was het hechtingsgen PCDHGC3. Zelfs in niet‑uitzaaiende SDHB‑gemuteerde tumoren was het regelgebied van dit gen al deels uitgeschakeld; in metastatische tumoren was die onderdrukking nog sterker. Een ander gen, SATB2, betrokken bij het ordenen van grote DNA‑regio’s, werd alleen in metastatische tumoren uitgeschakeld, ongeacht SDHB‑status. Samen wijzen deze patronen erop dat verlies van SDHB cellen ‘‘primeert’’ voor een minder rijpe, mobielere toestand, en dat aanvullende epigenetische veranderingen hen vervolgens helpen los te komen en zich te verspreiden.
Herschakelen van suikerverbruik
Verrassend genoeg hielden niet alle veranderingen verband met het onderdrukken van genen. Een kleiner aantal genen raakte minder gemethyleerd en actiever, en deze waren sterk betrokken bij het transport van suikers in cellen. Daaronder viel het fructosetransportergene SLC2A5. Het eiwit daarvan, bekend als GLUT5, vervoert fructose — een suiker die veel voorkomt in fruit en in veel bewerkte voedingsmiddelen — de cel in. In laboratoriummodellen van tumorachtige cellen die aan lage zuurstof waren blootgesteld, werd SLC2A5 geleidelijk aan geactiveerd, terwijl andere suikermetingen minder consistent reageerden. De auteurs maakten daarna patiëntafgeleide celkweken van PPGL‑tumoren en toonden aan dat wanneer glucose schaars was, toevoeging van fructose deze cellen hielp om te blijven delen, vooral onder lage‑zuurstoftoestanden die de tumoromgeving nabootsen.
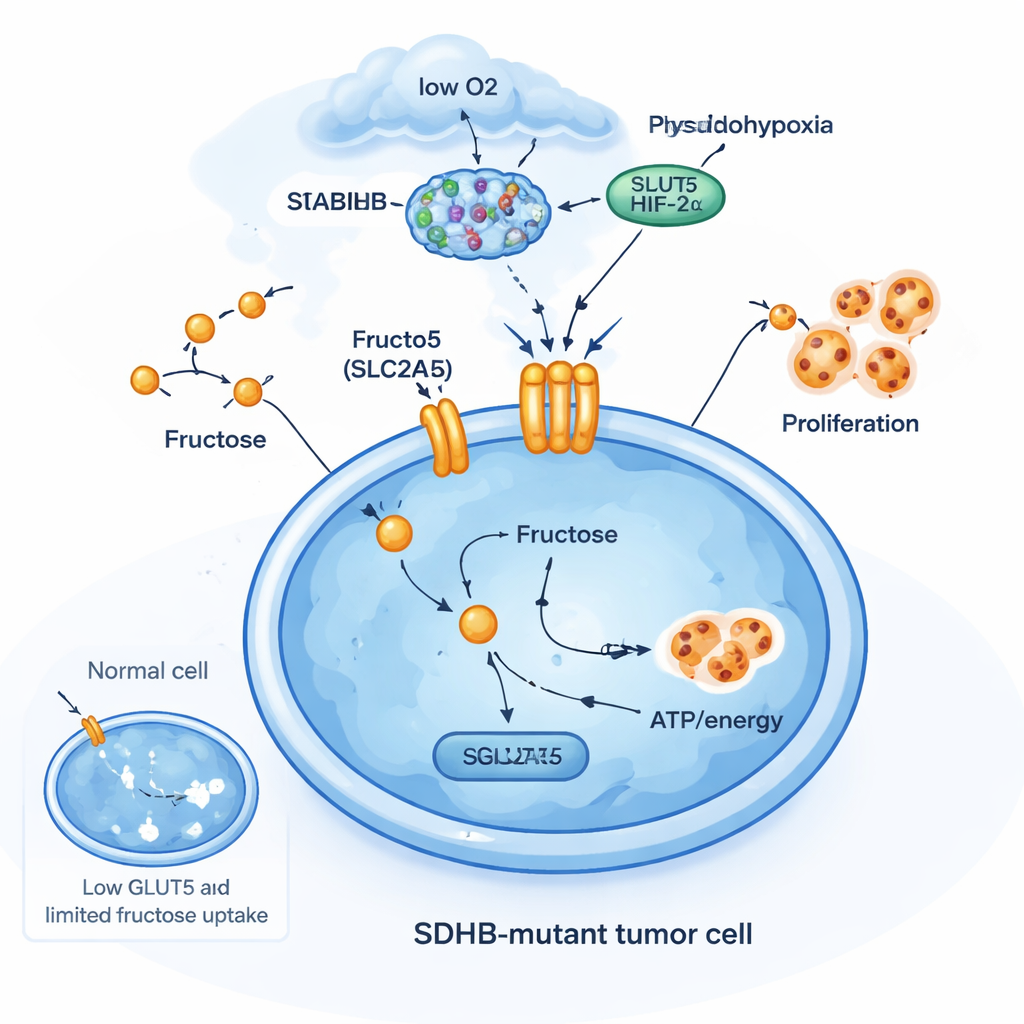
Een fructose‑gestuurde overlevingstruc
Om te begrijpen waarom SDHB‑mutaties hier van belang zijn, verwijderde het team SDHB in verschillende celtypes met genetische bewerking. In chromaffiene‑achtige cellen uit de bijnier en in een nierkankercellijn met constante activatie van de zuurstof‑sensor HIF2α verhoogde verlies van SDHB de SLC2A5‑niveaus. Maar in meer gangbare kankercellijnen die deze neuro‑endocriene of HIF2α‑kenmerken misten, schakelde dezelfde SDHB‑afknipbeweging SLC2A5 niet aan. Dit toont aan dat de fructosetransporter geen deel uitmaakt van een algemene stressrespons; het is een zeer specifieke aanpassing in bepaalde celtypen die al in een ‘‘pseudo‑hypoxische’’ toestand verkeren. In diese cellen werken SDHB‑verlies, succinaatophoping en HIF2α‑activiteit samen om een nieuw metabolisch pad te openen: opname van fructose om groei te ondersteunen wanneer zuurstof en glucose beperkt zijn.
Wat dit betekent voor patiënten
Simpel gezegd onthult de studie een dubbele verschuiving in SDHB‑gemuteerde metastatische PPGL’s. Ten eerste is hun DNA‑regelapparaat herschreven zodat cellen een minder gespecialiseerde, meer plastische toestand innemen die vatbaar is voor invasie. Ten tweede is hun energiesysteem herschikt om fructose aan te boren als alternatieve brandstof in harde, zuurstof‑ en glucosearme niches. Door de fructosetransporter SLC2A5/GLUT5 als sleutelspeler in dit proces te identificeren, wijst het werk op een mogelijke achillespees: het blokkeren van fructoseopname of ‑metabolisme zou deze tumoren selectief kunnen uithongeren terwijl de meeste normale weefsels gespaard blijven. Hoewel dergelijke therapieën nog niet beschikbaar zijn, is het in kaart brengen van dit epigenetische en metabole landschap een cruciale stap richting meer precieze, op metabolisme gerichte behandelingen voor patiënten met hoogrisico SDHB‑gemuteerde PPGL’s.
Bronvermelding: Cubiella, T., Alba-Linares, J.J., San-Juan-Guardado, J. et al. Epigenetic and metabolic rewiring in metastatic pheochromocytomas and paragangliomas driven by SDHB mutations. Commun Biol 9, 266 (2026). https://doi.org/10.1038/s42003-026-09543-9
Trefwoorden: feochromocytoom, paraganglioom, SDHB-mutatie, epigenetica, fructosemetabolisme