Clear Sky Science · nl
Multi-omische analyse van menselijke PHACTR1-signaleringsnetwerken
Waarom dit bloedvatgen voor jou van belang is
Hartaanvallen, beroertes en hoge bloeddruk houden allemaal verband met de gezondheid van onze bloedvaten. Eén gen, PHACTR1, komt herhaaldelijk naar voren in grote genetische onderzoeken naar deze aandoeningen, maar wetenschappers begrepen lange tijd niet waarom. Deze studie gebruikte een brede, "alle lagen"-benadering binnen menselijke cellen om in kaart te brengen wat PHACTR1 daadwerkelijk doet, en onthult hoe het celgroei, energiegebruik en ijzerverwerking kan beïnvloeden — processen die uiteindelijk de gezondheid van slagaders bepalen.
Een grootbeeldscan binnenin cellen
In plaats van zich te richten op één molecuul tegelijk, gebruikten de onderzoekers een strategie die multi-omics heet — waarbij duizenden RNA’s, eiwitten, kleine metabolieten en vetten (lipiden) gelijktijdig in cellen werden gemeten. Ze manipuleerden menselijke cellen zodat ze ofwel extra PHACTR1 aanmaakten of het gen minder actief hadden, waarmee ze natuurlijke genetische variaties bij mensen nabootsten. Door deze gemodificeerde cellen te vergelijken met normale controles over vier moleculaire lagen en de gegevens in geavanceerde pad-analysetools te voeren, bouwden ze een globaal kaartbeeld van hoe veranderingen in PHACTR1 doorwerken in het cellulaire machinerie. 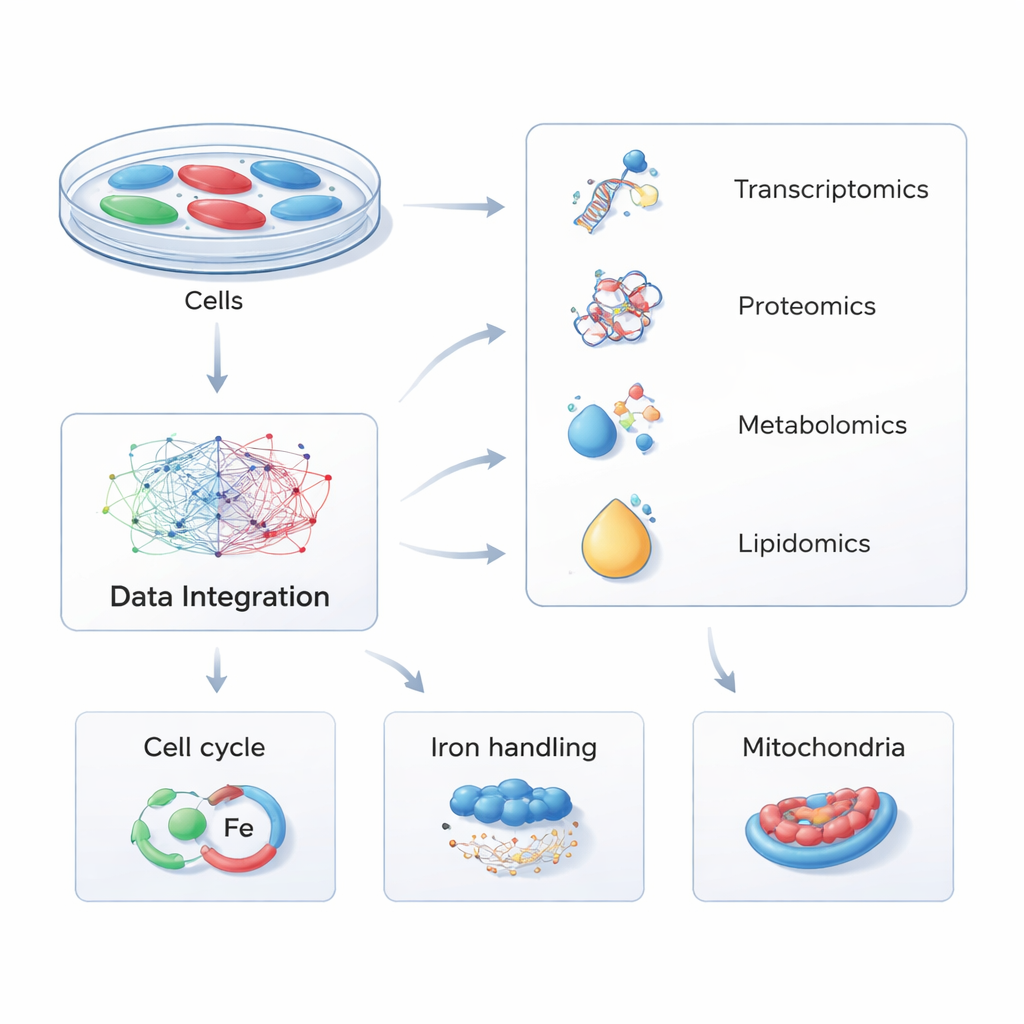
Voorbij het celskelet: controle over groeicycli
PHACTR1 stond tot nu toe vooral bekend om het helpen organiseren van het interne raamwerk van actinevezels. De nieuwe gegevens toonden aan dat het ook een stevige rol speelt in de controle van de celcyclus — de choreografie waarmee cellen hun DNA kopiëren en delen. Cellen met extra PHACTR1 versprongen uit de rustende G1-fase en stapelden zich op in fasen van DNA-replicatie en voor-deelingsfasen, terwijl minder cellen succesvol volledige mitose binnengingen. Belangrijke regelproteïnen zoals Cyclin B1, Cdt1 en andere celcyclus-eiwitten waren veranderd. Toen het team de experimenten herhaalde in primaire humane endotheelcellen — de cellen die bloedvaten bekleden — zagen ze opnieuw veranderingen in kernregelaars van de celcyclus. Dit suggereert dat PHACTR1 helpt bepalen wanneer vaatcellen rusten, delen of stagneren, een evenwicht dat cruciaal is bij zowel het repareren van vaatwanden als het ontstaan van gevaarlijke weefselovergroei.
Ijzerbeheer en bescherming tegen schade
De integratie van multi-omics wees ook op ijzergerelateerde paden en een gespecialiseerde vorm van door ijzer aangedreven celdood genaamd ferroptose. Hoewel de cellen niet actief stierven door ferroptose, verlaagde het verhogen van PHACTR1 de niveaus van belangrijke ijzer-handlingeiwitten, waaronder ferritine zware keten (de belangrijkste ijzeropslagmantel) en heem-oxygenase 1 (dat ijzer uit heem recyclet). In primaire endotheelcellen veranderde PHACTR1 deze eiwitten op vergelijkbare wijze en beïnvloedde het sleutelverdedigers tegen oxidatieve schade. Omdat slecht beheerd ijzer ontsteking, oxidatieve stress en instabiele plaques in slagaders kan aanwakkeren, suggereren deze resultaten dat PHACTR1 kan bijsturen hoe vaatcellen ijzer opslaan en ontgiften, en daarmee mogelijk iemands kwetsbaarheid voor bepaalde vaatziekten beïnvloedt.
Mitochondriën, energie en vaatgezondheid
Een andere verrassing was de rol van PHACTR1 in mitochondriën, de energiecentrales van de cel. Het team vond PHACTR1-eiwit binnen geïsoleerde mitochondriën en zag dat het veranderen van de niveaus de mitochondriale netwerkstructuur hervormde. Bij hoge PHACTR1 waren de mitochondriën meer verlengd, en een eiwit genaamd Drp1 werd chemisch aangepast op een plaats die mitochondriale splitsing vermindert. De niveaus van een scaffold-eiwit, AKAP1, dat helpt signalering aan het mitochondriale oppervlak te organiseren, stegen en daalden synchroon met PHACTR1. Deze structurele verschuivingen kwamen overeen met veranderingen in de energieproductie van de cel: veel PHACTR1 verminderde mitochondriale ATP-productie en hield verband met een ophoping van bepaalde vetzuurgerelateerde moleculen die traag vetverbranding signaleren, terwijl weinig PHACTR1 cellen meer op suikerverbranding (glycolyse) liet vertrouwen. Analyses van menselijke arteriële monsters toonden aan dat PHACTR1 en AKAP1 geneigd zijn samen actief te zijn, waarmee deze mitochondriale controlecircuits direct worden verbonden met echte bloedvaten. 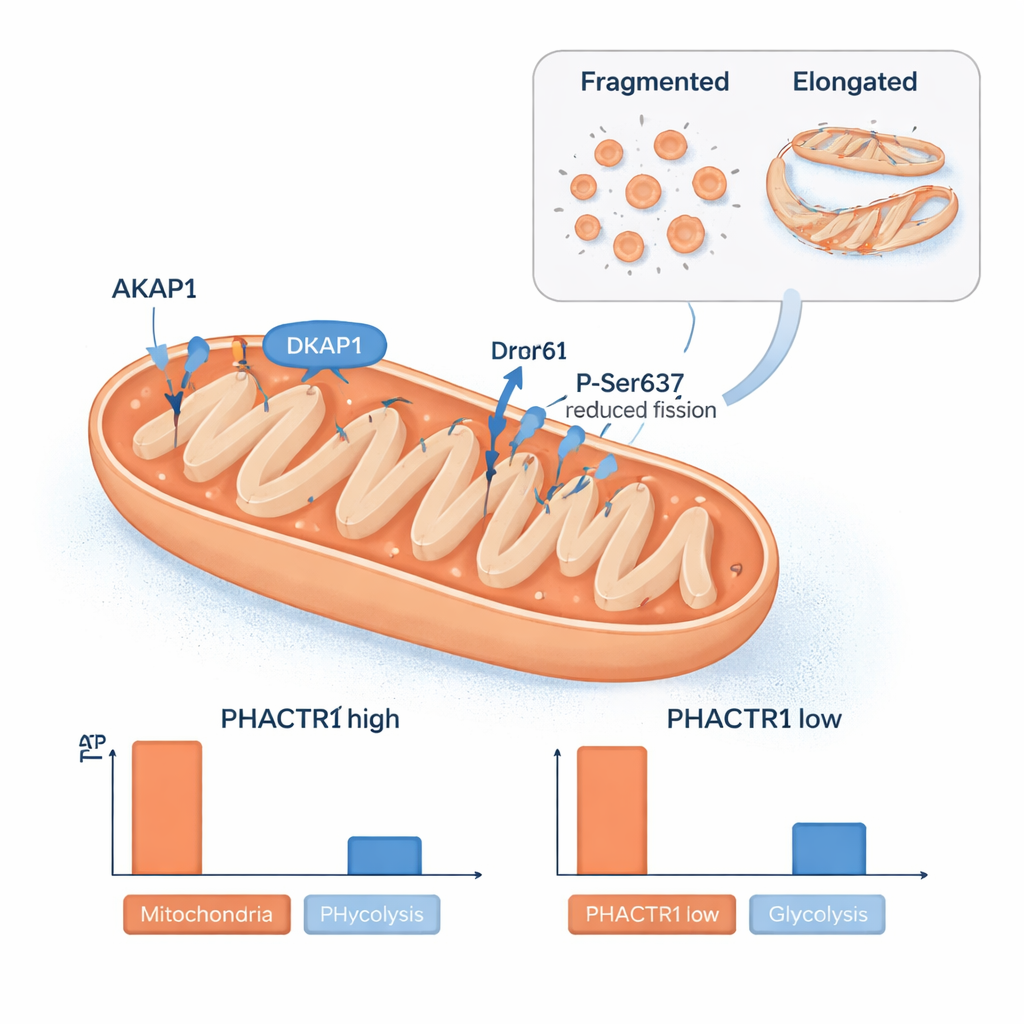
Wat dit allemaal betekent voor bloedvaten
Gezamenlijk laat dit werk zien dat PHACTR1 geen gen met één functie is, maar een meestercoördinator die raakt aan hoe vaatcellen delen, ijzer opslaan en hun energie regelen. Door deze verbindingen over duizenden moleculen in kaart te brengen, helpt de studie verklaren waarom natuurlijke verschillen in PHACTR1 gekoppeld zijn aan een breed scala aan vaatgerelateerde ziekten — van coronaire hartziekte tot spontane scheuren in slagaders en migraine. Voor niet-specialisten is de kernboodschap dat een door menselijke genetica aangeduid gen nu wordt herleid tot concrete cellulaire gedragingen die plaquegroei, vaatstabiliteit en energiebalans beïnvloeden. Op de lange termijn kan inzicht in deze door PHACTR1 aangestuurde netwerken de weg openen naar preciezere therapieën die celcycli, ijzerbeheer of mitochondriale functie in een gezondere richting sturen bij mensen met een verhoogd risico op hart- en vaatziekten.
Bronvermelding: Wolhuter, K., Ma, L., Bryce, N.S. et al. Multi-omic analysis of human PHACTR1 signaling networks. Commun Biol 9, 265 (2026). https://doi.org/10.1038/s42003-026-09542-w
Trefwoorden: PHACTR1, vaatziekte, multi-omics, mitochondriën, ijzerstofwisseling