Clear Sky Science · nl
Het remmen van PAK4 bevordert door gemcitabine geïnduceerde pyroptose bij alvleesklierkanker via de NLRP1/caspase-3/GSDME-as
Waarom het “vurige” doden van kankercellen belangrijk kan zijn
Alvleesklierkanker behoort tot de dodelijkste vormen van kanker, en zelfs onze beste chemotherapiemiddelen verliezen vaak hun effect doordat tumoren resistent worden. Deze studie onderzoekt een verrassende wending: hetzelfde middel, gemcitabine, kan kankercellen op een explosievere, ontstekingsbevorderende manier doden die pyroptose heet — mits een belangrijk moleculair “rempedaal” genaamd PAK4 wordt uitgeschakeld. Het begrijpen en richten op dit rempedaal zou bestaande behandelingen voor veel patiënten effectiever kunnen maken.
Een hardnekkige kanker die behandeling afslaat
Pancreasductaal adenocarcinoom wordt meestal laat vastgesteld en reageert slecht op therapie, waardoor gemcitabine ondanks zijn beperkingen een hoeksteen blijft. Gemcitabine doodt gewoonlijk cellen via apoptose, een ordelijke, stille vorm van geprogrammeerde celdood. Meer dan de helft van de pancreas tumoren die in deze studie werden onderzocht, produceerde echter hoge niveaus van een eiwit genaamd GSDME, dat deze stille dood kan omzetten in pyroptose — een snelle, ‘opbarstende’ vorm van celdood die het celmembraan beschadigt en ontstekingssignalen vrijgeeft. Dat riep een belangrijke vraag op: als tumoren pyroptose kunnen ondergaan, waarom zijn zo veel tumoren dan nog steeds resistent tegen gemcitabine?
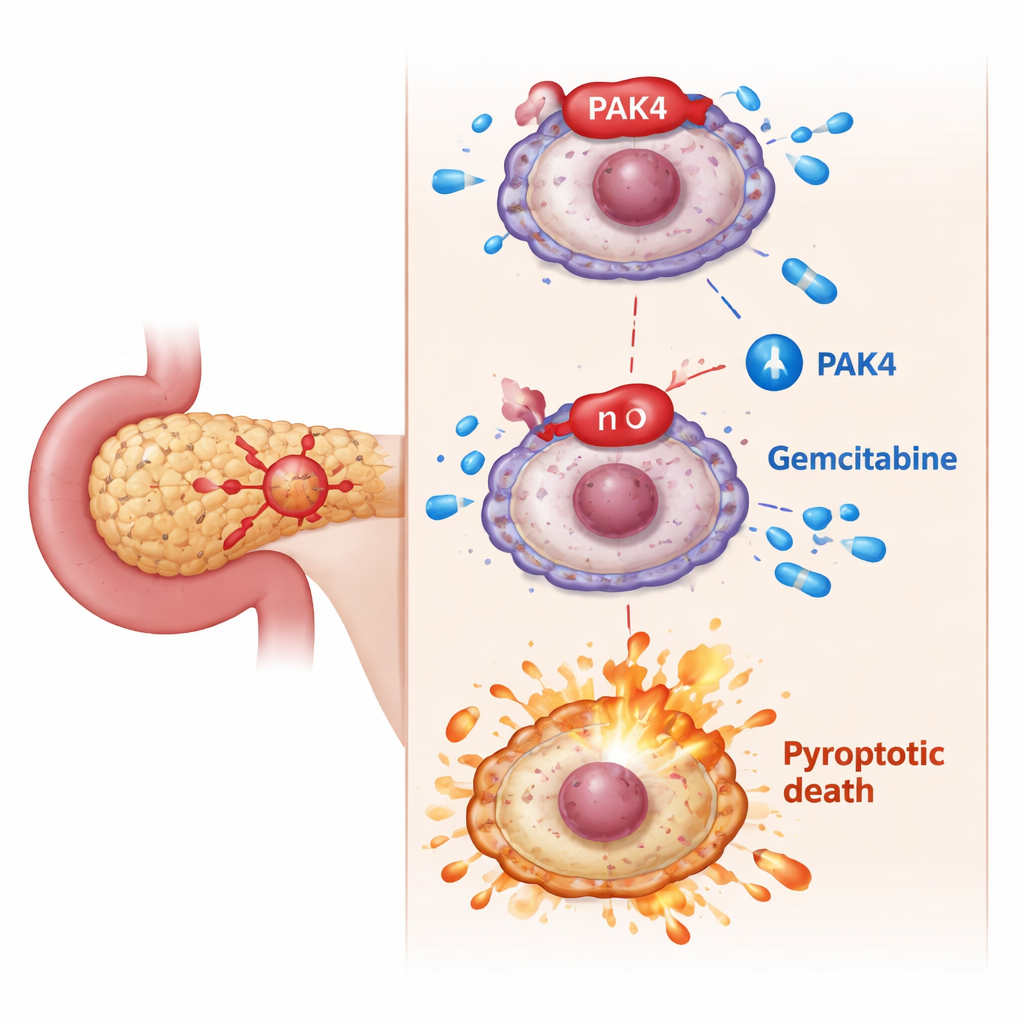
Het verborgen rempedaal: PAK4 blokkeert vurige celdood
De onderzoekers richtten zich op PAK4, een groeibevorderend eiwit dat bekendstaat als overactief bij alvleesklierkanker en gekoppeld is aan een slechte respons op gemcitabine. In celexperimenten waren kankercellen met hoge PAK4-niveaus moeilijker te doden met gemcitabine. Wanneer het team PAK4 verlaagde, werd gemcitabine plotseling veel dodelijker: cellen vertoonden klassieke pyroptotische kenmerken — zwelling, ballonachtige blaren, gescheurde membranen en verhoogde afgifte van intracellulaire inhoud. Op moleculair niveau hing deze verschuiving af van het afsnoeien van GSDME tot een actief fragment door een ander eiwit, caspase-3. Het blokkeren van caspase-3 stopte GSDME in het veroorzaken van pyroptose en bevestigde dat PAK4 gewoonlijk deze doodsroute in toom houdt.
Hoe PAK4 het alarmsysteem van de cel afbreekt
Dieper gravend vonden de wetenschappers dat PAK4 GSDME niet rechtstreeks aanvalt. In plaats daarvan saboteert het een upstream ‘alarmsensor’ genaamd NLRP1. Bij patiënten correleerden hogere NLRP1-niveaus met betere overleving, wat suggereert dat het helpt het lichaam tumoren te laten beheersen. In kankercellen leidde het weghalen van NLRP1 tot een scherpe afname van door gemcitabine geïnduceerde celdood en GSDME-activatie, wat aantoont dat NLRP1 in de pyroptose-machine voorziet. PAK4- en NLRP1-niveaus stonden in tumorstalen omgekeerd evenredig: waar PAK4 hoog was, was NLRP1 laag. De studie toonde aan dat actieve PAK4 via een ander eiwit, de E3-ligase Mdm2, NLRP1 labelt voor afbraak door het cellulair afvalverwerkingssysteem. Door NLRP1 op deze wijze te markeren, voorkomt PAK4 de activering van een ketenreactie — via caspase-9 en caspase-3 — die normaal zou culmineren in GSDME-gedreven pyroptose.
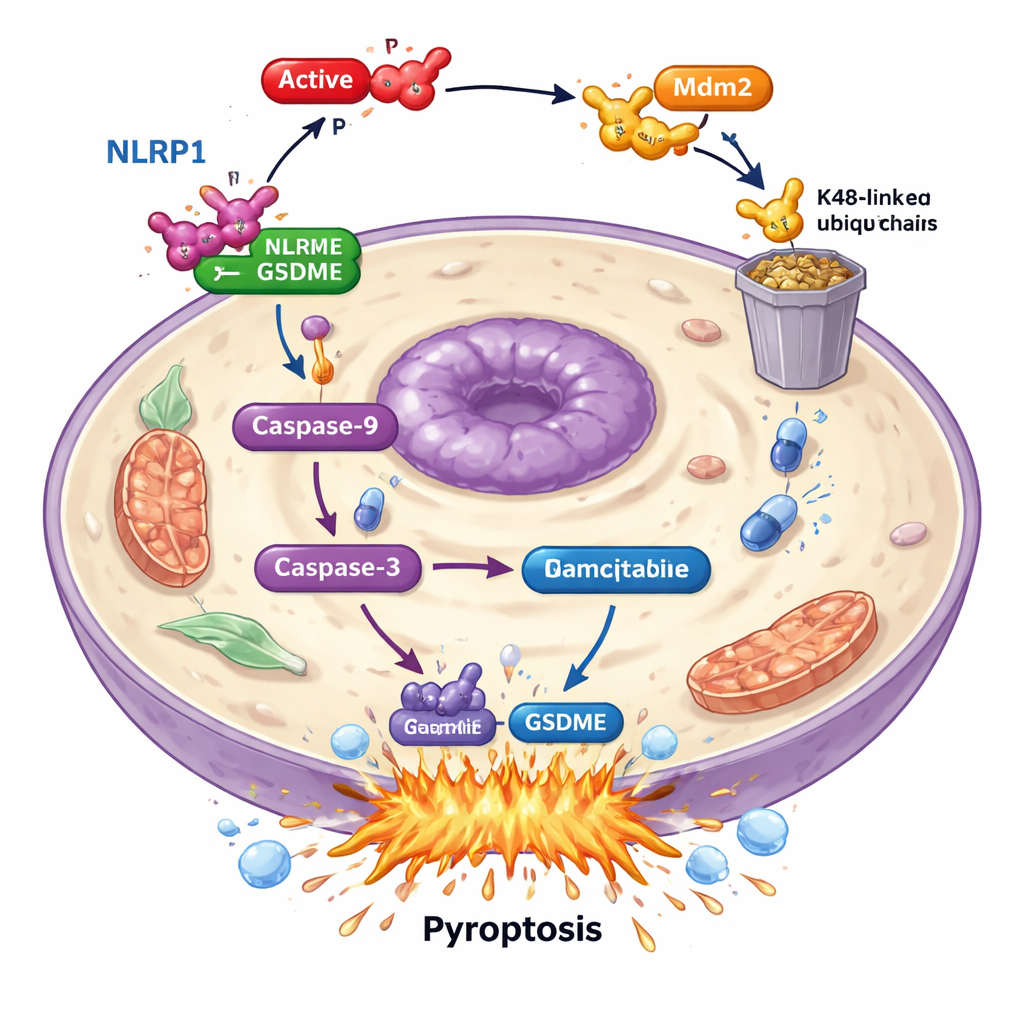
PAK4 uitschakelen om chemotherapie te versterken
Aangezien PAK4 fungeert als een rem op pyroptose, testte het team of het blokkeren van zijn activiteit de dodelijke werking van gemcitabine kon doen herleven. Ze gebruikten een klein-moleculair PAK4-remmer, PF-3758309. Alleen al deze remmer duwde pancreaskankercellen richting pyroptose, met toegenomen caspase-3-activatie, GSDME-splitsing en celmembraanruptuur. In combinatie met gemcitabine was het effect nog sterker: meer cellen stierven door pyroptose en de moleculaire signalen van de route werden versterkt. In muismodellen met humane pancreas tumoren maakte zowel het verlagen van PAK4 als behandeling met de PAK4-remmer gemcitabine effectiever in het krimpen van tumoren en verhoogde het pyroptotische merkers in de kankers.
Wat dit betekent voor patiënten en toekomstige behandelingen
Simpel gezegd onthult dit werk een moleculaire vergrendeling — PAK4 — die voorkomt dat alvleesklierkankercellen op een bijzonder destructieve manier sterven onder chemotherapie. Door PAK4 uit te schakelen, zouden artsen tumoren die met gemcitabine worden behandeld kunnen aansporen tot pyroptose, waardoor het middel effectiever wordt en mogelijk het immuunsysteem tegen de kanker wordt geactiveerd. Hoewel meer werk in patiënt-afgeleide modellen en klinische trials nodig is, schetst de studie een duidelijk stappenplan: richt op de PAK4–Mdm2–NLRP1–GSDME-route om resistente tumoren om te zetten in behandelbare tumoren, met behulp van reeds beschikbare geneesmiddelen in slimmer samengestelde combinaties.
Bronvermelding: Lu, T., Song, Y., Liang, K. et al. Targeting PAK4 promotes Gemcitabine-induced pyroptosis in pancreatic cancer via NLRP1/caspase-3/GSDME axis. Commun Biol 9, 260 (2026). https://doi.org/10.1038/s42003-026-09538-6
Trefwoorden: alvleesklierkanker, gemcitabine-resistentie, pyroptose, PAK4, gerichte therapie